-
填空题
(1)基态Fe原子有 个未成对电子,Fe3+的电子排布式为 。可用硫氰化钾检验Fe3+,形成的配合物的颜色为 。
(2)Cr位于元素周期表第_________周期第_________族,其原子核外电子排布式为 。
(3)前四周期原子序数依次增大的元素A,B,C,D中,A和B的价电子层中未成对电子均只有1个,平且A-和B+的电子相差为8;与B位于同一周期的C和D,它们价电子层中的未成对电子数分别为4和2,且原子序数相差为2。四种元素中第一电离最小的是_________,电负性最大的是________。(填元素符号)
(4)Ni2+的价电子排布图为 。
(5)3p能级上有两个为成对电子的元素形成 化合物。(填“离子”或“共价”)
高二化学填空题困难题查看答案及解析
-
(1)基态Fe原子有________个未成对电子,Fe3+的电子排布式为 ________。可用硫氰化钾检验Fe3+,形成的配合物的颜色为________。
(2)周期表前四周期的元素a、b、c、d、e,原子序数依次增大。a的核外电子总数与其周期数相同,b的价电子层中的未成对电子有3个,c的最外层电子数为其内层电子数的3倍, d与c同族;e的最外层只有1个电子,但次外层有18个电子。b、c、d中第一电离能最大的是________(填元素符号),e的价层电子轨道示意图为________。
(3)X、Y、Z、R为前四周期元素,且原子序数依次增大。XY2是红棕色气体;X与氢元素可形成XH3;Z基态原子的M层与K层电子数相等;R2+离子的3d轨道中有9个电子。
请回答下列问题:
Y基态原子的电子排布式是_____;Z所在周期中第一电离能最大的主族元素是______。
(4)基态硼原子的电子排布式为______。Ga基态原子的核外电子排布式是______。Cu+基态核外电子排布式为________。
高二化学推断题困难题查看答案及解析
-
早期发现的一种天然二十面体准晶颗粒由Al、Cu、Fe三种金属元素组成。回答下列问题:
(1)基态Fe原子有______个未成对电子,Fe3+的电子排布式为______。可用硫氰化钾检验Fe3+,形成的配合物的颜色为______。
(2)新制的Cu(OH)2可将乙醛(CH3CHO)氧化成乙酸,而自身还原成Cu2O。1mol乙醛分子中含有的键的数目为______。乙醛中碳原子的杂化轨道类型为______,乙酸的沸点明显高于乙醛,其主要原因是______。Cu2O为半导体材料,在其立方晶胞内部有4个氧原子,其余氧原子位于面心和顶点,则该晶胞中有______个铜原子。
(3)Al单质为面心立方晶体,其晶胞边长a0.405nm,晶胞中铝原子的配位数为______。列式表示Al单质的密度______ gcm-3。(阿伏加德罗常数用NA表示)
高二化学综合题中等难度题查看答案及解析
-
铁及其化合物在生活中有广泛应用。
(1)Fe2+基态的电子排布式为___。
(2)实验室用Fe3+检验苯酚。苯酚分子中碳原子的杂化方式为___。
(3)以Fe和BN为原料合成的铁氮化合物在光电子器材领域有广泛应用。
①以氨硼烷(NH3BH3)为原料可以获得BN。氨硼烷的结构式为___(配位键用“→”表示),氨硼烷易溶于水,其主要原因是___。
②以硼烷和氨气为原料可合成氨硼烷。NH3属于___分子(填“极性”或“非极性”)。
③如图为Fe与N所形成的一种化合物的基本结构单元,该化合物的化学式为___。

高二化学综合题中等难度题查看答案及解析
-
五种短周期元素A、B、C、D、E的原子序数依次增大。A和C同族,B和D同族,C离子和B离子具有相同的电子层结构。A和B、D、E均能形成共价型化合物。A和B形成的化合物在水中呈碱性,且可用来检验E的单质。
回答下列问题:
(1)五种元素中,原子半径最大的是 ,非金属性最强的是 。(填元素符号)
(2)由A和B、D、E所形成的共价型化合物中,热稳定性最差的是 (用化学式表示)。
(3)A和E形成的化合物与A和B形成的化合物反应,产物的化学式为 ,其中存在的化学键类型为 。A、C形成化合物的电子式为 。
(4)D最高价氧化物的水化物的化学式为 。
(5)单质D在充足的单质E中燃烧,反应的化学物方程式为 ;D在不充足的E中燃烧,生成的主要产物的化学式为 。
(6)单质E与水反应的离子方程式为 。
高二化学填空题困难题查看答案及解析
-
X、Y、Z、Q、T均为前四周期元素,X原子的M层上有两个未成对电子且无空轨道;Y的其中一种离子可通过硫氰化钾溶液鉴别;基态Z原子的L电子层的p亚层上有一个空轨道;基态Q原子的L电子层的p亚层上有一对成对电子;T原子的M电子层上p轨道半充满。下列叙述正确的是( )
A. 元素Y和Q形成化合物Y2Q3可溶于水
B. T有一种单质的空间构型为正四面体
C. X和Q结合生成的化合物为离子化合物
D. Z的氢化物Z2H4结构中没有双键
高二化学单选题中等难度题查看答案及解析
-
铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用。
(1)基态Fe3+的电子排布式为_________________。
(2)实验室用KSCN溶液、苯酚(
)检验Fe3+。N、O、S的第一电离能由大到小的顺序为______(用元素符号表示),苯酚中碳原子的杂化轨道类型为_______。
(3)FeCl3的熔点为306℃,沸点为315℃。FeCl3的晶体类型是________。FeSO4常作补铁剂,SO42-的立体构型是__________。
(4)羰基铁[Fe(CO)5]可用作催化剂、汽油抗暴剂等。1 mol Fe(CO)5分子中含________molσ键,与CO互为等电子体的离子是__________(填化学式,写一种)。
(5)氮化铁晶体的晶体结构示意图如图1所示。该晶体中铁、氮的微粒个数之比为_____。

(6)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe3+紧邻且等距离的Fe2+数目为_____;Fe2+与O2-的最短核间距为___________pm。
高二化学填空题困难题查看答案及解析
-
铁被誉为“第一金属”,铁及其化合物在生活中有广泛应用。
(1)基态Fe3+第M层的电子排布式为_______________________。
(2)实验室用KSCN溶液、苯酚(
)检验Fe3+。N、O、S的第一电离能由大到小的顺序为___________________(用元素符号表示),苯酚中碳原子的杂化轨道类型为____________。
(3)FeSO4常作补铁剂,SO42-的立体构型是_______________。
(4)羰基铁[Fe(CO)5]可用作催化剂、汽油抗爆剂等。1molFe(CO)5分子中含_______molσ键,与CO互为等电子体的离子是________(填化学式,写一种)。
(5)氮化铁晶体的晶胞结构如图1所示。该晶体中铁、氮的微粒个数之比为________。
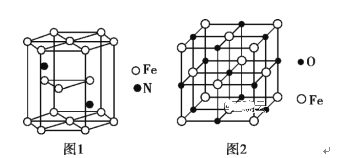
(6)氧化亚铁晶体的晶胞如图2所示。已知:氧化亚铁晶体的密度为ρg·cm-3,NA代表阿伏加德罗常数的值。在该晶胞中,与Fe2+紧邻且等距离的Fe2+数目为_________;Fe2+与O2-的最短核间距为_____________ pm。
高二化学综合题中等难度题查看答案及解析
-
铁及其化合物有重要且广泛的应用
(1)基态Fe2+的价层电子排布图为_____________
(2)检验Fe3+可以用KSCN溶液,写出SCN-的一种等电子体分子_______。
(3)部分电离能数据如下表:
元素
Mn
Fe
电离能
717
759
1 509
1 561
3 248
2 957
根据表中数据可知,气态
再失去一个电子比气态
再失去一个电子难,其原因是___________________________。
(4)过渡金属原子可以与CO分子形成配合物,配合物价电子总数符合“18电子规则”。如Cr可以与CO形成
分子:价电子总数
的价电子数
提供电子数
.Fe原子也能与CO形成配合物,其化学式为________.
(5)已知Fe单质有如图所示的两种常见堆积方式:
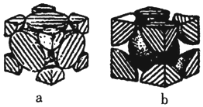
其中属于体心立方密堆积的是______
填“a”或“b”
;若单质Fe按a方式紧密堆积,设原子半径为rpm,图中晶胞的棱长为_________
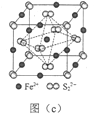
(6)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为___________g·cm−3。
高二化学综合题中等难度题查看答案及解析
-
铁及其化合物有重要且广泛的应用
(1)基态Fe2+的价层电子排布图为_____________
(2)检验Fe3+可以用KSCN溶液,写出SCN-的一种等电子体分子_______。
(3)部分电离能数据如下表:
元素
Mn
Fe
电离能
717
759
1 509
1 561
3 248
2 957
根据表中数据可知,气态Mn2+再失去一个电子比气态Fe2+再失去一个电子难,其原因是___________________________。
(4)已知Fe单质有如图所示的两种常见堆积方式:
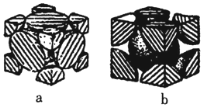
其中属于体心立方密堆积的是______填“a”或“b”;若单质Fe按a方式紧密堆积,设原子半径为rpm,图中晶胞的棱长为_________
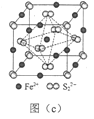
(5)FeS2晶体的晶胞如图(c)所示。晶胞边长为a nm、FeS2相对式量为M,阿伏加德罗常数的值为NA,其晶体密度的计算表达式为___________g·cm−3。
高二化学综合题困难题查看答案及解析