-
按原子序数递增的顺序(稀有气体除外),对第三周期元素性质的描述正确的是( )
A. 原子半径和离子半径均减小
B. 氧化物对应的水化物碱性减弱,酸性增强
C. 单质的晶体类型金属晶体、原子晶体和分子晶体
D. 单质的熔点降低
高二化学单选题中等难度题查看答案及解析
-
按原子序数递增的顺序(稀有气体除外),对第三周期元素性质的描述正确的是( )
A.原子半径和离子半径均减小
B.氧化物对应的水化物碱性减弱,酸性增强
C.非金属气态氢化物稳定性逐渐增强
D.单质的熔点降低
高二化学单选题中等难度题查看答案及解析
-
元素单质及其化合物有广泛用途,请根据周期表中第三周期元素相关知识回答下列问题:
(1)按原子序数递增的顺序(稀有气体除外),以下说法正确的是________。
a.原子半径和离子半径均减小
b.金属性减弱,非金属性增强
c.氧化物对应的水化物碱性减弱,酸性增强
d.单质的熔点降低
(2)原子最外层电子数与次外层电子数相同的元素名称为___________,氧化性最弱的简单阳离子是(填离子符号)___________。
(3)已知:
化合物
MgO
Al2O3
MgCl2
AlCl3
类型
离子化合物
离子化合物
离子化合物
共价化合物
熔点/℃
2800
2050
714
191
①工业制镁时,电解MgCl2而不电解MgO的原因是______________;
②制铝时,电解Al2O3而不电解AlCl3的原因是_________________;
③写出电解Al2O3反应方程式 。
高二化学填空题困难题查看答案及解析
-
对于原子半径的理解,不正确的是
A.同周期元素(除了稀有气体元素外),从左到右,原子半径依次减小。
B.对于第三周期元素,从钠到氯,原子半径依次减小。
C.各元素的原子半径总比其离子半径大。
D.阴离子的半径大于其原子半径,阳离子的半径小于其原子半径。
高二化学选择题中等难度题查看答案及解析
-
下列曲线分别表示元素的某种性质与核电荷数的关系(Z为核电荷数,Y为元素的有关性质)。下列有关说法错误的是:
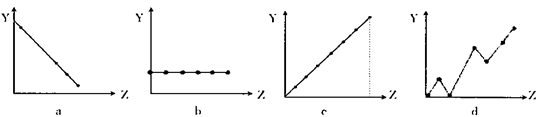
A.a图表示第三周期元素的原子半径(稀有气体除外)
B.b图表示ⅡA族元素的最外层电子数
C.c图表示第三周期元素的最高化合价
D.d图表示第三周期元素单质的熔沸点
高二化学选择题简单题查看答案及解析
-
X、Y、Z都是第三周期元素,核电荷数依次增大,X的氧化物对应水化物强碱,Z的原子半径最小。据此判断下列说法不正确的是
A.X是第ⅠA元素,Z是第ⅦA元素 B.X、Y、Z三种元素的电负性逐渐减小
C.Z的最高价氧化物对应的水化物是强酸 D.X、Z形成的化合物是离子化合物
高二化学选择题简单题查看答案及解析
-
下列说法正确的是( )
A.同周期的IA族元素的金属性比IIA族的元素金属性强
B.第三周期元素的阴离子半径从左到右逐渐减小
C.VIA族的气态氢化物一定比VA族的稳定性强
D.原子晶体的熔点一定比离子晶体的高
高二化学选择题简单题查看答案及解析
-
以下有关原子结构与元素周期律的叙述中正确的是
A.第IA族碱金属元素最高价氧化物的水化物的碱性随原子序数递增而增强
B.同周期元素(除0族元素外)从左到右,原子半径和离子半径都逐渐减小
C.第ⅦA元素从上到下,其氢化物的稳定性逐渐增强
D.同主族元素从上到下,电负性逐渐增大
高二化学选择题中等难度题查看答案及解析
-
下列关于周期表中第三周期元素性质从左到右变化趋势的叙述,错误的是( )
A. 最高正价依次升高
B. 气态氢化物稳定性逐渐增强
C. 原子半径逐渐增大
D. 最高价氧化物对应的水化物碱性逐渐减弱,酸性逐渐增强
高二化学选择题简单题查看答案及解析
-
A、B、C、D、E为原子序数依次增大的五种短周期元素,其中C为第三周期简单离子半径最小的元素,0.1mol·L−1A、B、D的最高价氧化物对应的水化物溶液加水稀释时溶液的pH变化情况如图,则下列说法中不正确的是
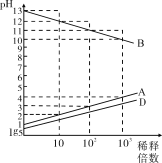
A. C制的容器可盛装A和D的最高价含氧酸的浓溶液
B. AE3、D2E2分子中所有原子最外层均达到8电子结构
C. B、D、E的单质或者化合物中都可能有能作漂白剂的物质
D. 工业上分别电解熔融的B与E、C与E形成的化合物制备B、C单质
高二化学单选题中等难度题查看答案及解析