-
(12分)
(l)当前频繁出现的雾霾天气与汽车尾气的排放有一定的关系,为了减少污染,可尝试使用汽车尾气净化装置,其原理如图所示。
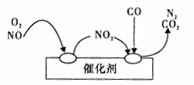
写出净化过程中的总化学反应方程式 。
(2)目前科学家也在尝试用Cu+做催化刘,将汽车尾气中NO2转化为无毒的N2,其原理如下图所示:
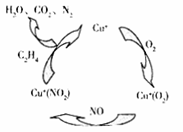
①该过程中,还原剂是 《填物质名称).
②若某辆汽车的NO排放为0.09g/km.则该车行驶100km.完成上述转化理论上需消耗乙烯的质量为 g.
(3)为探究本地区雾霾中的可溶性颗粒的成分,某化学研究性小组进行了实验探究.
[查阅资料]雾霾颗粒样品中可能含有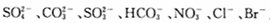 及一种常见阳离子
及一种常见阳离子 .现进行如下实脸
.现进行如下实脸

请回答下列问题:
①根据上述实验,雾霾浸取液中一定含有的离子是 _,肯定没有的离子是_ .
②若气体D遇空气会空成红棕色,则沉淀A中一定含有_ (填化学式).
-
2013年1月,我国中东部的大部分地区出现雾霾天气,许多城市的空气质量已经达到了严重污染。下列有关说法中,正确的是
A.雾霾天气仅影响出行能见度,对人体健康没有影响
B.减少化石燃料燃烧和汽车尾气排放,是减少雾霾发生的有效措施
C.当光束分别通过雾霾和豆浆时,仅豆浆可看到一条光亮的“通路”
D.气候环境报告中新增的“PM2.5”就是雾霾
-
为了减少汽车尾气对大气造成的污染,目前市场上推出了使用乙醇汽油(在汽油中加入适量乙醇)的汽车。下列叙述错误的是
A.汽车使用乙醇汽油可以减少有害气体的排放 B.乙醇汽油是可再生能源
C.乙醇充分燃烧生成CO2和H2O D.用粮食发酵可制得乙醇
-
雾霾天气是一种大气污染状态,其污染的来源多种多样,如汽车尾气、工业排放、建筑扬尘、垃圾焚烧等。
(1)汽车尾气中的NO(g)和CO(g)在一定温度和催化剂的条件下可净化。
① 已知部分化学键的键能如下
| 化学键 | N≡O | C≡O | C=O | N≡N |
| 键能(KJ/mol) | 632 | 1072 | 750 | 946 |
请完成汽车尾气净化中发生反应的热化学方程式
2NO(g)+2CO(g) N
N 2(g)+2CO2(g) ΔH= kJ/mol
2(g)+2CO2(g) ΔH= kJ/mol
② 若上述反应在恒温、恒容的密闭体系中进行,t1时刻达到平衡状态,则下列示意图不符合题意的是 (填选项序号)。

(2)t1℃下,向体积为10L的恒容密闭容器中通入NO和CO , 测得了不同时刻NO和CO的物质的量如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/×l0-2mol | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| n(CO)/×l0-1mol | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
则t1℃时该反应的平衡常数K= ,既能增大反应速率又能使平衡正向移动的措施是 。(写出一种即可)

(3)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。在氨气足量的情况下,不同c(NO2)/c(NO),不同温度对脱氮率的影响如图所示(已知氨气催化还原氮氧化物的正反应为放热反应),请回答:①温度对脱氮率的影响 ,②给出合理的解释: 。
-
近年来我国很多城市发生严重的雾霾天气,对人们的健康造成严重威胁,下列有关环境问题的说法不正确的是( )
A.改进汽车尾气净化技术,可 以减少大气污染物的排放
以减少大气污染物的排放
B.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,与肺癌、哮喘等疾病的发生的发生密切相关,是雾霾天气的主要原因
C.推广燃煤脱硫技术可以降低SO2对大气的污染
D.CO、SO2、NO、NO2都是对大气产生污染的气体,它们在空气中都能稳定存在
-
近年来我国很多城市发生严重的雾霾天气,对人们的健康造成严重威胁,下列有关环境问题的说法不正确的是
A.改进汽车尾气净化技术,可以减少大气污染物的排放
B.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,与肺癌、哮喘等疾病的发生密切相关,是雾霾天气的主要原因
C.推广燃煤脱硫技术,可以降低SO2对大气的污染
D.CO、SO2.NO、NO2都是对大气产生污染的气体,它们在空气中都能稳定存在
-
近年来我国很多城市发生严重的雾霾天气,对人们的健康造成威胁,下列有关环境问题的说法不正确的是
A.改进汽车尾气净化技术,可以减少大气污染物的排放
B.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,是雾霾天气产生的主要原因
C.推广燃煤脱硫技术,可以降低S02对大气的污染
D.CO、S02、NO、N02都是对大气产生污染的气体,它们在空气中都能稳定存在
-
近年来我国很多城市发生严重的雾霾天气,对人们的健康造成威胁,下列有关环境问题的说法不正确的是
A.改进汽车尾气净化技术,可以减少大气污染物的排放
B.PM2.5是指大气中直径小于或等于2.5微米的颗粒物,是雾霾天气产生的主要原因
C.推广燃煤脱硫技术,可以降低S02对大气的污染
D、CO、S02、NO、N02都是对大气产生污染的气体,它们在空气中都能稳定存在
-
雾霾天气是一种大气污染状态,雾霾的源头多种多样,比如汽车尾气、工业排放、建筑扬尘、垃圾焚烧,甚至火山喷发等。
(1)汽车尾气中的NO(g)和CO(g)在一定温度和催化剂的条件下可净化。反应的化学方程式为2NO(g)+2CO(g) N2(g)+2CO2(g)。
N2(g)+2CO2(g)。
①已知部分化学键的键能如下:
| 分子式/结构式 | NO/N≡O | CO/C≡O | CO2/O=C=O | N2/N≡N |
| 化学键 | N≡O | C≡O | C=O | N≡N |
| 键能(KJ/mol) | 632 | 1072 | 750 | 946 |
请计算上述反应的△H=_______________kJ/mol
②若上述反应在恒温、恒容的密闭体系中进行,并在t.时刻达到平衡状态,则下列示意图不符合题意的是_______________(填选项字母)。(下图中V正、K、n、P总分别表示正反应速率、平衡常数、物质的量和总压强)

③在T℃下,向体积为10L的恒容密闭容器中通人NO和CO,测得了不同时间时NO和CO的物质的量如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/×10-2mol | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| n(CO)/×10-1mol | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
T℃时该反应的平衡常数K=_______________,既能增大反应速率又能使平衡正向移动的措施是_______________(写出一种即可)。
(2)是硫酸工业释放出的主要尾气,为减少对环境造成的影响,采用以下方法将其资源化利用,重新获得重要工业产品硫化钙。

①写出反应Ⅰ的化学方程式_______________。
②反应Ⅱ中每生成1mol硫化钙理论上转移电子数为_______________。
③为充分利用副产品CO,设计电解CO制备CH4和W,工作原理如图所示,生成物W是_______________,其原理用电解总离子方程式解释是_______________。

-
雾霾天气是一种大气污染状态,雾霾的源头多种多样,比如汽车尾气、工业排放、建筑扬尘、垃圾焚烧,甚至火山喷发等。
(1)汽车尾气中的NO(g)和CO(g)在一定温度和催化剂的条件下可净化。
①已知部分化学键的键能如下
| 分子式/结构式 | NO/N≡O | CO/C≡O | CO2/O=C=O | N2/N≡N |
| 化学键 | N≡O | C≡O | C=O | N≡N |
| 键能(KJ/mol) | 632 | 1072 | 750 | 946 |
请完成汽车尾气净化中NO(g)和CO(g)发生反应的热化学方程式
2NO(g)+2CO(g) N2(g)+2CO2(g) ΔH=_________kJ/mol
N2(g)+2CO2(g) ΔH=_________kJ/mol
②若上述反应在恒温、恒容的密闭体系中进行,并在t1时刻达到平衡状态,则下列示意图不符合题意的是_________(填选项序号)。(下图中v正、K、n、P总分别表示正反应速率、平衡常数、物质的量和总压强)
 (2)在t1℃下,向体积为10L的恒容密闭容器中通入NO和CO , 测得了不同时间时NO和CO的物质的量如下表:
(2)在t1℃下,向体积为10L的恒容密闭容器中通入NO和CO , 测得了不同时间时NO和CO的物质的量如下表:
| 时间/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/×l0-2mol | 10.0 | 4.50 | 2.50 | 1.50 | 1.00 | 1.00 |
| n(CO)/×l0-1mol | 3.60 | 3.05 | 2.85 | 2.75 | 2.70 | 2.70 |
t1℃时该反应的平衡常数K=__,既能增大反应速率又能使平衡正向移动的措施是_。(写出一种即可)
(3)如图1所示,以N2O4为原料采用电解法可制备新型绿色硝化剂(一种氮氧化物)写出生成这种硝化剂的阳极电极反应式________________________。


图1 图2
(4)NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。在氨气足量的情况下,不同c(NO2)/c(NO)、不同温度对脱氮率的影响如图2所示(已知氨气催化还原氮氧化物的正反应为放热反应),请回答温度对脱氮率的影响____________________,给出合理的解释:____________________________________。


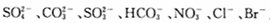 及一种常见阳离子
及一种常见阳离子.现进行如下实脸






 (2)在t1℃下,向体积为10L的恒容密闭容器中通入NO和CO , 测得了不同时间时NO和CO的物质的量如下表:
(2)在t1℃下,向体积为10L的恒容密闭容器中通入NO和CO , 测得了不同时间时NO和CO的物质的量如下表:
