-
工业上用铬铁矿生产重铬酸钾(化学式K2Cr2O,)的流程如下:
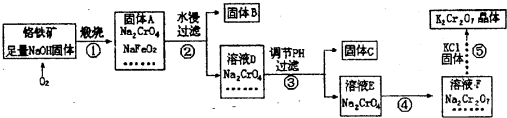
(1)固体A中,除Na2CrO4、NaFeO2、NaOH外还有______等;
(2)固体A水浸时,NaFeO2会发生强烈水解产生固体B,其化学反应方程式为______;
(3)固体C中含有2种物质,要先加入下列物质中的______,然后才能进行过滤分离.
A.氢氧化钠溶液 B.稀氨水 C.稀盐酸
(4)步骤④加入盐酸得到的溶液F中,除Na2Cr2O7外,还含有的溶质是______;
(5)在上述流程中,有氧化还原反应发生的是第______步.
(6)已知20℃时K2Cr2O7饱和溶液浓度为0.4mol•L-1,步骤⑤中加入固体氯化钾,若使K+离子浓度达到4mol•L-1(保持温度20℃),则溶液F中Cr2O2-7离子的浓度最大为______.
-
铬铁矿的主要成分的化学式为FeO·Cr2O3,还含有SiO2、Al2O3等杂质。工业上常采用固体碱熔氧化法用铬铁矿粉制备重铬酸钾,流程为:

已知:①NaFeO2遇水强烈水解;
②重铬酸钾为橙红色针状晶体,溶于水,不溶于乙醇,有强氧化性;
③2CrO42- + 2H+  Cr2O72-+ H2O
Cr2O72-+ H2O
(1)灼烧操作一般在坩埚中进行,下列物质适合用来制作此实验坩埚材料的是
A.铁 B.氧化铝 C.石英 D.陶瓷
(2)①铬铁矿经粉碎处理的目的是 。
②写出Cr2O3和纯碱、氧气反应生成Na2CrO4的化学方程式为 ;
③NaFeO2水浸时强烈水解生成氢氧化铁沉淀,离子方程式为___ ___。
(3)滤液1的成分除Na2CrO4、NaOH外,还含有(填化学式) ,
(4)通过途径Ⅰ从Na2CrO4溶液获得K2Cr2O7晶体,操作步骤有:“酸化”→加KCl固体→蒸发浓缩→操作a→过滤→洗涤→干燥。
① “酸化”步骤用醋酸调节溶液pH<5,其目的是 ;
②操作a的名称 。
-
铬铁矿的主要成分的化学式为FeO·Cr2O3,还含有SiO2、Al2O3等杂质。工业上常采用固体碱熔氧化法用铬铁矿粉制备重铬酸钾,流程为

已知:①NaFeO2遇水强烈水解;
②重铬酸钾为橙红色针状晶体,溶于水,不溶于乙醇,有强氧化性;
③2CrO42- + 2H+  Cr2O72-+ H2O
Cr2O72-+ H2O
(1)铬铁矿经粉碎处理的目的是__________________________;
(2)①写出反应器中灼烧时生成Na2CrO4的化学方程式为_________________________;
②水浸时生成滤渣1的离子方程式为________________。
(3)滤液1的成分除Na2CrO4、NaOH外,还含有____________________ (填化学式)。
(4)通过途径1从Na2CrO4溶液获得K2Cr2O7晶体,操作步骤有“酸化”→加KCl固体→蒸发浓缩→操作a→过滤→洗涤→干燥。
①洗涤晶体的具体操作_________________________;
②“酸化”步骤用醋酸调节溶液pH<5,其目的是________________________(用化学术语结合文字说明回答)。
(5)重铬酸钾纯度测定: 取产品重铬酸钾试样2.000g配成250mL溶液,取出25.00mL于锥形瓶中,加入10mL 2mol/LH2SO4和足量碘化钠(铬的还原产物为Cr3+),放于暗处5min,然后加入100mL水,加入3mL淀粉指示剂,用0.1200 mol·L-1Na2S2O3标准溶液滴定(I2+2S2O32−=2I−+S4O62−)。 若实验中共用去Na2S2O3标准溶液26.00mL,所得产品的中重铬酸钾的纯度为______________(设整个过程中其它杂质不参与反应)。
-
工业上以铬铁矿(含有Cr2O3,FeO、Al2O3、SiO2等成分)为主要原料生产重铬酸钠晶体(Na2Cr2O7·2H2O),其主要工艺流程如下:
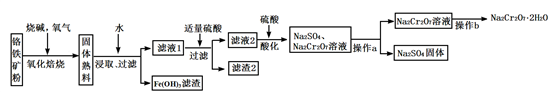
提示:熟料中含有Na2CrO4、NaFeO2等成分。
回答下列问题:
(1)将铬铁矿粉碎的目的是_____________________________ 。
(2)氧化焙烧时,生成Na2CrO4的化学方程式是__________。
(3)滤渣2中除Al(OH)3外还有__________(填化学式)。
(4)加入硫酸酸化的目的是__________________________。
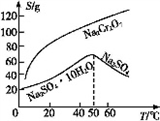
(5)根据下图,请将操作a补充完整:________________,洗涤,干燥。
(6)控制105~110℃,向较浓的Na2Cr2O7溶液中加入KCl固体发生复分解反应,立即析出K2Cr2O7晶体。能生成K2Cr2O7晶体的原因是_____________。
(7)向Na2Cr2O7酸性溶液中加入过量FeSO4溶液,生成Cr3+和 Fe3+,再加入过量的强碱溶液生成铁铬氧体沉淀(CrxFe3-xO4)。加入过量强碱生成铁铬氧体沉淀的离子方程式是______。
-
铬铁矿的成分主要为FeCr2O4,另含有少量Al2O3和SiO2。从铬铁矿中提取铁、铬的化合物,并获得副产物的工艺流程如下:
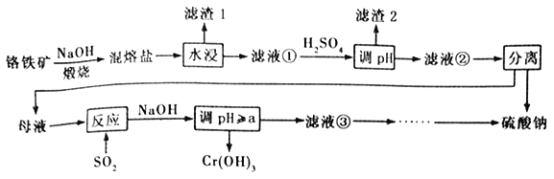
已知“混熔盐”中含有Na2CrO4和NaFeO2,其中NaFeO2极易水解。试回答下列问题:
(1)“滤渣1”为红褐色沉淀,其化学式为_________________;向滤液①中加H2SO4“调pH”的目的:一是使CrO42-转化为Cr2O72- ;二是____________________________。
(2)“煅烧”铬铁矿时,主要反应的化学方程式为_______________________________。
(3)根据右图溶解度(S)~温度(T)曲线判断,对滤液②进行的最佳“分离”方法为_________(填序号)。
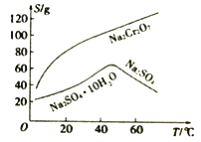
A.蒸发结晶 B.蒸发浓缩,趁热过滤 C.蒸发浓缩,冷却结晶,过滤
(4)“反应”的离子方程式为_______________________________。
(5)Cr(OH)3溶于盐酸生成配离子[CrCln(H2O) 6-n]x+。0.0015 mol [CrCln(H2O) 6-n]x+与氢离子交换树脂(HR)完全发生离子交换:
[CrCln(H2O) 6-n]x++xHR→Rx[CrCln(H2O) 6-n]+xH+,生成的H+可与25.00 mL0.1200 mol·L -1NaOH溶液恰好中和。则该配离子的化学式为__________________。
(6)已知25℃时,Cr(OH)3的溶度积常数Ksp[Cr(OH)3]=1.0×10-32。则使Cr3+恰好完全沉淀,即溶液中c(Cr3+) =1.0×10-5 mol·L -1时,应调节溶液pH的最小值a为多少? (列式计算)____________________________________________。
-
铬铁矿的成分主要为FeCr2O4,另含有少量Al2O3和SiO2。从铬铁矿中提取铁、铬的化合物,并获得副产物的工艺流程如下:

已知“混熔盐”中含有Na2CrO4和NaFeO2等成分,其中NaFeO2极易水解。试回答下列问题:
(1)“滤渣1”为红褐色沉淀,其化学式为_________________;通过水浸生成红褐色沉淀的化学方程式为_________________________________。
(2)向滤液①中加H2SO4“调“pH”的目的:一是使CrO42-转化为Cr2O72-,离子方程式为___________________________________;二是____________________________。
(3)“煅烧”铬铁矿时,主要成分反应的化学方程式为____________________________。
(4)根据下图溶解度(S)~温度(T)曲线判断,对滤液②进行的最佳“分离”方法为_____________(填序号)。
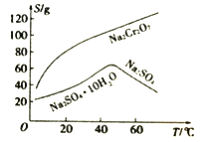
A.蒸发结晶 B.蒸发浓缩,趁热过滤 C.蒸发浓缩,冷却结晶,过滤
(5)“反应”的离子方程式为____________________________。
(6)Cr(OH)3溶于盐酸生成配离子[CrCln(H2O)6-n]x+。0.0015mol[CrCln(H2O)6-n]x+与氢离子交换树脂(HR)完全发生离子交换:[CrCln(H2O)6-n]x++xHR→Rx[CrCln(H2O)6-n] +xH+,生成的H+可与25.00mL 0.1200mol/L NaOH溶液恰好中和。则该配离子的化学式为__________________。
(7)已知25℃时,Cr(OH)3的溶度积常数Ksp[Cr(OH)3]=1.0×10-32。则使Cr3+恰好完全沉淀,即溶液中c(Cr3+)=1.0×10-5mol/L时,应调节pH的最小值a为多少___________?(列式计算)
-
重铬酸钾(K2Cr2O7)是常用的氧化剂,工业上以铬铁矿(含有Cr2O3、FeO、Al2O3、SiO2等)为原料制备重铬酸钾的流程如下。

已知:NaFeO2遇水强烈水解。
请回答下列问题:
(1)将矿石粉碎的目的是_________。
(2)高温灼烧后产物中含有NaFeO2、Na2CrO4等成份,写出生成Na2CrO4的化学方程式____________。
(3)“滤渣1”中有红褐色物质,写出生成该物质的离子方程式______________。
(4)“滤渣2”中主要成分是A1(OH)3和 ___________。
(5)“酸化”反应的离子方程式为2CrO42-(aq)+2H+(aq) Cr2O72-(aq)+H2O。在25℃时,取Na2CrO4溶液进行酸化实验,测得部分实验数据如下:
Cr2O72-(aq)+H2O。在25℃时,取Na2CrO4溶液进行酸化实验,测得部分实验数据如下:
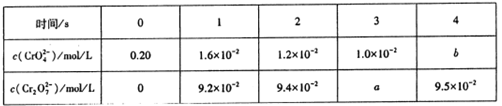
表格中b=__________;若反应达到平衡时,溶液的pH=1,则该反应的平衡常数K=__________;
(6)简要说明Na2CrO7溶液中加入KCl固体,“结品”析出K2Cr2O7晶体的原因_________________。
-
以含有Al2O3、Fe2O3等杂质的铬铁矿[主要成份为Fe(CrO2)2]为主要原料生产重铬酸钠晶体( Na2Cr2O7·2H2O)的主要工艺流程如下:

己知:铬铁矿在空气中与纯碱煅烧生成Na2CrO4和一种红棕色固体,同时释放出CO2气体,同时A12O3+Na2CO3  2NaAlO2+CO2↑。请回答:
2NaAlO2+CO2↑。请回答:
(1)在铬铁矿Fe(CrO2)2中,Cr的化合价为____。
(2)滤渣1的成分为________,滤渣2的成分为____。
(3)将滤渣l放入稀硫酸溶解后得溶液W,检验该溶液中金属离子的方法是 。
(4)铬铁矿中的Al2O3杂质在工业上可用来冶炼铝,该化学方程式为
(5)根据有关国家标准,含CrO42-的废水要经化学处理,使其浓度降至5.0×10-7 mo1/L以下才能排放。含CrO42-的废水处理通常有以下两种方法。
①沉淀法:加入可溶性钡盐生成BaCrO4沉淀 ,再加入可溶性硫酸盐处理多余的Ba2+。加入可溶性钡盐后的废水中Ba2+的浓度应不小于 mol/L,后续废水处理方能达到国家排放标准。
,再加入可溶性硫酸盐处理多余的Ba2+。加入可溶性钡盐后的废水中Ba2+的浓度应不小于 mol/L,后续废水处理方能达到国家排放标准。
②还原法: 。写出酸性条件下 CrO42-与绿矾在溶液中反应的离子方程式 。
。写出酸性条件下 CrO42-与绿矾在溶液中反应的离子方程式 。
(6)某高效净水剂是由K2FeO4得到的,工业上以溶液W、次氯酸钾和氢氧化钾为原料制备K2FeO4,该反应的化学方程式是 。
-
以含有Al2O3、Fe2O3等杂质的铬铁矿[主要成分为Fe(CrO2)2]为主要原料生产重铬酸钠晶体(Na2Cr2O7·2H2O)的主要工艺流程如下:
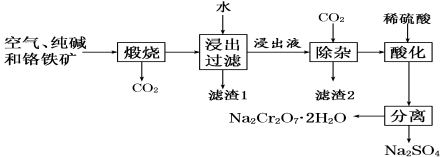
已知:铬铁矿在空气中与纯碱煅烧生成Na2CrO4和一种红棕色固体,同时释放出CO2气体,且Al2O3+Na2CO3 2NaAlO2+CO2↑。请回答:
2NaAlO2+CO2↑。请回答:
(1)在铬铁矿Fe(CrO2)2中,Cr的化合价为 。
(2)滤渣2的成分为 。
(3)将滤渣1放入稀硫酸溶解后得溶液W,检验该溶液中金属离子的方法是 。
(4)根据有关国家标准,含CrO 的废水要经化学处理,使其浓度降至5.0×10-7 mol/L以下才能排放。含CrO
的废水要经化学处理,使其浓度降至5.0×10-7 mol/L以下才能排放。含CrO 的废水处理通常用以下方法:还原法:
的废水处理通常用以下方法:还原法: 。写出酸性条件下CrO
。写出酸性条件下CrO 与绿矾(FeSO4.7H2O)在溶液中反应的离子方程式:____________________________。
与绿矾(FeSO4.7H2O)在溶液中反应的离子方程式:____________________________。
-
以含有Al2O3、Fe2O3等杂质的铬铁矿[主要成分为Fe(CrO2)2]为主要原料生产重铬酸钠晶体(Na2Cr2O7·2H2O)的主要工艺流程如下:

己知:铬铁矿在空气中与纯减煅烧生成Na2CrO4和一种红棕色固体,同时释放出CO2气体,
且 Al2O3+Na2CO3 2NaAlO2+ CO2↑。请回答:
2NaAlO2+ CO2↑。请回答:
(1)在铬铁矿Fe(CrO2)2中,Cr的化合价为___________。
(2)滤渣2的成分为_____________。
(3)将滤渣1放入稀硫酸溶解后得溶液W,检验该溶液中金属离子的方法是_________。
(4)根据有关国家标准,含CrO42-的废水要经化学处理,使其浓度降至5.0×10-7mol/L以下才能排放。含CrO42-的废水处理通常有以下两种方法。
①沉淀法:
加入可溶性钡盐生成BaCrO4沉淀[Ksp(BaCrO4)=1.2×10-10],再加入可溶性硫酸盐处理多余的Ba2+。加入可溶性钡盐后的废水中Ba2+的浓度应不小于________________mol/L,后续废水处理方能达到国家排放标准。
②还原法:CrO42- Cr3+
Cr3+ Cr(OH)3。写出酸性条件下CrO42-与绿巩在溶液中反应的离子方程式:_________________________________。
Cr(OH)3。写出酸性条件下CrO42-与绿巩在溶液中反应的离子方程式:_________________________________。
(5)某高效净水剂是由K2FeO4得到的,工业上以溶液w、次氯酸钾和氢氧化钾为原料制备K2FeO4,该反应的离子方程式是______________________。













 。写出酸性条件下CrO
。写出酸性条件下CrO