-
随着现代化工业的发展,能源问题已经越来越引起人们的重视。科学家预言,未来最理想的燃料是绿色植物,即将植物的秸秆(主要成分是纤维素)用适宜的催化剂作用水解成葡萄糖,再将葡萄糖转化为乙醇,用作燃料。
(1)写出绿色植物秸秆转化为乙醇的化学方程式:
①_____________________________________________________________。
②____________________________________________________________。
(2)乙醇除用作燃料外,还可用来合成其他有机物,下列主要是以乙醇为起始原料的转化关系图。请在表中填上相应物质的结构简式。

(3)写出上面关系图中由c生成C4H4O4的化学方程式。(有机物用结构简式表示)_________________________________________________________。
-
每年夏季,农民焚烧植物秸秆(主要成分是纤维素),既污染了环境,又浪费了资源,工业上以植物秸秆为原料合成某聚酯化合物的路线如下:

已知A是常见的消毒剂,又可作为能源。
(1)乙烯中官能团的结构式为___________;葡萄糖分子中官能团的电子式为_______________;
(2)由B转化为C的反应条件是________________;C转化为D的反应类型是___________;
(3)测定D中所含官能团的物理方法是__________;若B是氯代烃,其系统命名法的名称是_______;
(4)写出下列反应方程式:
A:由植物秸秆转化成葡萄糖________________________________________________;
B:由A转化成乙烯__________________________________________________;
C:生成聚酯化合物__________________________________________________。
-
随着环保意识增强,清洁能源越来越受到人们关注。
(1)甲烷是一种理想的洁净燃料。已知:CH4(g)+2O2(g)= CO2(g)+ 2H2O(g);△H= -802.3kJ·mol-1 H2O(1)=H2O(g),△H =+44.0kJ·mol-l
写出常温常压下甲烷完全燃烧的热化学方程式____,计算4.8g甲烷气体完全燃烧生成液态水,放出热量为____kJ。
(2)利用甲烷与水反应制备氢气,因原料廉价,具有推广价值。该反应为CH4(g)+H2O(g) CO(g)+3H2(g)△H=+206.lkJ·mol-l。
CO(g)+3H2(g)△H=+206.lkJ·mol-l。
①800℃时,反应的化学平衡常数K=l.0,某时刻测得该温度下密闭容器中各物质的物质的量浓度如下表。
| CH4 | H2O | CO | H2 |
| 3.0 mol•L‾1 | 8.5 mol•L‾1 | 2.0 mol•L‾1 | 2.0 mol•L‾1 |
则此时正、逆反应速率的关系是正反应速率____逆反应速率。(填“>”、“<”、“=”)
②为了探究温度、压强对上述化学反应速率的影响,某同学设计了以下三组对比实验(温度为360℃或480℃、压强为101 kPa或303 kPa,其余实验条件见下表)。
| 实验序号 | 温度/℃ | 压强/kPa | CH4初始浓度/ mol•L‾1 | H2O初始浓度/ mol•L‾1 |
| 1 | 360 | p | 2.00 | 6.80 |
| 2 | t | 101 | 2.00 | 6.80 |
| 3 | 360 | 101 | 2.00 | 6.80 |
表中t=___,P=____;设计实验2、3的目的是____;实验l、2、3中反应的化学平衡常数的大小关系是____(用K1、K2、K3表示)。
-
随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。
(1)如图为C及其氧化物的变化关系图,若①变化是置换反应,则其化学方程式可为___。

(2)一定条件下,在密闭容器中发生反应CO2(g)+C(s) 2CO(g)达到平衡,能使平衡向正反应方向移动的有__(填字母)。
2CO(g)达到平衡,能使平衡向正反应方向移动的有__(填字母)。
A.保持其他条件不变,增大压强
B.保持容器总体积不变,通入少量Ar
C.增加碳的用量
D.保持其他条件不变,升高温度
(3)根据下列3个热化学反应方程式:
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) △H=-24.8kJ/mol
3Fe2O3(s)+CO(g)=2Fe3O4(s)+CO2(g) △H=-47.2kJ/mol
Fe3O4(s)+CO(g)=3FeO(s)+CO2(g) △H=+640.4kJ/mol
写出CO气体还原FeO固体得到Fe固体和CO2气体的热化学反应方程式:__。
-
随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。
(1)如图为C及其氧化物的变化关系图,若①是通过O2与C反应实现的,测知生成14gCO时放出60kJ的热量,则其热化学方程式为 。
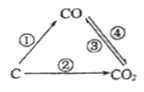
(2)把煤作为燃料可通过下列两种途径:
途径I:C(s)+O2(g)=CO2(g) △H1<0 ①
途径II:先制成水煤气:C(s)+H2O(g)=CO(g)+H2(g) △H2>0 ②
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g) △H3<0 ③
2H2(g)+O2(g)=2H2O(g) △H4<0 ④
则途径I放出的热量 (填“大于”“等于”或“小于”)途径II放出的热量;△H1、△H2、△H3、△H4的数学关系式是 。
(3)甲醇(CH3OH)是一种可再生能源,具有开发和应用的广阔前景,工业上可用如下方法合成甲醇:
方法一 CO(g)+2H2(g)  CH3OH(g)
CH3OH(g)
方法二 CO2(g)+3H2(g)  CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
在25℃、101kPa下,1 克液态甲醇完全燃料放热25kJ,写出甲醇燃烧生成1molCO2的热化学方程式 。若将该反应设计成原电池反应,用稀H2SO4 作电解质,则其电极方程式分别为正极: 负极:
(4)金属钛冶炼过程中其中一步反应是将原料金红石转化:
TiO2(金红石)+2C+2Cl2 TiCl4+2CO
TiCl4+2CO
已知:C(s)+O2(g)=CO2(g) △H= - 400kJ·mol―1
2CO(g)+O2(g)=2CO2(g) △H= - 560kJ·mol―1
TiO2(s)+2Cl2(g)=TiCl(s)+O2(g) △H=+140kJ·mol―1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的△H= 。
(5)臭氧可用于净化空气、饮用水消毒,处理工业废物和作为漂白剂。臭氧几乎可与除铂、金、铱、氟以外的所有单质反应。如:
6Ag(s)+O3(g)=3Ag2O(s) △H=―260kJ·mol―1
已知:2Ag2O(s)=4Ag(s)+O2(g) △H=+70kJ·mol―1
则O3转化为O2的热化学方程式为 。
-
随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。
(1)如图为C及其氧化物的变化关系图,若①变化是置换反应,则其化学方程式可以是 。

(2)把煤作为燃料可通过下列两种途径:
途径I:C(s)+O2(g)=CO2(g) △H1<0 ①
途径II:先制成水煤气:C(s)+H2O(g)=CO(g)+H2(g) △H2>0 ②
再燃烧水煤气:2CO(g)+O2(g)=2CO2(g) △H3<0 ③
2H2(g)+O2(g)=2H2O(g) △H4<0 ④
则途径I放出的热量 (填“大于”“等于”或“小于”)途径II放出的热量;△H1、△H2、△H3、△H4的数学关系式是 。
(3)甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上可用如下方法合成甲醇:
方法一 CO(g)+2H2(g) CH3OH(g) 方法二 CO2(g)+3H2(g)
CH3OH(g) 方法二 CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)
在25℃、101kPa下,1 克甲醇完全燃料放热22.68kJ,写出甲醇燃烧热的热化学方程式 。
(4)金属钛冶炼过程中其中一步反应是将原料金红石转化:
TiO2(金红石)+2C+2Cl2 TiCl4+2CO
TiCl4+2CO
已知:C(s)+O2(g)=CO2(g) △H=―393.5kJ·mol―1
2CO(g)+O2(g)=2CO2(g) △H=―566kJ·mol―1
TiO2(s)+2Cl2(g)=TiCl(s)+O2(g) △H=+141kJ·mol―1
则TiO2(s)+2Cl2(g)+2C(s)=TiCl4(s)+2CO(g)的△H= 。
(5)臭氧可用于净化空气、饮用水消毒,处理工业废物和作为漂白剂。臭氧几乎可与除铂、金、铱、氟以外的所有单质反应。如:
6Ag(s)+O3(g)=3Ag2O(s) △H=―235.8kJ·mol―1
已知:2Ag2O(s)=4Ag(s)+O2(g) △H=+62.2kJ·mol―1
则O3转化为O2的热化学方程式为 。
-
随着世界工业经济的发展、人口的剧增,全球能源紧张及世界气候面临越来越严重的问题,如何降低大气中CO2的含量及有效地开发利用CO2引起了全世界的普遍重视。
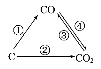
(1)如图为C及其氧化物的变化关系图,若①变化是置换反应,则其化学方程式可为;
(2)把煤作为燃料可通过下列两种途径:
途径Ⅰ:C(s)+O2(g)===CO2(g)ΔH1<0;①
途径Ⅱ:先制成水煤气:C(s)+H2O(g)===CO(g)+H2(g)ΔH2>0;②
再燃烧水煤气:2CO(g)+O2(g)===2CO2(g)ΔH3<0,③
2H2(g)+O2(g)===2H2O(g)ΔH4<0。④
则途径Ⅰ放出的热量________(填“大于”、“等于”或“小于”)途径Ⅱ放出的热量。
(3)甲醇是一种可再生能源,具有开发和应用的广阔前景,已知反应2CH3OH(g) CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
CH3OCH3(g)+H2O(g)某温度下的平衡常数为400。此温度下,在密闭容器中加入CH3OH,反应到某时刻测得各组分的浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| 浓度/(mol·L-1) | 0.44 | 0.6 | 0.6 |
比较此时正、逆反应速率的大小:v正____v逆(填“>”“<”或“=”)。
(4)生产液晶显示器的过程中使用的化学清洗剂NF3是一种温室气体,其存储能量的能力是CO2的12000~20000倍,在大气中的寿命可长达740年之久,以下是几种化学键的键能:
| 化学键 | N≡N | F—F | N—F |
| 键能/kJ·mol-1 | 941.7 | 154.8 | 283.0 |
则反应N2(g)+3F2(g)═2NF3(g)的ΔH=
(5)25℃、101kPa时,已知:
2H2O(g)═O2(g)+2H2(g)△H1
Cl2(g)+H2(g)═2HCl(g)△H2
2Cl2(g)+2H2O(g)═4HCl(g)+O2(g)△H3
则△H3与△H1和△H2间的关系正确的是
A.△H3=△H1+2△H2B.△H3=△H1+△H2
C.△H3=△H1﹣2△H2D.△H3=△H1﹣△H2
(6)臭氧可用于净化空气,饮用水消毒,处理工业废物和作为漂白剂。臭氧几乎可与除铂、金、铱、氟以外的所有单质反应。如6Ag(s)+O3(g)=3Ag2O(s)ΔH=-235.8kJ·m ol-1,
ol-1,
已知:2Ag2O(s)=4Ag(s)+O2(g)ΔH=+62.2kJ·mol-1,
则O3转化为O2的热化学方程式为。
-
有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。
(1)氢能被称为绿色能源的原因是____(任答一点)。
(2)在101 kPa下,1 g氢气完全燃烧生成气态水放出120.9 kJ的热量,请回答下列问题:
①该反应的反应物总能量______生成物总能量。(填“>、=、<”)
②该反应的热化学方程式为______。
③已知H-O键能为463.4 kJ/mol,O=O键能为498kJ/mol,计算H-H键能为___kJ/mol。
(3)氢能的储存是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:Mg(s)+H2(g)=MgH2(s) ΔH1=-74.5 kJ/mol;
Mg2Ni(s)+2H2(g)=Mg2NiH4(s) ΔH2=-64.4 kJ/mol;Mg2Ni(s)+2MgH2(s)=2Mg(s)+Mg2NiH4(s)ΔH3,则ΔH3=_____ kJ/mol。
-
有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。
(1)氢能被称为绿色能源的原因是________________(任答一点)
(2)在101KP下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题
①该反应反应物总能量______________生成物总能量(填“大于”,“小于”或“等于”)
②氢气的燃烧热为______________
③该反应的热化学方程式为__________________________________________________
④若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O键能为463 kJ·mol-1,O=O键能为498 kJ·mol-1,计算H-H键能为_____________kJ·mol-1
(3)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)===MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)===Mg2NiH4(s) ΔH2=-64.4kJ·mol-1;
Mg2Ni(s)+2MgH2(s)===2Mg(s)+Mg2NiH4(s) ΔH3。
则ΔH3=____________kJ·mol-1
-
有科学家预言,氢能将成为21世纪的主要能源,而且是一种理想的绿色能源。
(1)在101KP下,1g氢气完全燃烧生成液态水放出142.9kJ的热量,请回答下列问题
①该反应反应物总能量______________生成物总能量(填“大于”,“小于”或“等于”)
②氢气的燃烧热为_________。 ③该反应的热化学方程式为___________________。
④若1mol氢气完全燃烧生成1mol气态水放出241kJ的热量,已知H-O键能为463 kJ·mol-1,O=O键能为498 kJ·mol-1,计算H-H键能为_____________kJ·mol-1
(2)氢能的存储是氢能利用的前提,科学家研究出一种储氢合金Mg2Ni,已知:
Mg(s)+H2(g)===MgH2(s) ΔH1=-74.5kJ·mol-1;
Mg2Ni(s)+2H2(g)===Mg2NiH4(s) ΔH2=-64.4kJ·mol-1;
Mg2Ni(s)+2MgH2(s)===2Mg(s)+Mg2NiH4(s) ΔH3。
则ΔH3=____________kJ·mol-1





