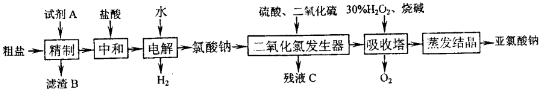
回答下列问题:
(1)“精制”过程中,加入过量的Na2CO3的作用是______.
(2)电解时发生主要反应的离子方程式为______ ClO3-+3H2↑
高三化学解答题中等难度题

高三化学解答题中等难度题

高三化学解答题中等难度题查看答案及解析
以地下卤水(主要含NaCl,还有少量Ca2+、Mg2+)为主要原料生产亚硫酸钠的新工艺如下,同时能得到用作化肥的副产品氯化铵。

已知以下四种物质的溶解度曲线图:

(1)“除杂”时,先加入适量石灰乳过滤除去Mg2+,再通入CO2并用少量氨水调节pH过滤除去Ca2+,“废渣”的主要成分为 ________、________。
(2)“滤渣1”的化学式为________。
(3)在“滤液1”中加入盐酸的目的是________。“滤渣2”的化学式为________。
(4)已知H2CO3和H2SO3的电离常数如下表,“通入SO2”反应的化学方程式为________。
| 物质 | 电离常数(25℃) |
| H2CO3 | K1=4.4X10-7 K2=4.7X10-11 |
| H2SO3 | K1=1.23X10-2 K2=5.6X10-8 |
高三化学填空题极难题查看答案及解析
锂辉石是我国重要的锂资源之一,其主要成分为 Li2O、SiO2、Al2O3 以及含有少量 Na+、Fe2+、Fe3+、Ca2+、Mg2+等金属离子。工业上用锂辉石制备金属锂的工艺流程如下:

已知:①部分阳离子以氢氧化物形式沉淀时溶液的 pH 见下表:
| 沉淀物 | Al(OH)3 | Fe(OH)2 | Fe(OH)3 | Ca(OH)2 | Mg(OH)2 |
| 完全沉淀的pH | 5.2 | 9.6 | 3.2 | 13.1 | 10.9 |
②常温下,Ksp(Li2CO3)= 2.0×10-3。Li2CO3 在水中溶解度随着温度升高而减小。
③有水存在时,LiCl 受热可发生水解。
回答下列问题:
(1)为提高“酸浸”速率,上述流程中采取的措施有_____。
(2)滤渣 I 的主要成分是_____。滤渣 II 的主要成分是 Fe(OH)3、Al(OH)3。“氧化” 和“除杂”步骤主要除去的离子有_________。
(3) “沉锂”过程中发生反应的离子方程式是_____。用热水洗涤 Li2CO3 固体,而不用冷水洗涤,其原因是_____。
(4)设计简单的实验方案实现由过程 a 制取固体 LiCl:_____。
(5)工业上实现过程 b 常用的方法是_____。
(6)Li 可用于制备重要还原剂四氢铝锂(LiAlH4)。在有机合成中,还原剂的还原能力常用“有效氢”表示,其含义为 1克还原剂相当于多少克 H2 的还原能力。LiAlH4 的“ 有效氢”为_____(保留 2 位小数)。
高三化学综合题中等难度题查看答案及解析
以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示:

回答下列问题:
(1)写出Mg2B2O5·H2O与硫酸反应的化学方程式________________。
为提高浸出速率,除适当增加硫酸浓度外,还可采取的措施有_____________(写出两条)。
(2) “浸渣”中除含有某种有磁性的物质外,还含有的物质是_____(写化学式)。
(3)“净化除杂”需先加H2O2溶液,作用是__________。然后再调节溶液的pH约为5,目的是______________。
(4)“粗硼酸”中的主要杂质是________(填名称)。
(5)单质硼可用于生产具有优良抗冲击性能的硼钢。以硼酸和金属镁为原料可制备单质硼,用化学方程式表示制备过程_____________、 _________________。
高三化学实验题中等难度题查看答案及解析
以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示:
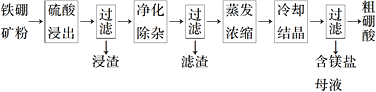
回答下列问题:
(1)写出Mg2B2O5·H2O与硫酸反应的化学方程式________________。
为提高浸出速率,除适当增加硫酸浓度外,还可采取的措施有_____________(写出两条)。
(2) “浸渣”中除含有某种有磁性的物质外,还含有的物质是_____(写化学式)。
(3)“净化除杂”需先加H2O2溶液,作用是__________。然后再调节溶液的pH约为5,目的是______________。
(4)“粗硼酸”中的主要杂质是________(填名称)。
(5)单质硼可用于生产具有优良抗冲击性能的硼钢。以硼酸和金属镁为原料可制备单质硼,用化学方程式表示制备过程_____________、 _________________。
高三化学实验题中等难度题查看答案及解析
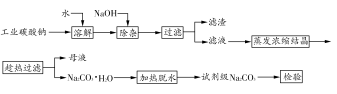
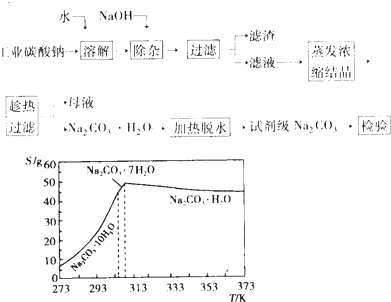
碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺路线如下:
已知碳酸钠的溶解度(S)随温度变化的曲线如下图所示:
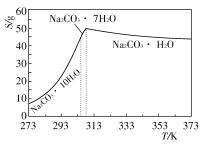
回答下列问题:
(1)滤渣的主要成分为____________________________________。
(2)“趁热过滤”的原因是_______________________________________。
(3)若在实验室进行“趁热过滤”,可采用的措施是__________(写出1种)。
(4)若“母液”循环使用,可能出现的问题及其原因是_______________。
(5)已知:Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g)ΔH1=+532.36 kJ·mol-1
Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g)ΔH2=+473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式______________________。
高三化学填空题中等难度题查看答案及解析
高三化学解答题中等难度题查看答案及解析
(12分)碳酸钠是造纸、玻璃、纺织、制革等行业的重要原料。工业碳酸钠(纯度约98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO等杂质,提纯工艺路线如下:

已知碳酸钠的溶解度(S)随温度变化的曲线如图所示:

回答下列问题:
(1)滤渣的主要成分为_________________________。
(2)“趁热过滤”的原因是______________________。
(3)在实验室做Na2CO3·H2O脱水实验,判断其脱水完全的方法是:__________。
(4)生产过程中“母液”____(填“能”或“不能”)循环使用。若不能,其原因是:_________。
(5)已知:① Na2CO3·10H2O(s)=Na2CO3(s)+10H2O(g);ΔH1= +532.36 kJ·mol-1
② Na2CO3·10H2O(s)=Na2CO3·H2O(s)+9H2O(g);ΔH2= +473.63 kJ·mol-1
写出Na2CO3·H2O脱水反应的热化学方程式_____________________。
高三化学填空题困难题查看答案及解析
(14分)硼及其化合物在工业上有许多用途。以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示:
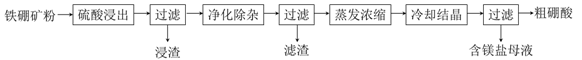
回答下列问题:
(1)写出Mg2B2O5·H2O与硫酸反应的化学方程式_____________。为提高浸出速率,除适当增加硫酸浓度浓度外,还可采取的措施有_________(写出两条)。
(2)利用 的磁性,可将其从“浸渣”中分离。“浸渣”中还剩余的物质是______(写化学式)。
(3)“净化除杂”需先加H2O2溶液,作用是_______。然后再调节溶液的pH约为5,目的是________。
(4)“粗硼酸”中的主要杂质是 (填名称)。
(5)以硼酸为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂,其电子式为_______。
(6)单质硼可用于生成具有优良抗冲击性能硼钢。以硼酸和金属镁为原料可制备单质硼,用化学方程式表示制备过程___________。
高三化学实验题困难题查看答案及解析
硼及其化合物在工业上有许多用途。以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示:
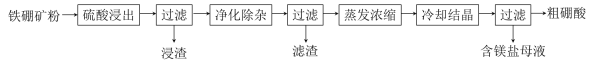
已知:硼酸为粉末状晶体,易溶于水,加热到一定温度可分解为无水物。
回答下列问题:
(1)写出Mg2B2O5·H2O与硫酸反应的化学方程式___。为提高浸出速率,除适当增加硫酸浓度浓度外,还可采取的措施有(写两条):___。
(2)“浸渣”中还剩余的物质是:___(写化学式)。
(3)“净化除杂”需先加H2O2溶液,作用是___。然后再调节溶液的pH约为5,目的是___。
(4)“粗硼酸”中的主要杂质是___(填名称)。
(5)单质硼可用于生成具有优良抗冲击性能硼钢。以硼酸和金属镁为原料可制备单质硼,用化学方程式表示制备过程___。
高三化学工业流程中等难度题查看答案及解析