-
已知:H2(g) + F2(g) = 2HF(g) ΔH=− 270 kJ/mol[表示1 mol H2(g)与1 mol F2(g)化合生成2 mol HF(g)放出270 kJ热量],下列说法正确的是

A.该反应的逆反应是放热反应
B.该反应过程的能量变化可用右图来表示
C.1 mol H2(g)与1 mol F2(g)反应生成2 mol液态HF放出的热量小于270 kJ
D.在相同条件下,1 mol H2(g)与1 mol F2(g)的能量总和大于2 mol HF(g)的能量
-
已知:H2(g)+F2(g)=2HF(g) △H=—270kJ/mol,下列说法正确的是( )
A.2L氟化氢气体分解成1L的氢气和1L的氟气吸收270kJ热量
B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的热量小于270kJ
C.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量
D.1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270kJ热量
-
已知:H2(g)+F2(g)===2HF(g);ΔH=-270kJ·mol-1,下列说法正确的是( )
A.1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270 kJ热量
B.1 mol 氢气与1 mol 氟气反应生成2 mol液态氟化氢放出的热量小于270 kJ
C.在相同条件下,1 mol氢气与1 mol氟气的能量总和大于2 mol氟化氢气体的能量
D. 2 L氟化氢气体分解成1 L氢气和1 L氟气吸收270 kJ热量
-
已知:H2(g)+F2(g) ===2HF(g) △H=-270kJ/mol,下列说法正确的是
A.1个氢气分子与1个氟气分子反应生成2个氟化氢分子放出270kJ
B.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出的 热量小于270kJ
热量小于270kJ
C.在相同条件下,1mol氢气与1mol氟气的能量总和大于2mol氟化氢气体的能量
D.2mol氟化氢气体分解成1mol的氢气和1mol的氟气放出270kJ热量
-
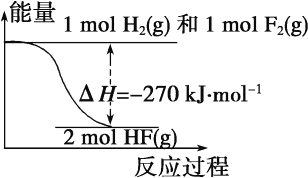
已知:H2(g)+F2(g)===2HF(g) ΔH=-270 kJ·mol-1,下列说法正确的是:
A. 氟化氢气体分解生成氢气和氟气的反应是放热反应
B. 1 mol H2 与 1 mol F2 反应生成 2 mol 液态 HF 放出的热量小于 270 kJ
C. 在相同条件下,1 mol H2与 1 mol F2的能量总和小于 2 mol HF 气体的能量
D. 该反应中的能量变化可用如图来表示
-
已知:H2(g)+F2(g)=2HF(g)+270KJ,下列说法正确的是
A.1个氢气分子与1个氟气分子反应生成2个氟化氢气体分子放出270KJ热量
B.2L氟化氢气体分解成1L氢气与1L氟气吸收270KJ热量
C.1mol氢气与1mol氟气反应生成2mol液态氟化氢放出热量大于270KJ
D.该反应过程的能量变化可用图来表示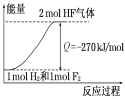
-
已知:2H2(g)+O2(g)=2H2O(g);ΔH=-270kJ·mol-1,下列说法错误的是( )
A.2mol水蒸气分解成2mol氢气与1mol氧气吸收270kJ热量
B.2mol氢气与1mol氧气反应生成2mol液态水放出热量大于270kJ
C.在相同条件下,2mol氢气与1mol氧气的能量总和大于2mol水蒸汽的能量
D.2个氢气分子与1个氧气分子反应生成2个水蒸汽分子放出270kJ热量
【解析】若正反应是放热反应,则逆反应就是吸热反应,所以A是正确的。气态水的能量高于液态水的能量,因此氢气燃烧生成液态水放出的能量多于生成气态水放出的能量,B正确。反应放热,说明反应物的总能量高于生成物的总能量,C正确。在热化学方程式中物质前面的计量数表示的是物质的物质的量,所以D是错误的。
-
已知:H2(g)+F2(g)==="2HF(g)" 的能量变化如图所示,下列有关叙述中正确的是
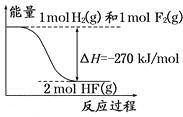
A. 氟化氢气体分解生成氢气和氟气的反应是放热反应
B. 1 mol H2与1 mol F2反应生成2 mol液态HF放出的热量小于270 kJ
C. 在相同条件下,1 mol H2与1 mol F2的能量总和大于2 mol HF气体的能量
D. 断裂1 mol H—H键和1 mol F—F 键放出的能量大于形成2 mol H—F键放出的能量
-
下列说法或表示法不正确的是
A.1mol硫蒸气与2mol硫蒸气完全燃烧时,燃烧热相同
B.已知:2H2(g)+O2(g)=2H2O(l) △H=-571.6kJ·mol-1,则H2的燃烧热为285.8kJ·mol-1
C.在稀溶液中:H+(aq)+OH-(aq)=H2O(aq)△H=-57.3kJ·mol-1,若将含1molCH3COOH的醋酸溶液与含1molBa(OH)2的溶液混合,放出的热量小于57.3kJ
D.在101kPa、25℃时,2gH2完全燃烧生成液态水,放出285.8kJ热量,氢气燃烧的热化学方程式表示为2H2(g)+O2(g)=2H2O(l) △H=+285.8kJ·mol-1
-
已知O2F2可以发生反应:H2S+4O2F2 = SF6+2HF+4O2,下列说法正确的是( )
A.SF6是还原产物
B.O2F2是还原剂
C.若生成3.2g O2,则转移0.2 mol e−
D.还原剂与氧化剂的物质的量之比为4:1



