-
粗盐提纯的研究.
【有关资料】
| 化学式 | CaCO3 | CaSO3 | CaC2O4 | Mg(OH)2 |
| Ksp | 4.96×10-9 | 4.96×10-9 | 2.34×10-9 | 5.61×10-12 |
某研究性学习小组对粗盐的提纯和检验进行研究,并提出一些新的方案.已知该粗盐样品中主要含有不溶性杂质、Mg2+、Ca2+等(忽略SO42-的存在),该小组设计流程如下:

【设计除杂过程】
(1)操作①中需要使用的玻璃仪器有______、______.操作②的名称为______,若在操作②结束后发现溶液B略有浑浊,应采取的措施是______.
(2)混合液A的主要成分是______.(填化学式)
【检验除杂效果】
(3)为检验溶液B中Mg2+、Ca2+是否除尽,通常分别取少量溶液B于两支试管中,进行如下实验:
步骤一:检验Mg2+是否除尽.向其中一支试管中加入______溶液(填化学式),看是否有沉淀生成.
步骤二:检验Ca2+是否除尽.向另一支试管中加入某溶液,看是否有沉淀生成.效果最好的是______(填字母).
A、Na2CO3 B、Na2SO3 C、Na2C2O4
【获取纯净食盐】
(4)对溶液B加热并不断滴加6mol•L-1的盐酸溶液,同时用pH试纸检测溶液,直至pH=5时停止加盐酸,得到溶液C.该操作的目的是______.
(5)将溶液C倒入______(填仪器名称)中,加热蒸发并用玻璃棒不断搅拌,直到______时(填现象),停止加热.
【问题讨论】
(6)在除杂过程中,向粗盐悬浊液中加混合液A时需要加热,目的是______,该操作中控制溶液pH=12可确保Mg2+除尽,根据提供的数据计算,溶液B中Mg2+物质的量浓度将被控制在______以下.
-
粗盐提纯的研究.
【有关资料】
| 化学式 | CaCO3 | CaSO3 | CaC2O4 | Mg(OH)2 |
| Ksp | 4.96×10-9 | 4.96×10-9 | 2.34×10-9 | 5.61×10-12 |
某研究性学习小组对粗盐的提纯和检验进行研究,并提出一些新的方案.已知该粗盐样品中主要含有不溶性杂质、Mg2+、Ca2+等(忽略SO42-的存在),该小组设计流程如下:

【设计除杂过程】
(1)操作①中需要使用的玻璃仪器有______、______.操作②的名称为______,若在操作②结束后发现溶液B略有浑浊,应采取的措施是______.
(2)混合液A的主要成分是______.(填化学式)
【检验除杂效果】
(3)为检验溶液B中Mg2+、Ca2+是否除尽,通常分别取少量溶液B于两支试管中,进行如下实验:
步骤一:检验Mg2+是否除尽.向其中一支试管中加入______溶液(填化学式),看是否有沉淀生成.
步骤二:检验Ca2+是否除尽.向另一支试管中加入某溶液,看是否有沉淀生成.效果最好的是______(填字母).
A、Na2CO3 B、Na2SO3 C、Na2C2O4
【获取纯净食盐】
(4)对溶液B加热并不断滴加6mol•L-1的盐酸溶液,同时用pH试纸检测溶液,直至pH=5时停止加盐酸,得到溶液C.该操作的目的是______.
(5)将溶液C倒入______(填仪器名称)中,加热蒸发并用玻璃棒不断搅拌,直到______时(填现象),停止加热.
【问题讨论】
(6)在除杂过程中,向粗盐悬浊液中加混合液A时需要加热,目的是______,该操作中控制溶液pH=12可确保Mg2+除尽,根据提供的数据计算,溶液B中Mg2+物质的量浓度将被控制在______以下.
-
粗盐提纯的研究.
【有关资料】
| 化学式 | CaCO3 | CaSO3 | CaC2O4 | Mg(OH)2 |
| Ksp | 4.96×10-9 | 4.96×10-9 | 2.34×10-9 | 5.61×10-12 |
某研究性学习小组对粗盐的提纯和检验进行研究,并提出一些新的方案.已知该粗盐样品中主要含有不溶性杂质、Mg2+、Ca2+等(忽略SO42-的存在),该小组设计流程如下:

【设计除杂过程】
(1)操作①中需要使用的玻璃仪器有______、______.操作②的名称为______,若在操作②结束后发现溶液B略有浑浊,应采取的措施是______.
(2)混合液A的主要成分是______.(填化学式)
【检验除杂效果】
(3)为检验溶液B中Mg2+、Ca2+是否除尽,通常分别取少量溶液B于两支试管中,进行如下实验:
步骤一:检验Mg2+是否除尽.向其中一支试管中加入______溶液(填化学式),看是否有沉淀生成.
步骤二:检验Ca2+是否除尽.向另一支试管中加入某溶液,看是否有沉淀生成.效果最好的是______(填字母).
A、Na2CO3 B、Na2SO3 C、Na2C2O4
【获取纯净食盐】
(4)对溶液B加热并不断滴加6mol•L-1的盐酸溶液,同时用pH试纸检测溶液,直至pH=5时停止加盐酸,得到溶液C.该操作的目的是______.
(5)将溶液C倒入______(填仪器名称)中,加热蒸发并用玻璃棒不断搅拌,直到______时(填现象),停止加热.
【问题讨论】
(6)在除杂过程中,向粗盐悬浊液中加混合液A时需要加热,目的是______,该操作中控制溶液pH=12可确保Mg2+除尽,根据提供的数据计算,溶液B中Mg2+物质的量浓度将被控制在______以下.
-
常温下,有关物质的溶度积如下
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
下列有关说法不正确的是( )
A.常温下,除去NaCl溶液中的MgCl2杂质,选用NaOH溶液比Na2CO3溶液效果好
B.常温下,除去NaCl溶液中的CaCl2杂质,选用NaOH溶液比Na2CO3溶液效果好
C.向含有Mg 2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg 2+)∶c(Fe3+)=2 .125×1021
D.将适量的Ca(OH)2固体溶于100mL水中,刚好达到饱和[c(Ca2+)=1.054×10-2mol/L],若保持温度不变, 向其中加入100mL 0.012mol/L的NaOH,则该溶液变为不饱和溶液。
-
常温下,有关物质的溶度积如下表所示。
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe(OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
下列有关说法不正确的是( )
A.常温下,除去NaCl溶液中的MgCl2杂质,选用NaOH溶液比Na2CO3溶液效果好
B.常温下,除去NaCl溶液中的CaCl2杂质,选用Na2CO3溶液比NaOH溶液效果好
C.常温下,向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)=2.125×1021:1
D.无法利用Ca(OH)2制备NaOH
-
已知:Ⅰ.碳酸钠的饱和溶液在不同温度下析出的溶质如图所示:
Ⅱ、25℃时有关物质的溶度积如下:
| 物质 | CaCO3 | MgCO3 | Ca(OH)2 | Mg(OH)2 | Fe (OH)3 |
| Ksp | 4.96×10-9 | 6.82×10-6 | 4.68×10-6 | 5.61×10-12 | 2.64×10-39 |
工业碳酸钠(纯度约为98%)中含有Ca2+、Mg2+、Fe3+、Cl-和SO42-等杂质,提纯工艺线路如下:
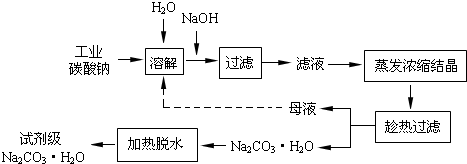
(1)加入NaOH溶液时,反应的离子方程式为__________________;
(2)向含有Mg2+、Fe3+的溶液中滴加NaOH溶液,当两种沉淀共存且溶液的pH=8时,c(Mg2+):c(Fe3+)= ___________;
(3)“母液”中除了含有Na+、CO32-外,还含有_________等离子。
(4)有人从“绿色化学”角度设想将“母液”沿流程中虚线所示进行循环使用。请你分析实际工业生产中是否可行_________(填“可行”或“不可行”),并说明理由__________________;
(5)已知:Na2CO3•10H2O(s)=Na2CO3(s)+10H2O(g)△H=+532.36kJ•mol-1
Na2CO3•10H2O(s)=Na2CO3•H2O(s)+9H2O(g) △H=+473.63kJ•mol-1
写出Na2CO3•H2O脱水反应的热化学方程式__________________;
-
25℃时,CaCO3、CaC2O4的Ksp分别为3.4×10—9和2.3×10—9,醋酸、HCN的Ka分别为1.75×10—5和4.9×10—10,分离CaCO3和CaC2O4固体混合物(不要求复原)。应选择的试剂为
A.盐酸 B.硝酸 C.乙酸 D.HCN
-
“变化观念与平衡思想”是化学学科的核心素养,室温时0.10mol/L草酸钠溶液中存在多个平衡,其中有关说法正确的是(已知室温时,Ksp(CaC2O4)=2.4×10-9)( )
A.若将溶液不断加水稀释,则水的电离程度增大
B.溶液中各离子浓度大小关系c(Na+)>c(C2O42-)>c(OH-)>c(H+)>c(HC2O4-)
C.若用pH计测得溶液的pH=a,则H2C2O4的第二级电离平衡常数Ka2=1013-2a
D.向溶液中加入等体积CaCl2溶液,当加入的CaCl2溶液浓度大于2.4×10-8mol/L时即能产生沉淀
-
“变化观念与平衡思想”是化学学科的核心素养,室温时,0.1 mol·L−1草酸钠溶液中存在多个平衡,其中有关说法正确的是[己知室温时,Ksp(CaC2O4)=2.4×10−9]
A.若将溶液不断加水稀释,则水的电离程度增大
B.溶液中各离子浓度大小关系:c(Na+)> c(C2O42−)> c(OH−)> c(H+)> c(HC2O4−)
C.若用pH计测得溶液的pH=9,则H2C2O4的第二级电离平衡常数Ka2=10−5
D.向溶液中加入等体积CaCl2溶液,当加入的CaCl2溶液浓度大于2.4×10−8 mol·L−1 时即能产生沉淀
-
“变化观念与平衡思想”是化学学科的核心素养,室温时,0.1 mol·L-1草酸钠溶液中存在多个平衡,其中有关说法正确的是[己知室温时,Ksp(CaC2O4)=2.4×10-9]
A. 若将溶液不断加水稀释,则水的电离程度增大
B. 溶液中各离子浓度大小关系:c(Na+)> c(C2O42-)> c(OH-)> c(H+)> c(HC2O4-)
C. 若用pH计测得溶液的pH=9,则H2C2O4的第二级电离平衡常数Ka2=10-5
D. 向溶液中加入等体积CaCl2溶液,当加入的CaCl2溶液浓度大于2.4×10-8 mol·L-1 时即能产生沉淀



