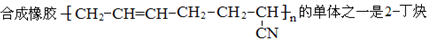-
(12分)已知:硫酸铜溶液中滴入氨基乙酸钠(H2N-CH2-COONa)即可得到配合物A。其结构如(下面左图):

(1)Cu元素基态原子的外围电子排布式为 。
(2)元素C、N、O的第一电离能由大到小排列顺序为 。
(3)A中碳原子的轨道杂化类型分别为 。
(4)1mol氨基乙酸钠(H2N-CH2-COONa)含有σ键的数目为 。
(5)氨基乙酸钠分解产物之一为二氧化碳。写出二氧化碳的一种等电子体: (写化学式)。
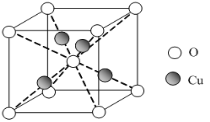
(6)已知:硫酸铜灼烧可以生成一种红色晶体,其结构如(上面右图),则该化合物的化学式是 。
-
已知:硫酸铜溶液中滴入氨基乙酸钠(H2N-CH2-COONa)即可得到配合物A。其结构如图:

(1)Cu元素基态原子的外围电子排布式为 。
(2)元素C、N、O的第一电离能由大到小排列顺序为 。
(3)A中碳原子的轨道杂化类型为 。
(4)1mol氨基乙酸钠(H2N-CH2-COONa)含有σ键的数目为 。
(5)氨基乙酸钠分解产物之一为二氧化碳。写出二氧化碳的一种等电子体: (写化学式)。
(6)已知:硫酸铜灼烧可以生成一种红色晶体,其结构如图,则该化合物的化学式是 。
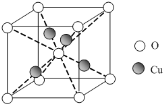
-
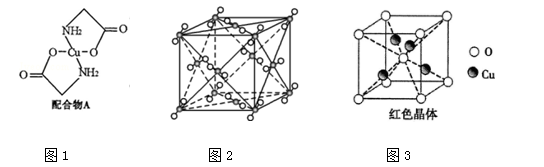
已知:硫酸铜溶液中滴入氨基乙酸钠(H2N﹣CH2﹣COONa)即可得到配合物A.其结构如图1:
(1)Cu元素基态原子的外围电子排布式为 。
(2)元素C、N、O的第一电离能由大到小排列顺序为 。
(3)配合物A中碳原子的轨道杂化类型为 。
(4)1mol氨基乙酸钠(H2N﹣CH2﹣COONa)含有σ键的数目为 。
(5)氨基乙酸钠分解产物之一为二氧化碳,其结构如图2,它属于________晶体,每个CO2分子与________个CO2分子紧邻。写出二氧化碳的一种等电子体: (写化学式)。
(6) 已知:硫酸铜灼烧可以生成一种红色晶体,其结构如图3,则该化合物的化学式是 。
-
Cu可形成多种配合物,某同学在探究配合物的形成时做了以下实验,根据下列信息回答问题:
(1)向盛有硫酸铜水溶液的试管里逐滴加入氨水,首先出现蓝色沉淀,继续滴加氨水,蓝色沉淀溶解,得到深蓝色的透明溶液,请写出先后发生反应的离子方程式___________。
(2)再向深蓝色透明溶液加入乙醇,析出深蓝色的晶体。深蓝色晶体的化学式为__________________。
(3)根据以上实验过程,判断NH3和H2O与Cu2+的配位能力:NH3________(填“>”“=”或“<”)H2O。
(4)已知Ti3+可形成配位数为6,颜色不同的两种配合物晶体,一种为紫色,另一种为绿色。两种晶体的组成皆为TiCl3·6H2O。为测定这两种晶体的化学式,某同学设计了如下实验:
a、分别取等质量的两种配合物晶体的样品配成待测溶液;
b、分别往待测溶液中滴入AgNO3溶液,均产生白色沉淀;
c、沉淀完全后分别过滤得两份沉淀,经洗涤干燥后称量,发现原绿色晶体的水溶液与AgNO3溶液反应得到的白色沉淀质量为紫色晶体的水溶液反应得到沉淀质量的 。绿色晶体配合物的化学式为____________,由Cl所形成的化学键类型是_____________。
。绿色晶体配合物的化学式为____________,由Cl所形成的化学键类型是_____________。
-
金属及其化合物在科学研究和工业生产中具有重要的用途。
(1)三氯化铁溶液用于检验食用香精乙酰乙酸乙酯时,会生成紫色配合物,其配离子结构如图所示:
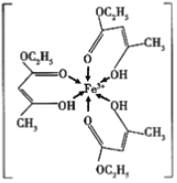
①此配合物中,铁离子价电子排布图为_____;
②此配离子中碳原子的杂化轨道类型为_____;
③此配离子中含有的化学键为_____。
A.离子键 B.金属键 C.极性键 D.非极性键 E.配位键 F.氢键 G.σ键 H.π键
(2)NO2-与钴盐形成的配离子[Co(NO2)6]3-可用于检验K+的存在。NO2-离子的VSEPR模型名称为_____,K3[Co(NO2)6]是黄色沉淀,该物质中四种元素的电负性由大到小的顺序是_____。
(3)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和CrO2,其中适合作录音带磁粉原料的是_____。
(4)锰的一种配合物的化学式为Mn(BH4)2(THF)3,写出两种与BH4-互为等电子体的微粒_____(请写一个分子和一个离子)。
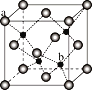
(5)ZnS在荧光体、光导体材料、涂料、颜料等行业中应用广泛,立方ZnS晶体的结构如图所示,a的配位数为_____,已知晶胞密度为ρ g/cm3,则相邻2个b微粒之间的距离为_____nm(列计算式)。
-
向盛有硫酸铜水溶液的试管里加入氨水,首先形成难溶物,继续添加氨水,难溶物溶解得到深蓝色的透明溶液.下列对此现象说法正确的是 ( )
A. 沉淀溶解后,将生成深蓝色的配合离子[Cu(NH3)4] 2+
B. 反应后溶液中不存在任何沉淀,所以反应前后Cu2+的浓度不变
C. 向反应后的溶液加入乙醇,溶液没有发生变化
D. 在[Cu(NH3)4] 2+离子中,Cu2+给出孤对电子,NH3提供空轨道
-
下列说法正确的是
A.硫酸钠溶液和醋酸铅溶液均能使蛋白质变性
B.油脂是高级脂肪酸甘油酯,均不能发生氢化反应
C.H2N—CH2—COOH既能与盐酸反应、又能与氢氧化钠溶液反应
D.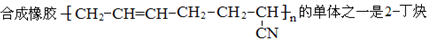
-
下列说法正确的是( )
A. 硫酸钠溶液和醋酸铅溶液均能使蛋白质变性
B. 油脂是高级脂肪酸的甘油酯,均不能发生氢化反应
C. H2N—CH2——COOH既能与盐酸反应,又能与氢氧化钠溶液反应
D. 在蛋白质的渗析、盐析、变性过程中都发生了化学变化
-
已知NH3分子可与Cu2+形成配合物离子[Cu(NH3)4]2+,则除去硫酸铜溶液中少量硫酸可选用的试剂是
A.NaOH B.NH3 C.BaCl2 D.Cu(OH)2
-
(填化学式)在空气中:将氯化铁溶液蒸干并灼烧得到的固体物质 _____;碳酸氢钠溶液蒸干并灼烧得到的固体物质________;硫酸铝溶液蒸干得到的固体物质________;亚硫酸钠溶液蒸干得到的固体物质________。