-
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:(己知:Ksp[Fe(OH)3]=4.0×10-38)
I:向废液中投入过量铁屑,充分反应后分离出固体和滤液:
II:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气.
回答下列问题:
(1)FeCl3蚀刻铜箔反应的离子方程式为______:
(2)过程I 加入铁屑的主要作用是______,分离得到固体的主要成分是______,从固体中分离出铜需采用的方法是______;
(3)过程II中发生反应的化学方程式为______;
(4)过程II中调节溶液的pH为5,金属离子浓度为______.(列式计算)高三化学解答题中等难度题查看答案及解析
-
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:
Ⅰ:向废液中投入过量铁屑,充分反应后分离出固体和滤液;
Ⅱ:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
回答下列问题:
(1)FeCl3蚀刻铜箔反应的离子方程式为________
。
(2)过程Ⅰ加入铁屑的主要作用是 ,分离得到固体的主要成分是 ,从固体中分离出铜需采用的方法是________
。
(3)过程Ⅱ中发生反应的化学方程式为 。
高三化学填空题中等难度题查看答案及解析
-
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:
Ⅰ:向废液中投入过量铁屑,充分反应后分离出固体和滤液;
Ⅱ:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
已知:Ksp[Fe(OH)3]=4.0×10-38
回答下列问题:
(1)FeCl3蚀刻铜箔反应的离子方程式为________________________________________;
(2)过程Ⅰ加入铁屑的主要作用是__________________,分离得到固体的主要成分是________,从固体中分离出铜需采用的方法是___________________________________;
(3)过程Ⅱ中发生反应的化学方程式为________________________________;
(4)过程Ⅱ中调节溶液的pH为5,金属离子浓度为__________________________。(列式计算)
高三化学填空题中等难度题查看答案及解析
-
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:
Ⅰ.向废液中投入过量铁屑,充分反应后分离出固体和滤液;
Ⅱ.向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
已知:Ksp[Fe(OH)3]=4.0×10-38
回答下列问题:
(1)FeCl3蚀刻铜箔反应的离子方程式为______________________________;
(2)过程Ⅰ加入铁屑的主要作用是________,分离得到固体的主要成分是______________,从固体中分离出铜需采用的方法是________________;
(3)过程Ⅱ中发生反应的化学方程式为______________;
(4)过程Ⅱ中调节溶液的pH为5,金属离子浓度为________。(列式计算)
高三化学填空题中等难度题查看答案及解析
-
(9分)
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下:
I:向废液中投入过量铁屑,充分反应后分离出固体和滤液;
II:向滤液中加入一定量石灰水,调节溶液pH,同时鼓入足量的空气。
己知:Ksp[Fe(OH)3]= 4.0×10-38
回答下列问题:
(1)FeCl3蚀刻铜箔反应的离子方程式为 :
(2)过程I 加入铁屑的主要作用是 ,分离得到固体的主要成分是 ,从固体中分离出铜需采用的方法是 ;
(3)过程II中发生反应的化学方程式为 ;
(4)过程II中调节溶液的pH为5,金属离子浓度为 。(列式计算)
高三化学填空题中等难度题查看答案及解析
-
在FeCl3溶液蚀刻铜箔制造电路板的工艺中,废液处理和资源回收的过程简述如下,请回答下列问题:
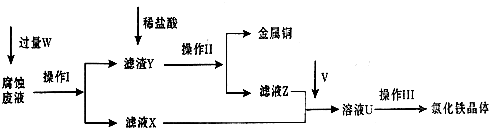
(1)请写出FeCl3溶液与铜反应的离子方程式:______;操作Ⅰ加入的试剂W是______.
(2)操作Ⅱ之前最好加入适量稀盐酸,某同学用10mol•L-1 的浓盐酸配制250mL 1mol•L-1 的稀盐酸,并进行有关实验.
①需要量取浓盐酸______mL.
②配制该稀盐酸时除量筒、烧杯、玻璃棒外,还必须用到的仪器有______、______.
③用已知浓度的氢氧化钠溶液滴定稀盐酸,滴定过程中眼睛应注视______,实验时未用标准液润洗滴定管,测得锥形瓶中待测液的浓度______实际浓度.(填“>”、“<”或“=”).
(3)操作Ⅲ前需要通入气体V,请写出实验室制取气体V的化学方程式:______ MnCl2+Cl2↑+2H2O高三化学解答题中等难度题查看答案及解析
-
(10分)电子工业中,可用FeCl3—HCl溶液作为印刷电路铜板蚀刻液。某探究小组设计如下线路处理废液和资源回收:
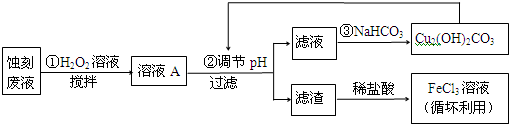
请回答:
(1)FeCl3—HCl溶液蚀刻铜板后的废液中含有的金属阳离子是 。
(2)FeCl3蚀刻液中加入盐酸的目的:可以 ,又可提高蚀刻速率。
(3)步骤①中加入H2O2溶液的目的是 。
(4)已知:生成氢氧化物沉淀的pH
Cu(OH)2
Fe(OH)2
Fe(OH)3
开始沉淀时
4.7
7.0
1.9
沉淀完全时
6.7
9.0
3.2
根据表中数据推测调节pH的范围是 。
(5)写出步骤②中生成CO2的一个离子方程式_____(已知Cu2(OH)2CO3不易溶于水)。
(6)写出步骤③生成Cu2(OH)2CO3的离子方程式___________________。
高三化学实验题困难题查看答案及解析
-
电子工业常用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板。某工程师为了从废液中回收铜,重新获得FeCl3溶液,设计了下列实验步骤:
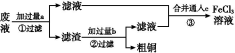
写出一个能证明还原性Fe比Cu强的离子方程式: 。
该反应在上图步骤 中发生。请根据上述反应设计一个原电池,在方框中画出简易装置图(标出电极名称、电极材料、电解质溶液)。
上述过程回收的铜是粗铜,为了获得更纯的铜必须进行电解精炼。写出电解精炼时阳极材料及主要的电极反应式 。
高三化学填空题中等难度题查看答案及解析
-
铁、铝、铜及其化合物在生产、生活中有着广泛的应用。请回答下列问题:
(1)铝离子的结构示意图为 。
(2)制造电路板的工艺中,FeCl3溶液可以蚀刻铜箔,该反应的离子方程式为 。
(3)氢氧化铝是医用的胃酸中和剂的一种。用离子方程式表示其作用机理是 。
(4)与明矾相似,硫酸铁也可用作絮凝剂,在使用时发现硫酸铁并不能使酸性废水中的悬浮物沉降除去,其原因是 。
(5)下表中,对陈述Ⅰ、Ⅱ的正确性的判断都正确的是 (填字母序号)。
选项
陈述Ⅰ
陈述Ⅱ
判断
A
铁是地壳中含量最高的金属元素
铁是人类最早使用的金属材料
Ⅰ对;Ⅱ对。
B
常温下铁与稀硫酸反应生成氢气
高温下氢气能还原氧化铁生成铁
Ⅰ对;Ⅱ对。
C
铁比铝更易锈蚀
铝比铁活泼
Ⅰ错;Ⅱ对。
D
铝在空气中表面生成致密氧化膜
可用铝罐储存运输浓硫酸、浓硝酸
Ⅰ错;Ⅱ对。
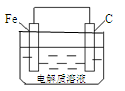
(6)钢铁的析氢腐蚀简单示意图如下图所示,正极的电极反应式为 。该图某处稍作修改即可成为钢铁电化学防护的简单示意图,其中一种方法是将C换成Zn等比Fe活泼的金属,请完善另一种方法的示意图。
高三化学填空题困难题查看答案及解析
-
26.(14分)铁、铝、铜及其化合物在生产、生活中有广泛的用途,试回答下列问题:
(1)制造电路板的工艺中,FeCl3溶液可以蚀刻铜箔,请写出该反应的离子方程式 ;
(2)已知铜与稀硫酸不反应,但将铜片在稀硫酸中长时间加热时溶液会呈蓝色,请用化学方程式表示原因 。
(3)氯化铝广泛用于有机合成和石油工业的催化剂。将铝土矿粉(主要成分为Al2O3)与焦炭混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式________________________。
(4)已知Cu2S可以和硝酸反应,请配平下列化学反应方程式:
□Cu2S+□HNO3
□CuSO4 +□ Cu(NO3)2+□NO↑+ □
(5)某校兴趣小组欲测定一种铁铝硅合金(FexAlySiz)粉末的组成,提出如下方案:准确称取1.46g该合金粉末,加入过量盐酸溶液充分反应后过滤,测定剩余固体质量0.07g。向滤液中滴加足量浓NaOH溶液,充分搅拌、过滤、洗涤得固体。再将所得固体充分加热、灼烧得红棕色粉末1.60g,通过计算确定此合金的组成为 (填化学式)。
高三化学填空题困难题查看答案及解析