-
(18分)下面是某同学研究氯气性质过程中的一个片断。请你帮助他完成部分实验并补全实验记录。
[观察]氯气的颜色、状态:________色________状态;闻氯气的气味:________气味。
[预测]氯气是一种非金属单质,它可能具有性质有________。
从元素化合价的角度分析,它可能具有性质有________。
[实验探究]
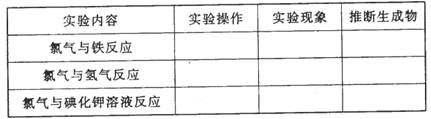
[实验结论]
(1)通过比较氯气和曾经学习过的氧气等非金属单质的性质,可推知氯气的化学性________,能与________反应。
(2)在上述过程中,该同学都用到了哪些研究物质性质的方法?
________。
(3)说明闻气体气味的方法。________。
-
新制氯水中含有多种粒子,某校化学研究性学习小组的同学为探究其性质,做了如下实验,请你帮助完成:
(1)HClO不稳定,见光易分解生成HCl和O2。请设计实验证明有O2生成 。
(2)氯气能使湿润的红色布条退色。对于使湿润的红色布条退色的物质,同学们的看法不一致,认为氯水中存在的几种粒子都有可能。请你设计实验,得出正确结论。
| 提出问题 | 收集资料 | 提出假设 | 验证假设 | 得结论出 |
| 氯水中何种物质能使湿润的红色布条退色? | ①氯气有强氧化性 ②氯气与冷水反应生成盐酸和次氯酸 ③次氯酸有强氧化性 | ① ② ③ ④H2O使布条退色 | ①:实验①:把红色干布条放入充满氯气的集气瓶中,布条不退色 实实验②: ; 实验③:把红色布条放在水里,布条不退色 | |
-
新制氯水中含有多种粒子,某校化学研究性学习小组的同学为探究其性质,做了如下实验,请你帮助完成:

(1)氯碱工业生产中同时有副产品氯气生成,反应的化学方程式为____________。
(2)新制的饱和氯水与碳酸钙反应时制取较浓HClO溶液的方法之一。
实验一:定性研究
A 在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去;
B 过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
C 为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生。经检测,上述实验中产生的无色气体均为CO2。
①已知:Ka1(H2CO3)=4.45×10-7,Ka2(HCO3-)=5.61×10-11,Ka(HClO)=2.95×10-8,写出将少量的氯气通入到过量的碳酸钠溶液中所发生反应的离子方程式:____________。
②试推测步骤B的滤液中的溶质除了CaCl2,HClO外,还有____________。
实验二:定量研究
在仪器A内放有用塑料网包住的块状碳酸钙(过量)和150mL新制饱和氯水,按如图所示的装置进行实验(实验前仪器B中充满了饱和NaHCO3溶液,部分夹持装置已省略),待不再产出气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热A中的液体,直到仪器B中的气体不再增加(不考虑HClO的分解)。
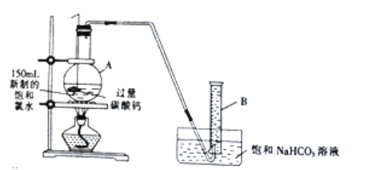
③仪器A的名称为__________。
④准确读出仪器B中气体体积的实验操作步骤依次是:
a.____________;
b.____________;
c.平视与刻度线相切的液面读数。
⑤实验结束后,测得仪器B中收集到的气体体积在标准状况下为168mL,则150mL新制的饱和氯水与过量碳酸钙完全反应后,所得溶液中HClO的物质的量浓度为__________。(反应前后,溶液体积变化忽略不计)。
-
(15分)新制氯水中含有多种粒子,某校化学研究性学习小组的同学为探究其性质,做了如下实验,请你帮助完成:
(1)氯气能使湿润的红色布条褪色。使其褪色的微粒的化学式是______________
(2)将氯水在光照上一段时间,溶液颜色逐渐变浅,其有关反应的化学方程式为:
________、________
(3)平衡常数(K)表明了封闭体系的可逆反应在给定的温度下进行的程度,对于同一个类型的反应,平衡常数越大,表明反应进行的程度越大。
H2CO3 HCO3-+ H+ Ka1(H2CO3)=4.45×10-7
HCO3-+ H+ Ka1(H2CO3)=4.45×10-7
HCO3- CO32-+H+ Ka2(HCO3-)=5.61×10-11
CO32-+H+ Ka2(HCO3-)=5.61×10-11
HClO H++ClO- Ka(HClO)=2.95×10-8
H++ClO- Ka(HClO)=2.95×10-8
请依据以上电离平衡常数,请写出将少量的氯气通入到过量的碳酸钠溶液中所发生反应的离子方程式:________
(4)饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一。
实验一、定性研究:
①在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应, 有少量气泡产生,溶液浅黄绿色褪去;
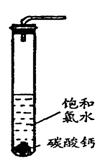 ②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
③为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生。
经检测,上述实验中产生的无色气体均为CO2。
请回答:
①反应后所得的溶液漂白性增强的原因是_____________________________________________
②依据上述实验可推知:②的滤液中的溶质除CaCl2、HClO外,还含有______ _。
实验二、定量研究:
在圆底烧瓶底部,有一用塑料网包住的过量块状 碳酸钙和150mL饱和氯水,按如图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加(不考虑HClO的分解)。
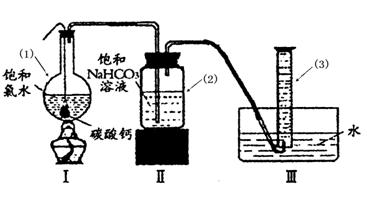
请回答:
③写出仪器(1)与仪器(3)的名称:(1)________(3)________
④为减少用装置Ⅲ收集气体过程中CO2因溶解而造成的损失,且水槽中仍然为水,请你对装置Ⅲ进行改进,最简单的方法是________。
⑤如何准确读出量筒中气体的体积
a.___________________________________________________________________________________________
b.上下移动量筒至量筒内液面与水槽液面相平
c._________________________________________
-
新制的饱和氯水中含有多种做粒,某校化学研究性学习小组的同学为探究其性质,做了如下实验,请你帮助完成。
(1)氯气能使湿润的红色布条褪色,使其褪色的微粒的化学式是__________。
(2)将氯水光照一段时间后,溶液颜色逐渐变浅,有关反应的化学方程式为__________、__________。
(3)新制的饱和氯水与碳酸钙的反应是制取较浓HClO 溶液 的 方 法 之一。
实验一 定性研究:

Ⅰ.如图所示,在试管中加入过量的块状碳酸钙,再加入约20 mL新制的饱和氯水,充分反应,有少量气泡产生,溶液浅黄绿色褪去。
Ⅱ.过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强。
Ⅲ.为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体,
将第三份加热,观察到溶液变浑浊且有大量无色气体产生。
经检测,上述实验中产生的无色气体均为CO2。
①反应后所得的溶液漂白性增强的原因是__________________________________________________。
②依据上述实验可推知:步骤Ⅱ的滤液中的溶质除CaCl2、HClO外,还有__________。
实验二 定量研究:
在仪器A内,放有塑料网包住的块状碳酸钙(过量)和150 mL新制的饱和氯水,按如图所示装置实验(实验前仪器B中充满了饱和NaHCO3溶液),待不再产生气泡后,将塑料网中剩余的碳酸钙提出液面,密封后再加热烧瓶中的液体,直到仪器B中的气体不再增加(不考虑HClO的分解)。

③仪器A的名称为__________。
④准确读出仪器B中气体体积的实验操作步骤依次是:a.等待仪器A冷却到室温;b.____________;c. 平视与刻度线相切的液面读数。
⑤实验结束后,测得仪器B中收集到的气体体积在标准状况下为168mL,则150mL 新制的饱和氯水与过量碳酸钙完全反应后,所得溶液中HClO的物质的量浓度为__________。(反应前后,溶液体积变化忽略不计)
-
新制氯水中含有多种粒子,某校化学研究性学习小组的同学为探究其性质,做了如下实验,请你帮助完成:
(1)氯气能使湿润的红色布条褪色。使其褪色的微粒的化学式是______________
(2)将氯水在光照上一段时间,溶液颜色逐渐变浅,其有关反应的化学方程式为:
________、________
(3)平衡常数表明了封闭体系的可逆反应在给定的温度下进行的程度,对于同一个类型的反应,平衡常数越大,表明反应进行的程度越大。
H2CO3 
 + H+ Ka1(H2CO3)=4.45×10—7
+ H+ Ka1(H2CO3)=4.45×10—7


 +H+ Ka2(HCO3-)=5.61×10-11
+H+ Ka2(HCO3-)=5.61×10-11
HclO  H++
H++ Ka(HClO)=2.95×10-8
Ka(HClO)=2.95×10-8
请依据以上电离平衡常数,请写出将少量的氯气通入到过量的碳酸钠溶液中所发生反应的离子方程式:
(4)饱和氯水与石灰石的反应是制取较浓HClO溶液的方法之一。

实验一、定性研究:
① 在试管中加入过量的块状碳酸钙,再加入约20mL饱和氯水,充分反应,
有少量气泡产生,溶液浅黄绿色褪去;
② 过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
③ 为了确定反应产物,将滤液分为三份,分别进行以下实验:
第一份与石灰水混合,立即产生大量白色沉淀;
第二份与稀盐酸混合,立即产生大量无色气体;
将第三份加热,看到溶液变浑浊且有大量无色气体产生。
经检测,上述实验中产生的无色气体均为CO2。
请回答:
① 反应后所得的溶液漂白性增强的原因是_____________________________________________
②依据上述实验可推知:②的滤液中的溶质除CaCl2、HClO外,还含有______ _________。
实验二、定量研究:
在圆底烧瓶底部,有一用塑料网包住的过量块状 碳酸钙和150mL饱和氯水,按如图所示装置实验,待不再产生气泡后,将塑料网中剩余的石灰石提出液面,密封后再加热、煮沸烧瓶中的液体,直到量筒中的气体不再增加(不考虑HClO的分解)。
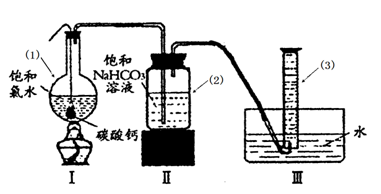
请回答:
③ 写出仪器(1)与仪器(3)的名称
(1)________(3)________
④ 为减少用装置Ⅲ收集气体过程中CO2因溶解而造成的损失,且水槽中仍然为水,请你对装置Ⅲ进行改进,最简单的方法是。
⑤ 如何准确读出量筒中气体的体积
a_________________________
b 上下移动量筒至量筒内液面与水槽液面相平
c ________
-
某研究小组通过实验探究Cu及其化合物的性质,操作正确且能达到实验目的的是( )
A.将铜丝插入浓硫酸中并加热,反应后再加入水,观察硫酸铜溶液的颜色
B.常温下将铜丝伸入盛满氯气的集气瓶中,观察CuCl2的生成
C.将CuCl2溶液在蒸发皿中加热蒸干,得到无水CuCl2固体
D.将表面有铜绿[Cu2(OH)2CO3]的铜器放入盐酸中浸泡,除去铜绿
-
某研究小组通过实验探究Cu及其化合物的性质,操作正确且能达到实验目的的是
A.将铜丝插入浓硫酸中并加热,反应后再加入水,观察硫酸铜溶液的颜色
B.常温下将铜丝伸入盛满氯气的集气瓶中,观察CuCl2的生成
C.将CuCl2溶液在蒸发皿中加热蒸干,得到Cu(OH)2固体
D.将表面有铜绿[Cu2(OH)2CO3]的铜器放入盐酸中浸泡,除去铜绿
-
某研究小组通过实验探究Cu及其化合物的性质,下列操作正确且能达到目的的是( )
A.将铜丝插入浓硫酸中加热,反应后把水加入反应器中,观察硫酸铜溶液的颜色
B.常温下将铜丝伸入盛满氯气的集气瓶中,观察CuCl2的生成
C.将CuCl2溶液在蒸发皿中加热蒸干,得到无水CuCl2固体
D.将表面有铜绿[Cu2(OH)2CO3]的铜器放入盐酸中浸泡,除去铜绿
-
某研究小组通过实验探究Cu及其化合物的性质,操作正确且能达到目的的是
A.将铜丝插入浓硫酸中加热,反应后把水加入反应器中,观察硫酸铜溶液的颜色
B.常温下将铜丝伸入盛满氯气的集气瓶中,观察CuCl2的生成
C.将CuCl2溶液在蒸发皿中加热蒸干,得到无水CuCl2固体
D.将表面有铜绿[Cu2(OH)2CO3]的铜器放入盐酸中浸泡,除去铜绿



 ②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;
②过滤,将滤液滴在有色布条上,发现其比氯水的漂白性更强;



