-
草酸(H2C2O4)与高锰酸钾在酸性条件下能够发生如下反应:
2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,
【实验1】甲同学用8.00 mL 0.001 mol/L KMnO4溶液与5.00 mL 0.01 mol/L
H2C2O4溶液反应,研究不同条件对化学反应速率的影响。改变的条件如下:
组别
KMnO4溶液
/ml
H2C2O4溶液
/ml
10%硫酸体积/mL
温度/℃
其他物质
Ⅰ
8.00
5.00
3.00
20
Ⅱ
8.00
5.00
3.00
30
Ⅲ
8.00
5.00
1.00
20
2.00 mL
蒸馏水
(1)如果研究温度对化学反应速率的影响,可用实验_________ 和________ 作对比(用Ⅰ~III表示)。
(2)对比实验Ⅰ和III,可以研究__________对化学反应速率的影响,实验Ⅲ中加入2.00 mL蒸馏水的目的是________________。
【实验2】乙同学在研究草酸与高锰酸钾在酸性条件下反应的影响因素时发现,草酸与酸性高锰酸钾溶液开始一段时间反应速率较慢,溶液褪色不明显,但不久后突然褪色,反应速率明显加快。
(1)针对上述现象,乙同学认为草酸与高锰酸钾反应放热,导致溶液温度升高,反应速率加快。从影响化学反应速率的因素看,你猜想还可能是 的影响。
(2)若用实验证明你的猜想,除了酸性高锰酸钾溶液和草酸溶液外,还需要选择的试剂最合理的是 (填字母)。A.硫酸钾 B.水 C.二氧化锰 D.硫酸锰
高二化学实验题困难题查看答案及解析
-
(12分)草酸与高锰酸钾在酸性条件下能够发生如下反应:
2MnO4- + 5H2C2O4 +6H+ =2Mn2+ +10CO2↑ +8H2O
用4mL0.001mol/LKMnO4溶液与2mL0.01mol/LH2C2O4溶液,研究不同条件对化学反应速率的影响。改变的条件如下:
组别
10%硫酸溶液的体积/mL
温度/℃
其他物质
Ⅰ
2mL
20
无
Ⅱ
2mL
20
10滴饱和MnSO4溶液
Ⅲ
2mL
30
无
Ⅳ
1mL
20
1mL蒸馏水
(1)如果研究催化剂对化学反应速率的影响,应使用实验 和 (用Ⅰ~Ⅳ表示,下同);如果研究温度对化学反应速率的影响,应使用实验 和 。
(2)对比实验Ⅰ和Ⅳ,可以研究 对化学反应速率的影响,实验Ⅳ中加入1mL蒸馏水的目的是 。
(3)在分析化学中常用Na2C2O4晶体作为基准物质测定KMnO4溶液的浓度。在H2SO4溶液中,反应如下:2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O
①用托盘天平称取W g Na2C2O4晶体。
②将WgNa2C2O4配成100 mL标准溶液,量取20.00 mL置于锥形瓶中,
酸性KMnO4溶液应装在________(填“酸式”或“碱式”)滴定管中。
③若滴定管的起始读数和终点读数如图所示,则酸性KMnO4的物质的浓度为________ (填表达式,用W表示)。

高二化学填空题困难题查看答案及解析
-
教材中用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
实验序号
A溶液
B溶液
①
20 mL 0.1 mol·L-1H2C2O4溶液
30 mL 0.01 mol·L-1KMnO4溶液
②
20 mL 0.2 mol·L-1
H2C2O4溶液
30 mL 0.01 mol·L-1KMnO4溶液

(1) 该实验探究的是________因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是-(填实验序号)。
(2)若实验①在2 min末收集了4.48 mL CO2(标准状况下),
则在2 min末,c(MnO4-)=________mol/L。
(3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定________来比较化学反应速率。
(4)小组同学发现反应速率总是如右图,其中t1~t2时间内速 率变快的主要原因可能是:①该反应放热、②________。
高二化学实验题困难题查看答案及解析
-
教材中用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
(1)该实验探究的是______因素对化学反应速率的影响.相同时间内针筒中所得CO2的体积大小关系是______>______(填实验序号).实验序号 A溶液 B溶液 ① 20mL 0.1mol•L-1
H2C2O4溶液30mL 0.01mol•L-1
KMnO4溶液② 20mL 0.2mol•L-1
H2C2O4溶液30mL 0.01mol•L-1
KMnO4溶液
(2)若实验①在2min末收集了4.48mL CO2(标准状况下),则在2min末,c(MnO4-)=______mol/L.
(3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定______来比较化学反应速率.
(4)小组同学发现反应速率总是如图二,其中t1~t2时间内速 率变快的主要原因可能是:①该反应放热、②______.
高二化学解答题中等难度题查看答案及解析
-
用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):

实验序号
A溶液
B溶液
①
20 mL 0.1 mol·L-1H2C2O4溶液
30 mL 0.01 mol·L-1KMnO4溶液
②
20 mL 0.2 mol·L-1H2C2O4溶液
30 mL 0.01 mol·L-1KMnO4溶液
(1)该实验探究的是________因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是________>________(填实验序号)。
(2)若实验①在2 min末收集了4.48 mL CO2(标准状况下),则在2 min末,c(MnO4-)=_______mol·L-1。(假设混合溶液体积为50 mL)
(3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定________来比较化学反应速率。
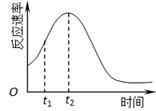
(4)小组同学发现反应速率总是如下图,其中t1~t2时间内速率变快的主要原因可能是:①产物Mn2+是反应的催化剂、②________。
高二化学实验题中等难度题查看答案及解析
-
(12分)用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4-(aq)+5H2C2O4(aq)+6H+(aq)=2Mn2+(aq)+10CO2(g)+8H2O(l) ΔH<0
一实验小组欲通过测定单位时间内生成CO2的体积,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化,所用注射器的容积充裕):
实验序号
A溶液
B溶液
①
20 mL 0.1 mol·L-1H2C2O4溶液
30 mL 0.01 mol·L-1KMnO4溶液
②
20 mL 0.2 mol·L-1H2C2O4溶液
30 mL 0.01 mol·L-1KMnO4溶液
(1)该实验探究的是 因素对化学反应速率的影响,如果实验完成时草酸与KMnO4均有剩余,则相同时间内针筒中所得CO2体积大小关系是: < (填实验序号)研究发现反应速率总是如图所示发生变化,则t1~t2时间内速率变快的主要原因可能是:①产物Mn2+是反应的催化剂,② 。

(3)若实验①在4 min末收集了4.48 mL CO2(标准状况),则4 min末c(MnO4-)= mol·L-1(假设溶液混合后体积为50 mL),此4 min内的平均速率为v(H2C2O4)= 。
(4)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可以通过测定 来比较化学反应速率。
高二化学实验题困难题查看答案及解析
-
用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4 -+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。某实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计方案如下(KMnO4溶液已酸化):
实验序号
A溶液
B溶液
①
20mL 0.lmol·L-l H2C2O4溶液
30mL 0.01mol.L-l KMnO4溶液
②
20mL 0.2mol·L-l H2C2O4溶液
30mL 0.01mol.L-l KMnO4溶液
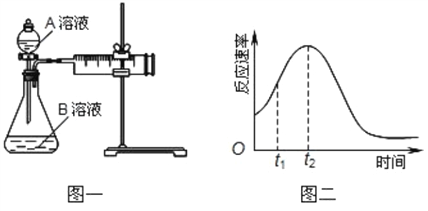
(1)该实验探究的是______对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是_____(填实验序号)。
(2)若实验①在2min末注射器的活塞向右移动到了b mL的位置,则这段时间的反应速率可表示为v(CO2)=______mL/min。若实验②在t min收集了4.48×10-3L CO2(标准状况下),则t min末c(MnO4-)=______。
(3)该小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是:①___________、②___________。
(4)已知草酸是一种二元弱酸,其电离常数K1=5.4×10-2、K2=5.4×10-5,写出草酸的电离方程式_______、________。试从电离平衡移动的角度解释K1>>K2的原因_______________。
高二化学实验题困难题查看答案及解析
-
用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4﹣+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O.一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):
实验序号
A溶液
B溶液
①
20mL 0.1mol·L﹣1H2C2O4溶液
30mL 0.01mol·L﹣1KMnO4溶液
②
20mL 0.2mol·L﹣
1H2C2O4溶液
30mL 0.01mol·L﹣1KMnO4溶液
(1)该实验探究的是 因素对化学反应速率的影响.相同时间内针筒中所得CO2的体积大小关系是 > (填实验序号).
(2)若实验①在2min末收集了2.24mL CO2(标准状况下),则在2min末,c(MnO4﹣)= mol/L.
(3)除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定 来比较化学反应速率.

(4)小组同学发现反应速率总是如图二,其中t1~t2时间内速率变快的主要原因可能是: .
高二化学填空题中等难度题查看答案及解析
-
(14分)用酸性KMnO4和H2C2O4(草酸)反应研究影响反应速率的因素,离子方程式为:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O。一实验小组欲通过测定单位时间内生成CO2的速率,探究某种影响化学反应速率的因素,设计实验方案如下(KMnO4溶液已酸化):

实验序号
A溶液
B溶液
①
20 mL 0.1 mol·L-1H2C2O4溶液
30 mL 0.01 mol·L-1KMnO4溶液
②
20 mL 0.2 mol·L-1H2C2O4溶液
30 mL 0.01 mol·L-1KMnO4溶液
(1) 该实验探究的是 因素对化学反应速率的影响。相同时间内针筒中所得CO2的体积大小关系是① ②(填“>”、“<”或“=”)。
(2) 若实验①在2 min末收集了4.48 mL CO2(标准状况下),则在2 min末,c(MnO4-)=_______mol·L-1。(假设混合溶液体积为50 mL)
(3) 除通过测定一定时间内CO2的体积来比较反应速率,本实验还可通过测定________________________________________________ 来比较化学反应速率。
(4) 小组同学发现反应速率总是如下图,其中t1~t2时间内速率变快的主要原因可能是:

①产物Mn2+是反应的催化剂、② 。
高二化学实验题困难题查看答案及解析
-
I、乙二酸俗名草酸,为了测定草酸晶体(H2C2O4·xH2O)中的x值。通过查阅资料,草酸易溶于水,水溶液可以用酸性KMnO4溶液进行滴定:2MnO4-+5H2C2O4+6H+=2Mn2++10CO2↑+8H2O,学习小组的同学设计了滴定的方法测定x值。
①称取1.260 g纯草酸晶体,将其制成100.00 mL水溶液为待测液。
②取25.00 mL待测液放入锥形瓶中,再加入适量的稀H2SO4。
③用浓度为0.1000 mol·L-1的酸性KMnO4标准溶液进行滴定,达到终点时消耗10.00 mL。
(1)滴定时,将酸性KMnO4标准液装在____________滴定管(填“酸式”或“碱式”)。
(2)本实验滴定达到终点的标志是__________________________。
(3)通过上述数据,求得x=________。
讨论:
①若滴定终点时俯视滴定管刻度,则由此测得的x值会________(填“偏大”“偏小”或“不变”,下同)。
②若滴定时所用的酸性KMnO4溶液因久置而导致浓度变小,则由此测得的x值会________。
II、(1)25℃时将amol•L-1的氨水与0.01mol•L-1的盐酸等体积混合所得溶液中c(NH4+)=c(Cl-),用含a的代数式表示NH3•H2O的电离平衡常数Kb=______
(2)25℃时,H2SO3
HSO3-+ H+的电离常数Ka = 1×10-2mol•L-1,则该温度下pH=3、
c(HSO3-)= 0.1mol•L-1的NaHSO3 溶液中c(H2SO3)=______.
高二化学实验题中等难度题查看答案及解析