-
实验室用粗锌与稀硫酸反应制取氢气,利用氢气还原氧化铜来测定铜的相对原子质量。实验装置如下:

(1)在启普发生器中纯锌与稀硫酸反应过于缓慢,可采取的加快速率的措施是①适当增大硫酸的浓度,②_______________________。
(2)用纯度不高的锌(粗锌)制取氢气,反应速率快,但制得的氢气因含H2S等还原性杂质而有难闻的气味,CuSO4洗气瓶中观察到的现象是_______________,是否可以将CuSO4溶液换成浓硫酸_________(答“是”或“否”) ;理由是__________________________。
(3)有同学发现粗锌与稀硫酸反应一段时间后,锌粒表面变黑,于是收集了少量该黑色固体,验证黑色固体含铁元素的简单化学方法_________________________________________。
(4)实验中得到的数据有:小瓷皿的质量m g,小瓷皿加样品的质量n g,反应后小瓷皿加固体的质量w g,已知氧的相对原子质量为16,则铜的相对原子质量是____________(用含m、n、w的代数式表示)。
(5)某次实验中测定结果明显偏大,可能的原因是________(选填编号)。
a.未充分冷却即停止通氢气 b.氧化铜样品中含有氯化铵杂质
c.反应后固体中有少量Cu2O d.氢气不干燥有少量水分
(6)由于启普发生器药品用量较多,利用下列仪器装配一套有启普发生器功能的简易装置,你选择____________(选填编号) (支撑仪器、橡皮塞、导气管略)。

(a) (b) (c) (d) (e) (f)
-
实验室用粗锌与稀硫酸反应制取氢气,利用氢气还原氧化铜来测定铜的相对原子质量。实验装置如下:
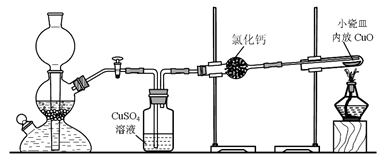
在启普发生器中纯锌与稀硫酸反应过于缓慢,可采取的加快速率的措施是①适当增大硫酸的浓度,②_______________________。
用纯度不高的锌(粗锌)制取氢气,反应速率快,但制得的氢气因含H2S等还原性杂质而有难闻的气味,CuSO4洗气瓶中观察到的现象是_______________,是否可以将CuSO4溶液换成浓硫酸_________(答“是”或“否”) ;理由是__________________________。
有同学发现粗锌与稀硫酸反应一段时间后,锌粒表面变黑,于是收集了少量该黑色固体,验证黑色固体含铁元素的简单化学方法_________________________________________。
实验中得到的数据有:小瓷皿的质量mg,小瓷皿加样品的质量n g,反应后小瓷皿加固体的质量w g,已知氧的相对原子质量为16,则铜的相对原子质量是____________(用含m、n、w的代数式表示)。
某次实验中测定结果明显偏大,可能的原因是________(选填编号)。
a.未充分冷却即停止通氢气 b.氧化铜样品中含有氯化铵杂质
c.反应后固体中有少量Cu2O d.氢气不干燥有少量水分
由于启普发生器药品用量较多,利用下列仪器装配一套有启普发生器功能的简易装置,你选择____________(选填编号) (支撑仪器、橡皮塞、导气管略)。

(a) (b) (c) (d) (e) (f)
-
实验室用粗锌与稀硫酸反应制取氢气,利用氢气还原氧化铜来测定铜的相对原子质量。实验装置如下:

(1)在启普发生器中纯锌与稀硫酸反应过于缓慢,可采取的加快速率的措施是①______,②______。
(2)用纯度不高的锌(粗锌)制取氢气,反应速率快,但制得的氢气因含H2S等还原性杂质而有难闻的气味,CuSO4洗气瓶中观察到的现象是有黑色沉淀生成,请写出该洗气瓶中发生复分解反应的化学方程式_______,是否可以将CuSO4溶液换成浓硫酸_________(答“是”或“否”);理由是_____________。请简述用CuSO4溶液配制检验醛基的新制氢氧化铜的方法________________________。
(3)装置中氯化钙的作用是__________________________。有同学发现粗锌与稀硫酸反应一段时间后,锌粒表面变黑,于是收集了少量该黑色固体,验证黑色固体含铁元素的化学方法___________。
(4)实验中得到的数据有:小瓷皿的质量mg,小瓷皿加样品的质量n g,反应后小瓷皿加固体的质量w g,已知氧的相对原子质量为16,则铜的相对原子质量是________________ (用含m、n、w的代数式表示)。
-
根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量么 (近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H20),由此计算
(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H20),由此计算 。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
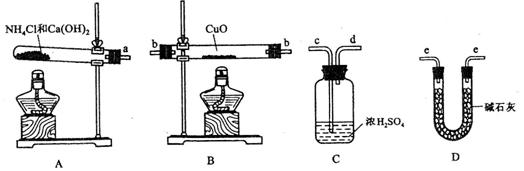
请回答下列问题:
(1)氨气还原炽热氧化铜的化学方程式为________________________________;
(2)从所提供的仪器及试剂中选择并组装本实验的一套合理、简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→______________________________;
(3)在本实验中,若测得m(CuO)= a g,m(H2O)= b g,则Ar(Cu)= _______________;
(4)在本实验中,使测定结果Ar(Cu)偏大的是_______________ (填序号);
1Cu0未完全起反应 ② CuO不干燥
3Cu0中混有不反应的杂质 ④ 碱石灰不干燥
⑤NH4C1与Ca(OH)2混合物不干燥
(5)在本实验中,还可通过测定_______________和_____________,或_______________和_______________达到实验目的。
-
根据氨气还原氧化铜的反应,可设计测定铜元素相对原子质量么 (近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H2O),由此计算
(近似值)的实验。先称量反应物氧化铜的质量m(CuO),反应完全后测定生成物水的质量m(H2O),由此计算 。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
。为此,提供的实验仪器及试剂如下(根据需要可重复选用,加入的NH4C1与Ca(OH)2的量足以产生使CuO完全还原的氨气):
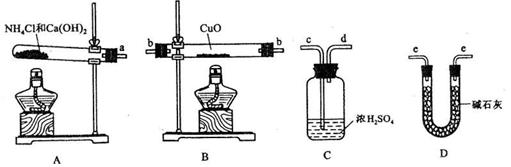
请回答下列问题:
(1)氨气还原炽热氧化铜的化学方程式为________________________________;
(2)从所提供的仪器及试剂中选择并组装本实验的一套合理.简单的装置,按气流方向的连接顺序为(用图中标注的导管口符号表示)a→__________________;
(3)在本实验中,若测得m(CuO)= a g,m(H2O)= b g,则Ar(Cu)= _______________;
(4)在本实验中,使测定结果Ar(Cu)偏大的是_______________ (填序号);
①CuO未完全起反应 ② CuO不干燥
③CuO中混有不反应的杂质 ④ 碱石灰不干燥
⑤NH4C1与Ca(OH)2混合物不干燥
(5)在本实验中,还可通过测定_______________和_______________,或__________和_________达到实验目的。
-
某化学小组采用下图装置模拟电解饱和食盐水制备氢气,通过氢气还原氧化铜测定Cu的相对原子质量,同时检验氯气的氧化性(图中夹持和加热仪器已经略去)。
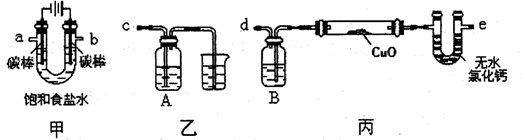
(1)写出装置甲中反应的离子方程式________。为完成上述实验,正确的连按方式为a连接________,b连接________(填字母)。
(2)①装置乙烧杯中液体的作用是________。A瓶内盛装的溶液最好是________(填字母)。
a.I-淀粉溶液 b.NaOH溶液
c.FeCl2与KSCN混合溶液 d.Na2SO3溶液
②加热装置丙中的氧化铜粉末之前,除了要检查该装置的气密性还需进行的必要操作是________。
(3)利用装置丙测定Cu的相对原子质量,现有两种方案:①测得反应前后洗气瓶B及其中液体质量差m1,②测得反应前后U形管及其中固体质量差m2。你认为合理的方案为________(填“①”或“②”)。若采用测得反应后硬质玻璃管中剩余固体的质量m3的方案,已知O的相对原子质量为16,实验中氧化铜样品质量为m,则测定Cu的相对原子质量的表达式为________,该方案在反应后硬质玻璃管冷却过程中没有一直通氢气,会导致测定Cu韵相对原子质量________(填“偏大”、“偏小”或“无影响”),理由是________。
-
实验室可用如图装置(启普发生器)制取氢气,欲使得到氢气的速率加快,下列措施可行的是

A. 将稀硫酸改为浓硫酸
B. 向稀硫酸中加入少量 固体
固体
C. 向稀硫酸中加入 溶液
溶液
D. 给装置中发生反应的部分加热
-
19.(12分)某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性。

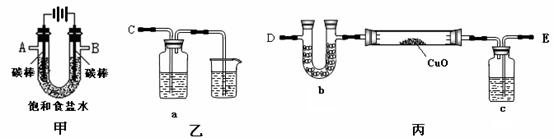
(1)为完成上述实验,正确的连接顺序为A连_______;B连_______(填写连接的字母)。
(2)对硬质玻璃管里的氧化铜粉末加热前,需要的操作为________。
(3)若检验氯气的氧化性,则乙装置的a瓶中溶液可以是 ,对应的现象为 。
(4)丙装置的c瓶中盛放的试剂为 ________,作用是_______________________。
(5)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案
精确测量硬质玻璃管的质量为a g, 放入CuO后,精确测量硬质玻璃管和CuO的总质量为b g , 实验完毕后
甲方案:通过精确测量硬质玻璃管和Cu粉的总质量为c g, 进而确定Cu的相对原子质量。
乙方案:通过精确测定生成水的质量d g,进而确定Cu的相对原子质量。
①请你分析并回答: 方案测得结果更准确。你认为不合理的方案的不足之处在________。
②按测得结果更准确的方案进行计算,Cu的相对原子质量________。
-
现有如下药品和装置:mg锌片、铁片、稀硫酸、水,设计一个实验,测定锌的相对原子质量(实验是在通常状况下进行的)。请完成下列实验:
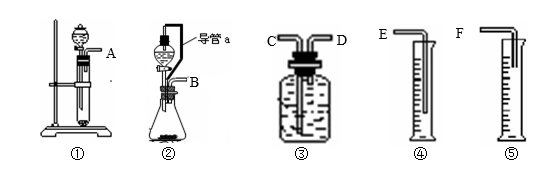
(1)写出该反应的化学方程式 。
(2)所选用装置的连接顺序为(填接口字母) 。
(3)取Wg纯铁片与稀硫酸反应测得生成气体V1mL,该步骤的目的是 。
(4)实验结束时,在读取测量实验中生成氢气的体积时,你认为合理的是 。
A.待实验装置冷却后再读数
B.上下移动量筒④,使其中液面与广口瓶中液面相平
C.上下移动量筒⑤,使其中液面与广口瓶中液面相平
D.视线与凹液面的最低点水平读取量筒中水的体积
(5)mg锌片与稀硫酸反应测得生成气体V2mL,则Zn的相对原子质量的数学表达式为 (用上述字母表示)。
(6)假设锌片中含不与酸反应的杂质,实验测得锌的相对原子质量可能比真实值(填“偏大”、“偏小”或“不变”,下同) ;实验结束时,仰视量筒读数,测得值 。
-
某化学小组拟采用如下装置(夹持和加热仪器已略去)来电解饱和食盐水,并用电解产生的H2还原CuO粉末来测定Cu的相对原子质量,同时检验氯气的氧化性。
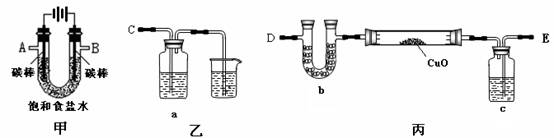
(1)为完成上述实验,正确的连接顺序为_______ 接A, B接_______(填写连接的字母)。
(2)对硬质玻璃管里的氧化铜粉末加热前,需要的操作为________。
(3)若检验氯气的氧化性,则乙装置的a瓶中溶液及对应的现象是________ ________ ________。
(4)为测定Cu的相对原子质量,设计了如下甲、乙两个实验方案
精确测量硬质玻璃管的质量为a g, 放入CuO后,精确测量硬质玻璃管和CuO的总质量为b g , 实验完毕后
甲方案:通过精确测量硬质玻璃管和Cu粉的总质量为c g, 进而确定Cu的相对原子质量。
乙方案:通过精确测定生成水的质量d g,进而确定Cu的相对原子质量。
请你分析并回答:你认为不合理的方案及其不足之处是________。
②按测得结果更准确的方案进行计算,Cu的相对原子质量________。











