-
将镁、铝的混合物0.1mol 溶于100mL 2mol/LH2SO4溶液中,然后在得到的溶液中滴加1mol/LNaOH 溶液,请回答:
(1)若在滴加NaOH溶液的过程中,欲使Mg2+、Al3+刚好完全沉淀,则加入NaOH溶液的体积是V(NaOH)=________mL。
(2)若在滴加NaOH溶液过程中,沉淀的质量随加入NaOH溶液的体积变化如下图所示。当V1=160mL时,求金属粉末中镁的物质的量和V2的体积?(要求写出解题过程)
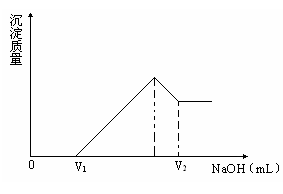
(3)若混合物仍为0.1mol ,其中Mg的物质的量分数为a,用100mL 2mol/L的H2SO4溶解此混合物后,再加入450mL 1mol/L的NaOH溶液,所得沉淀中无Al(OH)3,则满足此条件的a的取值范围为________。
-
0.1 mol的镁、铝混合物溶于100 mL 2 moI/LH2SO4溶液中,然后再滴加l mol/LNaOH溶液。请回答:
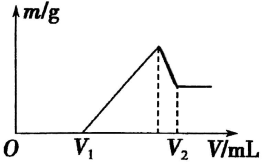
(l)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化如图所示。当V1=160mL时,则金属粉末中n(Mg)=_________ mol,V2=________mL。
(2)若在滴加NaOH溶液过程中,欲使Mg2+、Al3+刚好沉淀完全,则滴入NaOH溶液的体积V(NaOH)=________mL。
(3)若混合物仍为0.1 mol,其中Mg粉的物质的量分数为a,用100 mL2mol/L1硫酸溶解此混合物后,再加入450 mL l moI/LNaOH溶液,所得沉淀中无A1(OH)3。满足条件的a的取值范围是__________。
-
将0.1molMg 、Al混合物溶于100mL3mol/LHCl中,再滴加1mol/LNaOH 溶液,在滴加NaOH溶液的过程中,沉淀的质量m随NaOH溶液体积V变化如图所示:
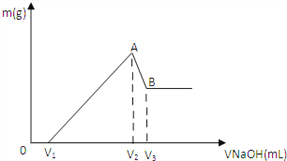
(1)写出A→B段反应的离子方程式_____________。
(2)A点沉淀的总物质的量n= _________________mol
(3)欲使Mg2+ 、Al3+刚好沉淀完全,则加入NaOH溶液的体积为多少___________mol
(4)若V1=60mL,则混合物中Mg的物质的量为多少___________mol V3= ___________mL
-
将0.1 mol的镁、铝混合物溶于100mL 2mol·L 的H2SO4溶液中,然后再滴加1mol·L
的H2SO4溶液中,然后再滴加1mol·L 的NaOH溶液。请回答:(不需要写出计算过程)
的NaOH溶液。请回答:(不需要写出计算过程)

(1)若在滴加NaOH溶液的过程中沉淀质量 随加入NaOH溶液的体积V变化如图所示。当
随加入NaOH溶液的体积V变化如图所示。当 mL时,则金属粉末中
mL时,则金属粉末中 (Mg)=mol,
(Mg)=mol, ________mL。
________mL。
(2)①要配制100 mL 2mol·L 的H2SO4溶液,需要的仪器除量筒、烧杯外,还有________。
的H2SO4溶液,需要的仪器除量筒、烧杯外,还有________。
②下列操作会使所配的溶液浓度偏小的是( )(填代号)
A.用量筒量取一定体积的98%的浓H2SO4,稀释后未经冷却即转入容量瓶内
B.稀释硫酸所用的小烧杯未洗涤
C.定容时俯视液面
D.用蒸馏水洗涤后的容量瓶未干燥
E.定容摇匀后,倒入干燥的试剂瓶中储存时,有少量溶液浅出瓶外
-
将由等物质量的铝、镁组成的混合物分成四等份,分别加入足量的①3mol/LNaOH溶液,②2mol/L稀硝酸(还原产物仅有NO),③18mol/LH2SO4,④1mol/LH2SO4产生气体物质的量由小到大的顺序为( )
A.①②③④ B.②③①④ C.④②①③ D.③①②④
-
用0.1mol/LNaOH溶液滴定40mL0.1mol/LH2SO3溶液,所得滴定曲线如下图所示(忽略混合时溶液体积的变化)。下列叙述不正确的是
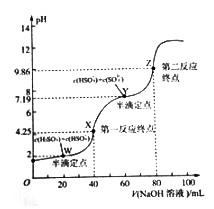
A. H2SO3的Ka1=1×10-2
B. 0.05mol/L NaHSO3溶液的PH=4.25
C. 图中Y点对应的溶液中,3c(SO32-)=c(Na+)+c(H+)-c(OH-)
D. 图中Z点对应的溶液中:c(Na+)> c(SO32-)> c(HSO32-)> c(OH-)
-
室温时,向100mL0.1mol/LNH4HSO4溶液中逐滴滴加0.1mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示(假设溶液的体积有加和性)。下列分析正确的是
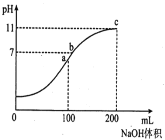
A.ab段和bc段发生的离子反应一定不同
B.水的电离程度最大的是c点
C.b点溶液中各离子浓度由大到小的排列顺序是:C(Na+)>C(NH4+)>C(SO42-)>C(H+)=C(OH-)
D.NH4+的水解平衡常数Kh的数量级为10-10
-
标准状况下2.24LH2和Cl2组成的混合气体,经光照后缓缓通入100ml 1mol/LNaOH溶液中充分反应,测得最终溶液中NaClO的浓度为0.1mol/L(假设溶液体积不变,且不考虑水解),则原混合气体中Cl2的体积分数为( )
A.55% B.60% C.65% D.70%
-
下列混合溶液中,各离子浓度的大小顺序不正确的是:
A、10mL0.1mol/L氨水与10mL0.1mol/L盐酸混合:
B、10mL1mol/LNH4Cl溶液与5mL2mol/LNaOH溶液混合:
C、 溶液与
溶液与 溶液混合:
溶液混合:

D、将pH=3的盐酸与pH=11的氨水等体积混合后:
c(NH4+)>c(Cl—)>c(OH-)>c(H+)
-
(15分)
已知G是合成某高分子化合物的原料,只含C、H、O三种元素,5.9g物质G能与1mol/LNaOH的溶液100mL恰好完全反应,0.1mol物质G与足量金属钠反应在标准状况下生成2.24L氢气,分子结构中含有一个甲基,A的分子式为C8H13O2Br,有机物A、B、C、D、E、F、G之间的相互转化关系如图所示:
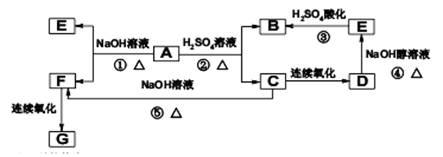
⑴写出C的结构简式:________ .
⑵A中官能团名称是:________ .
⑶B的同分异构体中属于酯的有多种,任写其中三种属于酯类的结构简式 :
________ ,________ ,________ .
⑷写出D→E化学反应方程式: .
⑸写出反应①化学反应方程式:________
⑹写出由F和G 在一定条件下合成高分子化合物的化学反应方程式:
________ .






