-
利用海水可以提取溴和镁,提取过程如下。

(1)提取溴的过程中,经过两次Br-→Br2转化的目的是________,吸收塔中发生反应的离子方程式是__________。用平衡移动原理解释通空气的主要目的是_______。
(2)从MgCl2溶液中得到MgCl2·6H2O晶体的主要操作是________________、过滤、洗涤、干燥。
(3)依据上述流程,若将10 m3海水中的溴元素转化为工业溴,至少需要标准状况下Cl2的体积为________L(忽略Cl2的溶解)。
-
利用海水可以提取溴和镁,提取过程如下:

(1)提取溴的过程中,经过2次Br-→Br2转化的目的是________,吸收塔中发生反应的离子方程式是________________。
(2)据上述流程,将10m3海水中溴元素(海水中Br-离子含量为64mg/L)转化为工业溴,整个流程中至少需要标准状况下Cl2的体枳为______L(忽略Cl2溶解)。
(3)从理论上考虑,下列物质也能吸收Br2的是_____。
A.H2O B.FeCl2 C.Na2SO3
(4)由无水氯化镁得到镁的化学方程式是_______。
(5)有同学认为:可以加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁,以简化实验步骤,体现实验的简约性原则,你是否同意该同学的观点,理由为_______________。
-
利用海水可以提取溴和镁,提取过程如下:

(1)提取溴的过程中,经过2次 转化的目的是__________,吸收塔中发生反应的离子方程式是
转化的目的是__________,吸收塔中发生反应的离子方程式是 ,蒸馏塔中发生反应的离子方程式是____________。
,蒸馏塔中发生反应的离子方程式是____________。
(2)从 溶液中得到
溶液中得到 晶体的主要操作是__________、_________、过滤、洗涤、干燥。由无水氯化镁得到镁的化学方程式是__________。
晶体的主要操作是__________、_________、过滤、洗涤、干燥。由无水氯化镁得到镁的化学方程式是__________。
(3)据上述流程,将 海水中溴元素(海水中
海水中溴元素(海水中 离子含量为
离子含量为 )转化为工业溴,整个流程中至少需要标准状况下
)转化为工业溴,整个流程中至少需要标准状况下 的体积为_________L(忽略
的体积为_________L(忽略 溶解)。
溶解)。
-
利用海水可以提取溴和镁,提取过程如下:

(1)提取溴的过程中,经过2次 转化的目的是__________,吸收塔中发生反应的离子方程式是
转化的目的是__________,吸收塔中发生反应的离子方程式是 ,蒸馏塔中发生反应的离子方程式是____________。
,蒸馏塔中发生反应的离子方程式是____________。
(2)从 溶液中得到
溶液中得到 晶体的主要操作是__________、_________、过滤、洗涤、干燥。由无水氯化镁得到镁的化学方程式是__________。
晶体的主要操作是__________、_________、过滤、洗涤、干燥。由无水氯化镁得到镁的化学方程式是__________。
(3)据上述流程,将 海水中溴元素(海水中
海水中溴元素(海水中 离子含量为
离子含量为 )转化为工业溴,整个流程中至少需要标准状况下
)转化为工业溴,整个流程中至少需要标准状况下 的体积为_________L(忽略
的体积为_________L(忽略 溶解)。
溶解)。
-
海水是巨大的资源宝库,可以进行综合利用.从海水中提取食盐和溴的过程如下:
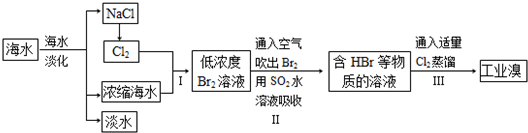
(1)请写出一种海水淡化的方法:______.
(2)步骤Ⅰ获得Br2的离子方程式为______;
(3)步骤Ⅱ用SO2水溶液吸收Br2,使溴蒸气转化为氢溴酸以达到富集的目的.其反应的化学方程式为Br2+SO2+2H2O=H2SO4+2HBr,在该反应中,氧化剂是______(填化学式).若反应中生成2molHBr,则消耗______molSO2,若完全吸收后的酸溶液体积为500mL,则溶液中氢离子浓度为______mol/L.
(4)根据上述反应判断SO2、Cl2、Br2三种物质氧化性由强到弱的顺序是______.
-
海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:

(1)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为 ___________ .
(2)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达 ,有关反应的离子方程式为_________________;
,有关反应的离子方程式为_________________;
(3)从理论上考虑,下列物质也能吸收Br2的是____________.
A. H2O B. Na2CO3 C. Na2SO3 D. FeCl3
(4)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料, 的沸点为
的沸点为 ,微溶于水,有毒性和强腐蚀性。步骤Ⅲ的操作中对盛有工业溴的蒸馏烧瓶采取的加热方式是__________ ,溴蒸汽冷凝后得到液溴和溴水的混合物,可利用它们的相对密度相差较大的特点进行分离,所用的分离仪器名称是__________ .
,微溶于水,有毒性和强腐蚀性。步骤Ⅲ的操作中对盛有工业溴的蒸馏烧瓶采取的加热方式是__________ ,溴蒸汽冷凝后得到液溴和溴水的混合物,可利用它们的相对密度相差较大的特点进行分离,所用的分离仪器名称是__________ .
-
海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
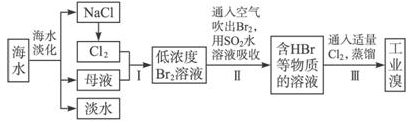
(1)请列举海水淡化的两种方法: 、 。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为 。
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为 。
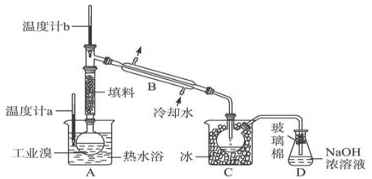
(4)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃.微溶于水,有毒性和强腐蚀性.他们参观生产过程后,了解到如下装置简图:请你参与分析讨论:
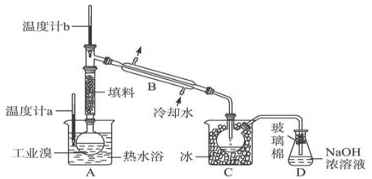
①图中仪器B的名称: 。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是 。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件: 。
④C中液体产生颜色为 。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是 。
-
海水是巨大的资源宝库,从海水中提取食盐和溴的过程如下:
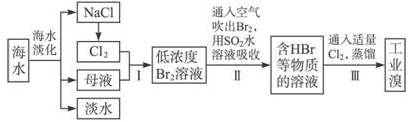
(1)请列举海水淡化的两种方法: 、 。
(2)步骤Ⅰ中已获得Br2,步骤Ⅱ中又将Br2还原为Br-,其目的为 。
(3)步骤Ⅱ用SO2水溶液吸收Br2,吸收率可达95%,有关反应的离子方程式为 。
(4)某化学研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料,Br2的沸点为59℃.微溶于水,有毒性和强腐蚀性.他们参观生产过程后,了解到如下装置简图:请你参与分析讨论:
①图中仪器B的名称: 。
②整套实验装置中仪器连接均不能用橡胶塞和橡胶管,其原因是 。
③实验装置气密性良好,要达到提纯溴的目的,操作中如何控制关键条件: 。
④C中液体产生颜色为 。为除去该产物中仍残留的少量Cl2,可向其中加入NaBr溶液,充分反应后,再进行的分离操作是 。
-
海洋中有大量的宝贵资源。下面是工业上利用海水提取溴和镁的流程图。
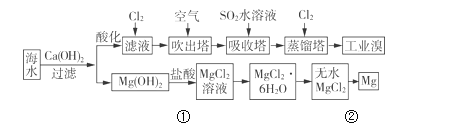
(1)提取溴的过程中,在第2次Br-→Br2 的转化中每产生1mol溴消耗标况下氯气______L。
(2)在吸收塔中,从理论上考虑下列物质也能吸收Br2的是________。
A.KBr B.Na2SO4 C.FeCl3 D.H2S
(3)在吸收塔中发生反应的离子方程式是_____________________。
(4)写出氢氧化镁得到镁的流程中涉及到的反应方程式①_____________ ②____________。
-
海水是可以综合利用的。从海水中提取食盐和溴的过程如下:
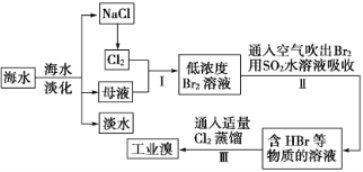
(1)请写出一种海水淡化的方法:_______________。
(2)步骤Ⅰ从母液中获取Br2的离子方程式为:_______________________。
(3)步骤Ⅱ用SO2水溶液吸收Br2,使溴蒸气转化为氢溴酸以达到富集的目的。其反应的化学方程式为:__________________________。











