-
(14分)氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
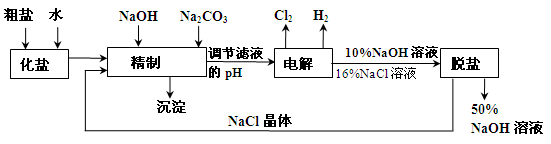
依据上图完成下列问题:
在电解过程中,阴极上生成气体的电子式为 。
(2)精制过程中除去阳离子中的Ca2+、Mg2+等杂质,除去Mg2+的离子方程式为 。
(3)精制过程要除去SO42-,可选择下列溶液中的 (填字母序号)
a. Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)在实际生产中也可以用BaCO3除去SO42-(已知溶解度BaSO4<BaCO3),试用平衡移动原理加以解释: 。
(5) 脱盐工作中,利用NaOH和NaCl在溶解度上的差异,通过蒸发、冷却、 、 (填操作名称)而制得50%的NaOH溶液。
(6)写出电解饱和食盐水的离子方程式:
-
氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:

依据上图完成下列问题:
在电解过程中,阴极上生成气体的电子式为________。
(2)精制过程中除去阳离子中的Ca2+、Mg2+等杂质,除去Mg2+的离子方程式为________。
(3)精制过程要除去 ,可选择下列溶液中的________(填字母序号),并将加入的顺序以箭头符号(↓)的形式画在图上(精制过程中加入试剂从左到右的顺序为先后顺序)。
,可选择下列溶液中的________(填字母序号),并将加入的顺序以箭头符号(↓)的形式画在图上(精制过程中加入试剂从左到右的顺序为先后顺序)。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)在实际生产中也可以用BaCO3除去 (已知溶解度BaSO4<BaCO3),试用平衡移动原理加以解释:________。
(已知溶解度BaSO4<BaCO3),试用平衡移动原理加以解释:________。
(5) 脱盐工作中,利用NaOH和NaCl在溶解度上的差异,通过蒸发、冷却、________、(填操作名称)而制得50%的NaOH溶液。
-
(14分)氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下:
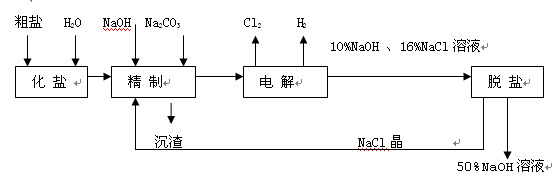
依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生反应的化学方程式为________,与电源负极相连的电极附近,溶液pH值________(选填:不变、升高或下降)
(2)工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为________ ,________
(3)为有效除去Ca2+、Mg2+、SO ,加入试剂的合理顺序为________(选填a,b,c多选扣分)
,加入试剂的合理顺序为________(选填a,b,c多选扣分)
a 先加NaOH,后加Na2CO3,再加钡试剂
b 先加NaOH,后加钡试剂,再加Na2CO3
c 先加钡试剂,后加NaOH,再加Na2CO3
(4)脱盐工序中利用NaoH和NaCl在溶解度上的差异,通过________、冷却、________(填写操作名称)除去NaCl
(5)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为
-
氯碱厂电解饱和食盐水溶液制取NaOH的工艺流程示意图如下:

依据上图,完成下列问题:
(1)写出电解饱和食盐水的离子方程式:________.
(2)粗盐常含Ca2+、Mg2+、SO42-等杂离子,精制过程中要将它们以沉淀的形式除去,则加入试剂的合理顺序为________(填编号).
A.先加入NaOH,后加入Na2CO3,再加入BaCl2溶液
B.先加入NaOH,后加入BaCl2溶液,再加入Na2CO3
C.先加入BaCl2溶液,后加入NaOH,再加入Na2CO3
(3)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________(填写操作名称)、冷却结晶、________(填写操作名称),除去NaCl.
(4)由图示可知在电解制碱过程中________可以循环使用,以提高反应物利用率;在制碱的同时,还产生H2和Cl2,工业上常常利用它们生产________.
(5)如图所示,目前电解法制烧碱通常采用离子交换膜法,阳离子交换膜不允许阴离子通过,阴离子交换膜不允许阳离子通过.则以下叙述正确的是________(填编号).
A.NaOH、H2均在Ⅰ区产生
B.图中a为阴离子交换膜,b为阳离子交换膜
C.Ⅲ区炭棒上的电极反应式为 2Cl--2e→Cl2↑
D.取少量Ⅲ区中的溶液,滴加酚酞,溶液变红色
(6)在实际生产中,经过脱盐后得到含溶质质量分数约为50%的NaOH溶液(密度为1.92g/cm3),则该烧碱溶液的物质的量浓度为________.

-
(8分)(1998年上海)氯碱厂电解饱和食盐水制取NaOH的工艺流程示意图如下

依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生反应的化学方程式为________,与电源负极相连的电极附近,溶液pH________(选填“不变”“升高”或“下降”)。
(2)工业食盐含Ca2+、Mg2+等杂质。精制过程发生反应的离子方程式为
________、________。
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以
是________ (选填a,b,c多选扣分)。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)为有效除去Ca2+、Mg2+、SO42—,加入试剂的合理顺序为________(选填a、b、c多选扣分)
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________、冷却、________(填写操作名称)除去NaCl
(6)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2与NaOH反应;采用无隔膜电解冷的食盐水时,Cl2与NaOH充分接触,产物仅是NaClO和H2,相应的化学方程式为________。
-
(17分) 氯碱厂电解饱和食盐水制取 的工艺流程示意图如下:
的工艺流程示意图如下:

依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极上所发生反应的化学方程式为_________________________________;与电源负极相连的电极附近,溶液 值___________。(选填:不变、升高或下降)
值___________。(选填:不变、升高或下降)
(2)工业食盐含 等杂质,精制过程发生反应的离子方程式为____________________________________________;
等杂质,精制过程发生反应的离子方程式为____________________________________________;
(3)如果粗盐中 含量较高,必须添加钡试剂除去
含量较高,必须添加钡试剂除去 ,该钡试剂可以是________(选填a、b、c多选倒扣分)
,该钡试剂可以是________(选填a、b、c多选倒扣分)
a.  b.
b.  c.
c. 
(4)为有效除去 ,加入试剂的合理顺序为_____________(选填a、b、c多选倒扣分)
,加入试剂的合理顺序为_____________(选填a、b、c多选倒扣分)
a. 先加 ,后加
,后加 ,再加钡试剂
,再加钡试剂
b. 先加 ,后加钡试剂,再加
,后加钡试剂,再加
c. 先加钡试剂,后加 ,再加
,再加
(5)脱盐工序中利用 和
和 在溶解度上的差异,通过____________、冷却、______________(填写操作名称)除去
在溶解度上的差异,通过____________、冷却、______________(填写操作名称)除去 。
。
(6)在隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止 与
与 反应;采用无隔膜电解冷的食盐水时,
反应;采用无隔膜电解冷的食盐水时, 与
与 充分接触,产物仅是
充分接触,产物仅是 和
和 ,相应的化学方程式为_____________________。
,相应的化学方程式为_____________________。
-
(16分)“向海洋进军”,已成为世界许多国家发展的战略口号,海水中通常含有较多的Ca2+、Mg2+、 等杂质离子,以海盐为原料的氯碱厂电解饱和食盐水制取NaOH的工艺流程如下:
等杂质离子,以海盐为原料的氯碱厂电解饱和食盐水制取NaOH的工艺流程如下:

依据上图,完成下列填空:
(1)在电解过程中,与电源正极相连的电极的电极反应式为 ;
(2)电解过程的总反应的化学方程式_________________________________________。
(3)电解槽阳极产物可用于_____________________________(至少写出两种用途)。
(4)工业食盐含Ca2+、Mg2+等杂质,精制过程中除去这2种离子所发生反应的离子方程式为: 。
(5)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(6)为了有效除去Ca2+、Mg2+、SO42-加入试剂的合理顺序为
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(7)已知NaOH、NaCl在水中的溶解度数据如下表:
| 温度/℃ | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 | 100 |
| NaOH /g | 109 | 118 | 129 | 146 | 177 | 300 | 313 | 318 | 337 |
| NaCl/ g | 36 | 36.3 | 36.6 | 37 | 37.3 | 37.8 | 38.4 | 39 | 39.8 |
根据上述数据,脱盐工序中利用通过 、 (填操作名称)除去NaCl。
-
氯碱厂电解饱和食盐水制取NaOH溶液的工艺流程如示意图所示,完成下列填空:

(1)在电解过程中,与电源负极相连的电极上的电极反应式为________________,若检验与电源正极相连的电极上的气体产物,实验室中通常选用的化学试剂是________________________________。
(2)工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为________________。
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是________。(选填a、b、c)。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)为了有效地除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为_______(选填a、b、c)。
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过________、冷却________、(填写操作名称)除去NaCl。
-
(18分)氯碱厂电解饱和食盐水制取NaOH溶液的工艺流程如示意图所示,完成下列填空:

(1)在电解过程中,与电源负极相连的电极上的电极反应式为________________,若检验与电源正极相连的电极上的气体产物,实验室中通常选用的化学试剂是________。
(2)工业食盐含Ca2+、Mg2+等杂质,精制过程发生反应的离子方程式为___________________
(3)如果粗盐中SO42-含量较高,必须添加钡试剂除去SO42-,该钡试剂可以是_____ (选填a、b、c)。
a.Ba(OH)2 b.Ba(NO3)2 c.BaCl2
(4)为了有效地除去Ca2+、Mg2+、SO42-,加入试剂的合理顺序为________(选填a、b、c)。
a.先加NaOH,后加Na2CO3,再加钡试剂
b.先加NaOH,后加钡试剂,再加Na2CO3
c.先加钡试剂,后加NaOH,再加Na2CO3
(5)脱盐工序中利用NaOH和NaCl在溶解度上的差异,通过蒸发浓缩、冷却、________(填写操作名称)除去NaCl。
(6)在电解过程中,发生总反应的化学方程式为__________________
(7)用隔膜法电解食盐水时,电解槽分隔为阳极区和阴极区,防止Cl2和NaOH反应,请写出Cl2和NaOH溶液反应的化学方程式__________。
-
氯碱厂电解饱和食盐水制取NaOH的工艺流程如下:
(1)精制过程中反应的离子方程式为______.
(2)电解过程的总反应方程式为______ 2NaOH+H2↑+Cl2↑










