-
氟及其化合物在生产生活中被广泛使用,造福人类。
(1)氟在元素周期表中的位置是___________。
(2)氢氟酸具有刻蚀玻璃的特性,写出该反应的化学方程式____________。已知25℃时,氢氟酸的电离平衡常数Ka=3.6×10-4,若将0.01 mol·L-1的HF溶液与pH=12的NaOH溶液等体积混合,则溶液中离子浓度由大到小的顺序为_____。
(3)次氟酸(HOF)由科学家在1971年首次制得,次氟酸的电子式为_______。
(4)四氟肼(N2F4)用作高能燃料的氧化剂,1 mol N2F4分子中含有的共价键数目是________NA。N2F4气体可用Fe3+氧化二氟胺(HNF2)制得,写出该反应的离子方程式______________。
(5)六氟化铀(UF6)是铀的稳定气态化合物,用作核燃料,由U3O8制取UF6的三步反应原理如下:
①U3O8+H2 →UO2+H2O (未配平) ②UO2+4HF=UF4+2H2O ③UF4+ F2 = UF6
则下列说法正确的是 _____________。
A.反应①②③都是氧化还原反应
B.反应③中U元素被氧化
C.反应①中氧化剂和还原剂的物质的量之比为2:1
(6)六氟磷酸锂(LiPF6)是锂离子电池广泛使用的电解质。LiPF6与极少量水反应可生成POF3等三种含氟化合物,写出该反应的化学方程式:________。
-
氟及其化合物在生产生活中被广泛使用,造福人类。
(1)氟在元素周期表中的位置是___________。
(2)氢氟酸具有刻蚀玻璃的特性,写出该反应的化学方程式____________。已知25℃时,氢氟酸的电离平衡常数Ka=3.6×10-4,若将0.01 mol·L-1的HF溶液与pH=12的NaOH溶液等体积混合,则溶液中离子浓度由大到小的顺序为_____。
(3)次氟酸(HOF)由科学家在1971年首次制得,次氟酸的电子式为_______。
(4)四氟肼(N2F4)用作高能燃料的氧化剂,1 mol N2F4分子中含有的共价键数目是________NA。N2F4气体可用Fe3+氧化二氟胺(HNF2)制得,写出该反应的离子方程式______________。
(5)六氟化铀(UF6)是铀的稳定气态化合物,用作核燃料,由U3O8制取UF6的三步反应原理如下:
①U3O8+H2 →UO2+H2O (未配平) ②UO2+4HF=UF4+2H2O ③UF4+ F2 = UF6
则下列说法正确的是 _____________。
A.反应①②③都是氧化还原反应
B.反应③中U元素被氧化
C.反应①中氧化剂和还原剂的物质的量之比为2:1
(6)六氟磷酸锂(LiPF6)是锂离子电池广泛使用的电解质。LiPF6与极少量水反应可生成POF3等三种含氟化合物,写出该反应的化学方程式:________。
-
氟及其化合物在生产生活中被广泛使用,造福人类。
(1)LiPF6是锂离子电池中广泛应用的电解质。某工厂用LiF、PCl5为原料,低温反应制备LiPF6,其流程如下

已知:HCl的沸点是-85.0 ℃,HF的沸点是19.5 ℃。
①反应设备不能用玻璃材质的原因是 (用化学方程式表示)。无水HF有腐蚀性和毒性,工厂安全手册提示:如果不小心将HF沾到皮肤上,可立即用2%的 溶液冲洗。
②该流程需在无水条件下进行,第③步反应中PF5极易水解,其产物为两种酸,写出PF5水解的化学方程式: 。
③第④步分离采用的方法是 ;第⑤步分离尾气中HF、HCl采用的方法是 。
(2)工业上制备氟气通常采用电解氧化法,如图是电解熔融的氟氢化钾(KHF2)的实验装置:


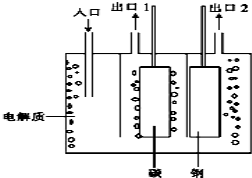
① 已知阴极的电极反应式为2HF2-+2e-═H2+4F-,则电解的总反应为
② 出口1处的物质是 (填化学式)。
(3)牙齿表面有一层釉质,其组成为羟基磷灰石Ca5(PO4)3OH(Ksp=6.8×10-21),容易受到酸的侵蚀,研究表明氟磷灰石Ca5(PO4)3F(Ksp=1.0×10-37)更能抵抗酸的腐蚀。请用平衡移动原理解释为什么人们常使用含氟牙膏防治蛀牙___________________。
-
(14分)铝是地壳中含量最高的金属元素,其单质、合金及其化合物在生产生活中的应用日趋广泛,铝土矿是生产铝及其化合物的重要原料。
(1)铝元素在元素周期表中的位置是 。
(2)铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。
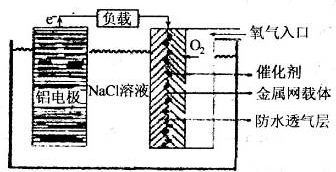
①该电池的总反应化学方程式为 ;
②电池中NaCl的作用是 。
③以铝一空气电池为电源电解KI溶液制取KIO3(石墨为电极材料)时,电解过程中阳极的电极反应式为 。
④某铝一空气电池的效率为50%,若用其作电源电解500mL的饱和NaCl溶液,电解结束后,所得溶液(假设溶液电解前后体积不变)中NaOH的浓度为0.3 mol·L-1,则该过程中消耗铝的质量为 。
(3)氯化铝广泛用于有机合成和石油工业的催化剂,聚氯化铝也被用于城市污水处理。
①氯化铝在加热条件下易升华,气态氯化铝的化学式为Al2Cl6,每种元素的原子最外层均达到8电子稳定结构,则其结构式为 。
②将铝土矿粉与碳粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式 。
-
(14分)铝是地壳中含量最高的金属元素,其单质、合金及其化合物在生产生活中的应用日趋广泛,铝土矿是生产铝及其化合物的重要原料。
(1)铝元素在元素周期表中的位置是 。
(2)铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。

①该电池的总反应化学方程式为 ;
②电池中NaCl的作用是 。
③以铝一空气电池为电源电解KI溶液制取KIO3(石墨为电极材料)时,电解过程中阳极的电极反应式为 。
④某铝一空气电池的效率为50%,若用其作电源电解500mL的饱和NaCl溶液,电解结束后,所得溶液(假设溶液电解前后体积不变)中NaOH的浓度为0.3 mol·L-1,则该过程中消耗铝的质量为
(3)氯化铝广泛用于有机合成和石油工业的催化剂,聚氯化铝也被用于城市污水处理。
①氯化铝在加热条件下易升华,气态氯化铝的化学式为Al2Cl6,每种元素的原子最外层均达到8电子稳定结构,则其结构式为 。
②将铝土矿粉与碳粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式 。
-
(14分)铝是地壳中含量最高的金属元素,其单质、合金及其化合物在生产生活中的应用日趋广泛,铝土矿是生产铝及其化合物的重要原料。
(1)铝元素在元素周期表中的位置是____ 。
(2)铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。
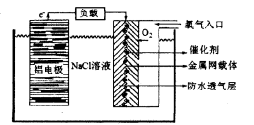
①该电池的总反应化学方程式为____ ;
②电池中NaCI的作用是 。
③以铝一空气电池为电源电解KI溶液制取KIO3(石墨为电极材料)时,电解过程中阳极的电极反应式为 。
④某铝一空气电池的效率为50%,若用其作电源电解500mL的饱和NaCI溶液,电解结束后,所得溶液(假设溶液电解前后体积不变)中NaOH的浓度为0.3 mol·L-1,则该过程中消耗铝的质量为 。(3)氯化铝广泛用于有机合成和石油工业的催化剂,聚氯化铝也被用于城市污水处理。
①氯化铝在加热条件下易升华,气态氯化铝的化学式为Al2Cl6,每种元素的原子最外层均达到8电子稳定结构,则其结构式为 。
②将铝土矿粉与碳粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式 。
-
(15分)在生产生活中,卤族元素(F、Cl、Br、I)的单质及化合物用途广泛。
(1)溴元素在周期表中的位置为 。
(2)下列说法中正确的是 。
A.CCl4和XeF2分子中各原子最外层均满足8e-结构
B.Cl2O5和Cl2O7都是酸性氧化物
C.氟非金属性强于氯,故氢氟酸的酸性强于盐酸
D.F-、Cl-、Br-、I-等离子的还原性逐渐增强
(3)已知:HCl的沸点是﹣85.0℃,HF的沸点是19.5℃。HF的电子式为 ;从HF、HCl混合气体中分离出HF的方法是 。
(4)向NaClO浓溶液中加入Al2(SO4)3浓溶液,迅速生成大量白色沉淀,同时有无色气体产生。生成白色沉淀的离子方程式为 。无色气体的成分为 。
(5)潮湿的氯气与碳酸钠粉末反应可用于制取氯的最低价氧化物,反应还同时生成两种盐,该反应的化学方程式为 。
(6)已知:还原性HSO3¯>I¯,氧化性IO3¯> I2,在下图中画出向含3 mol NaHSO3的溶液中逐滴加入KIO3溶液的过程中,析出I2的物质的量与KIO3的物质的量之间关系的曲线。
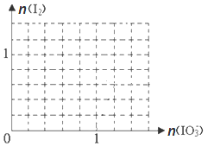
-
铝、铁、铜的单质、合金及其化合物在生产生活中的应用日趋广泛.
(1)铁元素在元素周期表中的位置是______.
(2)铝电池性能优越,铝一空气电池以其环保、安全而受到越来越多的关注,其原理如图所示.
①该电池的总反应化学方程式为______;
②电池中NaCl的作用是______.
(3)用铝电池电解CuSO4溶液(电极均为铂电极),通电一段时间后,一极上析出红色固体,另一极的电极反应式为______,此时向溶液中加入8g CuO固体后可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为______L.
(4)氯化铝广泛用于有机合成和石油工业的催化剂.将铝土矿粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式______ 2AlCl3+3CO.

-
铝、铁、铜的单质、合金及其化合物在生产生活中的应用日趋广泛。
(1)铁元素在元素周期表中的位置是__________。
(2)铝电池性能优越,铝-空气电池以其环保、安全而受到越来越多的关注,其原理如图所示。

①该电池的总反应化学方程式为____________________________________________。
②电池中NaCl的作用是___________________________________________________。
(3)用铝电池电解CuSO4溶液(电极均为铂电极),通电一段时间后,一极上析出红色固体,另一极的电极反应式为___________________,此时向溶液中加入SgCuO固体后可使溶液恢复到电解前的浓度,则电解过程中收集到的气体在标准状况下体积为_______L。
(4)氯化铝广泛用于有机合成和石油工业的催化剂。将铝土矿粉混合后加热并通入氯气,可得到氯化铝,同时生成CO,写出该反应的化学方程式______________。
(5)三氧化二铁和氧化亚铜(Cu2O)都是红色粉末,常用作燃料。已知氧化亚铜溶于稀硫酸生成Cu和CuSO4。取少量Fe2O3和Cu2O组成的混合物放入足量稀硫酸中。
①此过程中发生的反应有(用离子方程式表示):Fe2O3+6H+=Fe3++3H2O;____________________;____________________。
②设计实验证明反应后所得溶液中铁元素可能存在形式_____________________。
③若实验中观察到溶液变为蓝色且有固体剩余,则n(Cu2O) __________n(Fe2O3)。(填“>”、“<”或“=”)。
-
Ⅰ(6分)氯及其化合物在生活中应用广泛。
(1)指出氯元素在周期表中的位置
(2)将铁片插入盛有少量新制氯水试管中,无气泡产生,用长滴管吸取KSCN溶液滴入铁片附近,溶液变红色,然后红色消失。显红色的离子方程式为__________。
(3)向新制氯水加入碳酸钙固体,可以收集2种气体(水蒸汽除外),写出分子式__________。
Ⅱ(12分)某科研小组为开发新型净水剂,合成中间体物质A,A可以看成由氯化铝和一种盐按物质的量之比1:2组成,有下列变化:
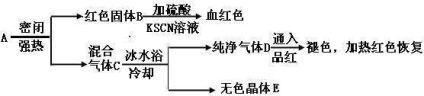
实验发现,加热4.375克A,可得到1.6克B、2.135克E和0.01mol的D。
(1)写出D的化学式__________。
(2)写出A强热发生的化学方程式__________。
(3)E晶体中某种物质在一定条件能和KI固体反应,写出该方程式__________。
将E晶体配成溶液,逐滴加入稀NaOH溶液,现象__________。
(4)若在高温下长时间煅烧A,在气体D中还能检验出另一种气体,分子式是__________。








