-
室温下,分别取10 mL pH均为2的盐酸、醋酸溶液分别与10mL 0.01 mol• L-1 NaHCO3溶液混合,实验测得产生CO2气体的体积(V)随时间(t)的变化如图所示。下列说法不正确的是
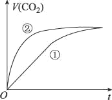
A.①表示的是盐酸的反应曲线
B.混合后的溶液中:c(CH3COO-)>c(C1-)
C.上述混合前三种溶液中水的电离程度:NaHCO3溶液>醋酸溶液=盐酸
D.醋酸和NaHCO3溶液混合后,所得的溶液中:c(CH3COO-)+ c(CH3COOH) = 0.005 mol• L-1
-
室温下,用0.100mol/L NaOH 溶液分别滴定20.00mL 0.100mol/L的盐酸和醋酸,滴定曲线如图所示.下列说法正确的是
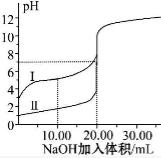
A.Ⅰ、Ⅱ分别表示盐酸和醋酸的滴定曲线
B.V(NaOH)=10.00 mL 时  >1
>1
C.pH=7时,两种酸所用NaOH溶液的体积相等
D.V(NaOH)=20.00 mL 时,c(Cl-)<c(CH3COO-)
-
下列事实能说明醋酸属于弱电解质的是
①中和10mL1mol/LCH3COOH溶液需要10mL1mol/LNaOH溶液
②相同条件下,完全相同的两块锌粒分别跟盐酸和醋酸反应,前者的速率快
③0.01mol/L醋酸溶液的pH大于2
④0.1mol/LCH3COONa溶液显碱性
A.①②③ B.②③④ C. ②③ D.①④
-
室温时,下列混合溶液的pH一定大于7的是
A. pH=3的盐酸和pH=11的氨水等体积混合
B. 0.01 mol•L-1的盐酸和pH=12的氢氧化钡溶液等体积混合
C. pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合
D. 0.01 mol•L-1的硫酸和0.01 mol•L-1的氨水等体积混合
-
下列事实能说明醋酸属于弱电解质的是( )
①中和10mL 1mol/LCH3COOH溶液需要10mL 1mol/LNaOH溶液
②物质的量浓度相同时,锌粒跟盐酸反应的速率比跟醋酸反应的速率快
③0.01mol/L醋酸溶液的pH大于2
④0.1mol/L CH3COONa溶液显碱性
A.①②③ B.②③④ C.①③④ D.①④
-
醋酸的下列性质中,可以证明它是弱电解质的是( )
 大小相同的铁片与pH相同盐酸和醋酸反应,刚开始时醋酸和盐酸产生H2速率相同;②室温时,0.1mol/L醋酸溶液的pH约为3;③10mL1mol/L醋酸恰好与10mL1mol/LNaOH溶液完全反应;④常温下,测得醋酸钠溶液的pH>7;
大小相同的铁片与pH相同盐酸和醋酸反应,刚开始时醋酸和盐酸产生H2速率相同;②室温时,0.1mol/L醋酸溶液的pH约为3;③10mL1mol/L醋酸恰好与10mL1mol/LNaOH溶液完全反应;④常温下,测得醋酸钠溶液的pH>7; 醋酸溶液的导电性比盐酸溶液的弱;⑥常温下,将pH=1的醋酸和盐酸稀释相同的倍数倍,测得醋酸的pH变化较小。
醋酸溶液的导电性比盐酸溶液的弱;⑥常温下,将pH=1的醋酸和盐酸稀释相同的倍数倍,测得醋酸的pH变化较小。
A.②④⑤⑥ B.②④⑥ C.①②④ D.②⑥
-
室温下,用0.100 mol·L-1 NaOH溶液分别滴定20.00 mL 0.100 mol·L-1 的盐酸和醋酸,如图所示。
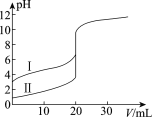
(1)表示滴定盐酸的曲线是________。(填I或II)
(2)当醋酸中滴入10 mL NaOH溶液时,溶液中含有的溶质有:________;溶液中离子浓度由大到小顺序为:________。
(3)当醋酸中滴入20 mL NaOH溶液时,将所得溶液加热,溶液pH随温度变化如图所示。下列说法正确的是________。(填序号)
a. 加热促进水的电离和醋酸钠水解
b. 加热使溶液碱性减弱
c. 加热使溶液中c(H+)/c(OH-)比值减小

-
室温下,用0.100mol/L NaOH溶液分别滴定20.00ml 0.100mol/L 的盐酸和醋酸,滴定曲线如图所示,下列说法正确的是( )
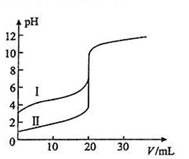
A、Ⅰ表示的是滴定盐酸的曲线
B、PH=7时,滴定醋酸消耗V(NaOH)小于20ml
C、V(NaOH) =20ml时,C(Cl— )== C(CH3COO— )
D、V(NaOH) =10ml时,醋酸溶液中:C(Na+ )> C(CH3COO— )> C(H+ )> C(OH— )
-
已知:电导率越大导电能力越强。25℃时,用0.100 mol/L NaOH溶液分别滴定10.00 mL 浓度均为0.100 mol/L的盐酸和醋酸溶液,测得滴定过程中溶液的电导率如图所示(注:混合后溶液体积等于混合前两溶液体积之和)。下列说法正确的是
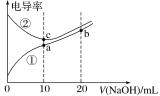
A. 曲线①代表滴定盐酸的曲线
B. a点溶液中:c(OH-)+c(CH3COO-)-c(H+)=0.1mol/L
C. a、b、c三点溶液中水的电离程度:c>a>b
D. b点溶液中:c(OH-)=c(H+)+c(CH3COO-)+2c(CH3COOH)
-
若用AG表示溶液的酸度,AG的定义为AG=lg 。室温下实验室中用0.01 mol·L-1的氢氧化钠溶液滴定20.00 mL 0.01 mol·L-1醋酸,滴定过程如图所示,下列叙述正确的是
。室温下实验室中用0.01 mol·L-1的氢氧化钠溶液滴定20.00 mL 0.01 mol·L-1醋酸,滴定过程如图所示,下列叙述正确的是
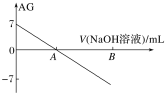
A.室温下,醋酸的电离常数约为10-5
B.A点时加入氢氧化钠溶液的体积为20.00 mL
C.若B点为40 mL,所得溶液中:c(Na+)=c(CH3COO-)+c(CH3COOH)
D.从A到B,水的电离程度逐渐变大






