-
过氧化碳酰胺[CO(NH2)2·H2O2]是一种与过氧化氢性质相似的固体氧化剂,因其具有价廉、安全、易于储存、使用方便等优点,被广泛应用于日用化工、食品、建筑、农业等领域。请回答下列问题:
I.过氧化碳酰胺的制备
实验室用尿素和双氧水制备过氧化碳酰胺的步骤如下:取5.0 mL 30% H2O2放入50 mL锥形瓶中,加入1.8 g尿素(H2O2与尿素的物质的量之比为3:2);将装有反应混合物的锥形瓶放入水浴锅中,水浴加热至60 °C,加热几分钟,得到一种澄清、透明的溶液;将溶液转移到大蒸发皿上,在60 °C恒温水浴锅上缓慢蒸发;溶液中缓慢析出针状晶体;当结晶完全后,将针状晶体用滤纸吸去水分,称重,得产品2.5 g。
已知:CO(NH2)2+H2O2=CO(NH2)2·H2O2。
(1)H2O2的电子式为________________________。
(2)水浴加热时温度控制在60 °C最好,其原因为___________________________。
(3)过氧化碳酰胺的产率为___________%(结果保留1位小数)。
II.过氧化碳酰胺的性质
称取0.50g过氧化碳酰胺于试管中,加5mL水溶解。
过氧化碳酰胺的鉴定反应步骤及现象如下:
在试管中加入5滴过氧化碳酰胺溶液、0.5 mL乙醚和2滴2 mol·L-1 H2SO4酸化,再加入2~3滴0.1 mol. L-1K2CrO4溶液.振荡试管,上层呈深蓝色,过氧化氢和重铬酸钾发生非氧化还原反应生成蓝色的CrO5,CrO5在乙醚中稳定,碳酰胺[CO(NH2)2]不和重铬酸钾反应,下层呈绿色,CrO5在水中不稳定,易分解生成Cr(OH)2+和O2。
(4)检验O3可用CrO3与O3反应,得蓝色晶体CrO5:CrO3+O3 →CrO5(未配平),则该反应中氧化剂与还原剂的个数比为_____________。
(5)CrO5在水中分解的离子方程式为_______________。
III.过氧化碳酰胺中活性氧含量的测定(以过氧化氢中氧原子的质量分数计)
准确称量7.5200 g产品,配制成100 mL溶液,用移液管移取10.00 mL溶液于250 mL锥形瓶中,加人适量水和硫酸,用0.1000mol·L-1的酸性高锰酸钾标准溶液平行滴定三次,平均消耗的体积为24.00mL。.
(6)配制100mL过氧化碳酰胺溶液所用到的玻璃仪器有____________,判断滴定至终点的现象为___________________,过氧化碳酰胺中活性氧含量为_____________(结果保留1位小数)。
高三化学实验题中等难度题查看答案及解析
-
过氧化碳酰胺[CO(NH2)2•H2O2]是一种高效、安全的固体消毒剂,白色晶体,易溶于水,稍高温度时可发生分解。某化学小组欲制备少量过氧化碳酰胺,并测定其活性氧的含量,回答下列问题。
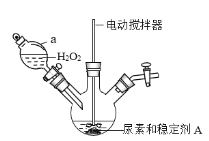
(一)过氧化碳酰胺的制备
(1)制备过氧化碳酰胺的发生装置如图所示(夹持装置略去),在组装仪器前应对a装置进行的操作是________。
(2)该反应的最佳温度为35℃,采用的合适加热方式为________。
(二)过氧化碳酰胺中活性氧含量的测定(以产品中过氧化氢所含氧原子的质量分数为准计算)。称取10.0g产品,配成250mL溶液,取25.00mL溶液于锥形瓶中,加入适量稀硫酸,用0.10mol•L-1高锰酸钾标准溶液滴定三次,消耗高锰酸钾溶液的体积分别为21.02mL、21.23mL、20.98mL。
(1)写出KMnO4标准溶液与H2O2反应的化学方程式____________。
(2)过氧化碳酰胺中活性氧含量为_____%。若配制过氧化碳酰胺溶液定容时俯视刻度线,则测得过氧化碳酰胺中活性氧含量______(填“偏高”“偏低”或“无影响”)。
(三)稳定剂A对过氧化碳酰胺的制备有一定的影响,小组成员查阅文献资料得到有关稳定剂及数据如表所示。则选择最佳稳定剂A为________,理由是_____________。
稳定剂名称
过氧化碳酰胺活性氧的含量/10-2
初始数
室温储存30天后数
减少量
热储存保温1天后数
减少量
EDTA
16.96
16.87
0.09
16.92
0.04
柠檬酸
16.94
16.90
0.04
16.91
0.03
EDTA与柠檬酸混合物
16.95
16.90
0.05
16.90
0.05
柠檬酸与焦磷酸钠混合物
16.90
16.86
0.04
16.87
0.03
高三化学实验题中等难度题查看答案及解析
-
【必考题】
过氧化尿素[CO(NH2)2•H2O2]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域.其合成如下: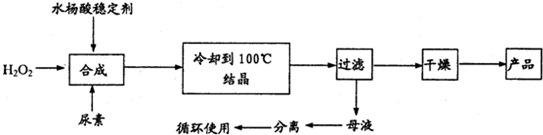
试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,并控制合成温度在25-30℃,其主要原因是______.
(2)从母液中分离出H2O2和尿素,采用的操作是______.
(a)盐析 过滤 (b)分液 过滤 (c)减压蒸馏 结晶 (d)常压蒸馏 萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O234%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容.准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000mol/L KMnO4 标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应).
①KMnO4溶液应盛放在______式(选填:“酸”、“碱”)滴定管中.
②完成并配平方程式:______MnO4-+______H2O2+______H+=______Mn2++______H2O+______
③根据滴定结果,可确定产品中活性氧的质量分数为:______.
④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量______(选填:“偏高”、“偏低”或“不变”).
⑤根据本次实验测得的活性氧含量,可判断该实验产品所含的一种主要杂质为______.高三化学解答题中等难度题查看答案及解析
-
【必考题】
过氧化尿素[CO(NH2)2•H2O2]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域.其合成如下: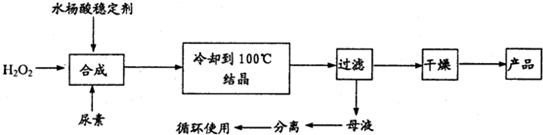
试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,并控制合成温度在25-30℃,其主要原因是______.
(2)从母液中分离出H2O2和尿素,采用的操作是______.
(a)盐析 过滤 (b)分液 过滤 (c)减压蒸馏 结晶 (d)常压蒸馏 萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O234%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容.准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000mol/L KMnO4 标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应).
①KMnO4溶液应盛放在______式(选填:“酸”、“碱”)滴定管中.
②完成并配平方程式:______MnO4-+______H2O2+______H+=______Mn2++______H2O+______
③根据滴定结果,可确定产品中活性氧的质量分数为:______.
④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量______(选填:“偏高”、“偏低”或“不变”).
⑤根据本次实验测得的活性氧含量,可判断该实验产品所含的一种主要杂质为______.高三化学解答题中等难度题查看答案及解析
-
过氧化尿素[CO(NH2)2·H2O2 ]是一种无毒、无味的白色结晶粉末,具有尿素和过氧化氢双重性质,是一种新型的氧化剂和消毒剂,广泛应用于漂白、纺织、医药、农业、养殖业等领域。其合成如下:
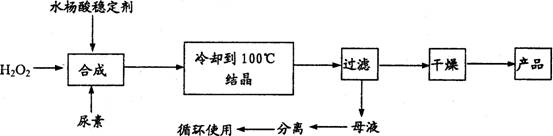
试回答下列问题:
(1)实际生产中需控制n(H2O2):n(CO(NH2)2)]=1.2:1,并控制合成温度在25—30℃,其主要原因是___________________________________。
(2)从母液中分离出H2O2和尿素,采用的操作是___________。
(a)盐析 过滤 (b)分液 过滤 (c)减压蒸馏 结晶 (d)常压蒸馏 萃取
(3)为测定产品中活性氧的含量(活性氧16%,相当于H2O2 34%),称取干燥样品12.000g,溶解,在250mL容量瓶中定容。准确量取25.00mL于锥形瓶中,加入1mL 6mol/L的硫酸,然后用0.2000 mol/L KMnO4 标准溶液滴定,至滴入最后一滴时,溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4溶液20.00mL(KMnO4溶液与尿素不反应)。
①KMnO4溶液应盛放在________式(选填:“酸”、“碱”)滴定管中。
②完成并配平方程式:__MnO4-+ ___H2O2+___H+=___Mn2++ ____H2O+___ _____
③根据滴定结果,可确定产品中活性氧的质量分数为:___________。
④若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量______(选填:“偏高”、“偏低”或“不变”)。
⑤根据本次实验测得的活性氧含量,可判断该实验产品所含的一种主要杂质为_________。
高三化学填空题简单题查看答案及解析
-
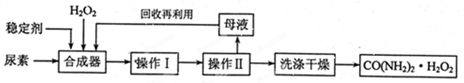
(14分)尿素可作为H2O2的稳定载体,生产一种固态、耐储存、易运输的新型氧化剂和消毒剂—过氧化尿素[CO(NH2)2·H2O2],其合成工艺流程如下:
请回答下列问题:
(1)操作I、II的名称分别是________、_________。CO(NH2)2·H2O2分子中尿素和过氧化氢之间以________结合,其结合力较弱,具有尿素和过氧化氢双重性质。
(2)工业上生产尿素所需的原料气可由天然气与水反应制备,已知:
①甲烷、氢气的燃烧热分别为890.3kJ/mol、285.8kJ/mol
②H2O(l)=H2O(g) H =+44.0kJ/mol
写出CH4与水蒸气作用生产CO2和H2的热化学方程式: 。
(3)为测定产品中H2O2的含量,称取干燥样品12.0g配成250mL溶液,取25.00mL
于锥形瓶中,加入适量硫酸酸化,用0.20mol/LKMnO4标准溶液滴定,三次滴定平均消耗KMnO4溶液20.00mL.(KMnO4溶液与尿素不反应).
①完成并配平方程式:
②计算出产品中H2O2的质量分数为_____________。
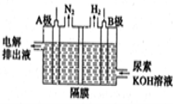
(4)电解含尿素的废水既可以处理废水,又可制得纯氢,电解原理如图所示。电解池中隔膜仅阻止气体通过,A、B两极均为惰性电极。请写出阳极的电极反应方程为_____________。
高三化学填空题困难题查看答案及解析
-
(16分)尿素可作为H2O2的稳定载体,生产一种固态、耐储存、易运输的新型氧化剂和消毒剂—过氧化尿素[CO(NH2)2·H2O2],其合成工艺流程如下:

请回答下列问题:
(1)操作I、II的名称分别是______、_______。CO(NH2)2·H2O2分子中尿素和过氧化氢之间以________结合,其结合力较弱,具有尿素和过氧化氢双重性质。
(2)工业上生产尿素所需的原料气可由天然气与水反应制备,已知:
①甲烷、氢气的燃烧热分别为890.3KJ/mol、285.8kJ/mol
②

写出CH4与水蒸气作用生产CO2和H2的热化学方程式:_______________。
(3)合成过氧化氢尿素加入的稳定剂可以是水杨酸、酒石酸等。酒石酸分子式为C4H6O6,其核磁共振氢谱只有3种锋,只含羧基和羟基两种官能团,则酒石酸的结构简式为_____。
(4)为测定产品中H2O2的含量,称取干燥样品12.0g配成250mL溶液,取25.00mL
于锥形瓶中,加入适量硫酸酸化,用0.20mol/LKMnO4标准溶液滴定,三次滴定平均消耗KMnO4溶液20.00mL.(KMO4溶液与尿素不反应).
①完成并配平方程式:
MnO4-+
H2O2+
_________=Mn2++
O2↑+
___;
②计算出产品中H2O2的质量分数为_______。
(5)电解尿素的废水既可以处理废水,又可制得纯氢,电解原理如图所示。电解池中隔膜仅阻止气体通过,B两极均为惰性电极。B极连接电源的____极(填
“正”或“负”),阳极电极反应方程为_____________。

高三化学简答题中等难度题查看答案及解析
-
过氧化氢俗称双氧水,它是一种液体,易分解为水和氧气,常作氧化剂、漂白剂和消毒剂,为贮存、运输、使用的方便,工业常将H2O2转化为固态的过碳酸钠晶体,该晶体具有Na2CO3和H2O2的双重性质.下列物质不会使过碳酸钠晶体失效的是( )
A.MnO2
B.H2S
C.稀盐酸
D.NaHCO3高三化学选择题中等难度题查看答案及解析
-
过氧化尿素(CO(NH2)2·H2O2)是过氧化氢水溶液与尿素的加和物,兼有尿素和过氧化氢的性质,是一种新型漂白、消毒剂,广泛应用于农业、医药、日用化工等领域。某化学小组同学用低浓度的双氧水和饱和尿素[CO(NH2)2]溶液在30℃条件下用右图装置合成过氧化尿素。请回答下列问题:
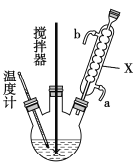
(1)仪器X的名称是______________;
(2)制备过氧化尿素的化学方程式为_______________________,反应时采取的受热方式为_____________;
(3)搅拌器不能选择铁质材料的原因是______________________
(4)过氧化尿素中活性氧含量的高低直接决定产品的质量,合格产品中活性氧的含量≥16%(相当于其中含H2O234%)。为了确定所得产品合格与否,质检员称取干燥样品8.000g,溶解于水,在250mL容量瓶中定容,准确量取其中25.00mL溶液于锥形瓶中,加入1mL6mol·L-1H2SO4,然后用0.2000mol·L-1KMnO4标准溶液滴定样品中的H2O2(KMnO4溶液与尿素不反应)。三次滴定平均消耗KMnO4溶液20.000mL:
①请完善滴定时反应的离子方程式:__MnO
+___H2O2+______==_______________
②若滴定前滴定管尖嘴处有气泡,滴定后消失,会使测得的活性氧含量_______(填“偏高”、“偏低”或“不变”);
③根据滴定结果确定产品质量_______(填“合格”或“不合格”),活性氧的质量分数为_________。
高三化学实验题中等难度题查看答案及解析
-
过氧化尿素[CO(NH2)2·H2O2]是一种白色粉末,溶于水形成的溶液呈弱酸性。过氧化尿素不稳定,在痕量重金属离子等活性催化剂的存在下迅速分解。工业生产过氧化尿素的原理和流程如下。
原理:CO(NH2)2+H2O2
CO(NH2)2·H2O2
流程:
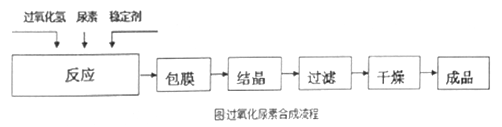
回答下列问题:
(l)已知过氧化尿素[CO(NH2)2·H2O2]中的CO(NH2)2与H2O2以氢键连接,其中碳元素的化合价是___________。(填序号)
A. +2价 B. -l价 C. 0价 D. +4价
(2)过氧化尿素鉴定反应:在重铬酸钾酸性溶液中加入乙醚和少许过氧化尿素,振荡。上层乙醚呈蓝色,这是由于在酸性溶液中过氧化尿素中的过氧化氢与重铬酸钾反应生成较稳定的蓝色过氧化铬(CrO5)。写出H2O2与重铬酸钾反应的离子方程式__________。
(3)经过上述化学工艺后的产品是粗产品。已知30℃时尿素的溶解度远大于过氧化尿素的溶解度,则提纯粗产品的操作顺序是___________ (填序号)。
①冷却至30℃结晶 ②过滤 ③蒸发浓缩 ④溶解 ⑤洗涤
(4)在实验室中采用上述原理制取过氧化尿素,搅拌器的材质一般用玻璃而非铁质,原因是___。
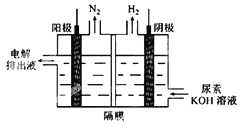
(5)电解尿素[CO(NH2)2]的碱性溶液制氢的装置示意图见图(电解池中隔膜仅阻止气体通过,阴、阳极均为惰性电极)。电解时,阳极的电极反应式为________。
(6)Ⅰ.为测定产品中H2O2的含量,常用KMnO4溶液滴定H2O2,高锰酸钾标准溶液通常放置时间较长,因此在滴定H2O2前,常用现配的草酸钠溶液先标定出KMnO4标准溶液的浓度。
Ⅱ.称取过氧化尿素样品4.000g ,溶解在250mL容量瓶中定容。准确量取25.00mL于锥形瓶中,加入1.00mL 6mo1/L的硫酸,用标定过的0.2000mol/L的高锰酸钾标准溶液滴定至滴入最后一滴时溶液显浅红色且半分钟内不褪色,三次滴定平均消耗KMnO4标准溶液10.00mL,(KMnO4与尿素不反应)。
①H2O2的质量分数是_______ (精确至0.1%)。
②若装草酸钠溶液的滴定管水洗后未润洗,最终H2O2的质量分数______ (填“偏大”、“偏小”或“不变”)
高三化学简答题困难题查看答案及解析