-
(1)利用电化学原理,将 NO2、O2 和熔融 KNO3 制成燃料电池,模拟工业电解法来处理含 Cr2O72-废水,如下图所示;电解过程中溶液发生反应: Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2 O。
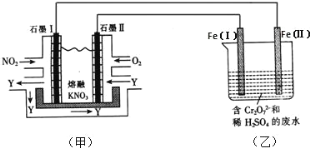
①甲池工作时,NO2 转变成绿色硝化剂 Y,Y 是 N2O5,可循环使用,则石墨Ⅱ附近发生的电极反应式为______。
②向完全还原为 Cr3+的乙池工业废水中滴加 NaOH 溶液,可将铬以 Cr(OH)3 沉淀的形式除去,已知 Cr(OH)3 存在以下溶解平衡:Cr(OH)(s) Cr3+(aq)+3OH-(aq),常温下 Cr(OH)3 的溶度积 K=c(Cr3+)•c(3OH-)=1.0×10-32,要使 c(Cr3+)降至 10-5mol•L-1,溶液的 pH 应调至___________。
Cr3+(aq)+3OH-(aq),常温下 Cr(OH)3 的溶度积 K=c(Cr3+)•c(3OH-)=1.0×10-32,要使 c(Cr3+)降至 10-5mol•L-1,溶液的 pH 应调至___________。
(2)镉镍可充电电池在现代生活中有广泛应用,它的充、放电反应按下式进行: Cd+2NiO(OH)+H2O Cd(OH)2+2Ni(OH)2
Cd(OH)2+2Ni(OH)2
回答下列问题:
①放电时,金属 Cd 作______极;
②充电时的阳极电极反应式为。_____
③充电时,当电路中通过 0.2moleˉ,阴极质量将___________(填“增加”、“减少”)___________。
-
利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,模拟工业电解法来处理含Cr2O72-废水,如下图所示;电解过程中溶液发生反应:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O

(1)甲池工作时,NO2转变成绿色硝化剂Y,Y是N2O5,可循环使用。则石墨Ⅱ是电池的 极;石墨Ⅰ附近发生的电极反应式为 。
(2)工作时,甲池内的NO3-离子向 极移动(填“石墨Ⅰ”或“石墨Ⅱ”);在相同条件下,消耗的O2和NO2的体积比为 。
(3)乙池中Fe(Ⅰ)棒上发生的电极反应为 。
(4)若溶液中减少了0.01 mol Cr2O72-,则电路中至少转移了 mol电子。
(5)向完全还原为Cr3+的乙池工业废水中滴加NaOH溶液,可将铬以Cr(OH)3沉淀的形式除去,已知Cr(OH)3存在以下溶解平衡:Cr(OH)3(s)  Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-)=1.0×10-32,要使c(Cr3+)降至10-5mol·L-1,溶液的pH应调至 。
Cr3+(aq)+3OH-(aq),常温下Cr(OH)3的溶度积Ksp=c(Cr3+)·c3(OH-)=1.0×10-32,要使c(Cr3+)降至10-5mol·L-1,溶液的pH应调至 。
-
工业含铬(Cr)废水的处理原理是将Cr2O72-转化为Cr3+,再将Cr3+转化为沉淀.废水pH与Cr2O72-转化为Cr3+的关系如图1,实验室模拟工业电解法处理含铬废水的装置如图2:
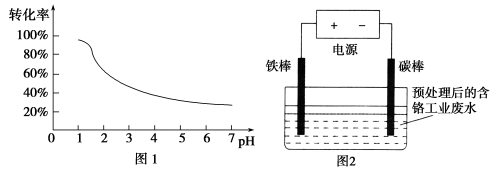
有关数据如下表所示:
| 沉淀物 | Fe(OH)3 | Fe(OH)2 | Cr(OH)3 |
| 开始沉淀的pH | 1.9 | 7.5 | 4.3 |
| 完全沉淀的pH | 3.4 | 9.7 | 7.6 |
请根据以上知识回答下列问题:
(1)含铬废水预处理的方法是 。
(2)电解过程中阳极质量减小,阴极有气体产生,写出两极的电极反应式:
阳极 ,阴极 。
(3)写出Cr2O72-转化为Cr3+的离子方程式: 。
(4)每处理1molCr2O72-,外电路中转移 mol电子。
(5)电解过程中解液的pH (填增大、减小或不变)
(6)处理过程中,当废水颜色不再发生明显变化时,切断电源,取出电极。此时,溶液中的阳离子有Fe2+、Fe3+、Cr3+,若想用调节pH的方法得到纯净的Cr(OH)3沉淀,应先向溶液中加入适量的 ,再调节pH= ,过滤后继续调节pH= 8。
-
工业上常用Fe作电极电解处理含Cr2O72-的酸性废水,最终使铬元素以Cr(OH)3沉淀的形式除去。某科研小组用该原理处理污水,设计装置如图所示。下列说法一定不正确的是
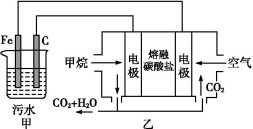
A.燃料电池中若有1.6 g CH4参加反应,则甲中C电极理论上生成气体体积为8.96 L
B.实验时若污水中离子浓度较小,导电能力较差,可加入适量的Na2SO4
C.该燃料电池正极的电极反应式为:O2+4e-+2CO2 2
2
D.甲中阳极附近溶液中的离子反应方程式是:  +6Fe2++14H+
+6Fe2++14H+ 2Cr3++6Fe3++7H2O
2Cr3++6Fe3++7H2O
-
含铬(Cr)工业废水的处理原理是将Cr2O72-转化为Cr3+,再将Cr3+转化为沉淀。转化过程中,废水pH与Cr2O72-转化为Cr3+的关系如图1所示,实验室模拟工业电解法处理含铬废水的装置如图2所示。


请根据以上知识回答下列问题:
(1)含铬废水预处理的方法是______________。
(2)写出下列反应的离子方程式:
①电解过程中的阴极反应式_________________;
②Cr2O72-转化为Cr3+的离子方程式________________。
-
含铬(Cr)工业废水的处理原理是将Cr2O72-转化为Cr3+,再将Cr3+转化为沉淀。转化过程中,废水pH与Cr2O72-转化为Cr3+的关系如图1所示,实验室模拟工业电解法处理含铬废水的装置如图2所示。
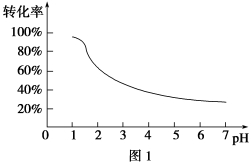
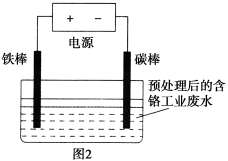
请根据以上知识回答下列问题:
(1)含铬废水预处理的方法是__________________。
(2)写出下列反应的离子方程式:
①电解过程中的阴极反应式___________________________;
②Cr2O72-转化为Cr3+的离子方程式_______________________。
-
下列装置由甲、乙两部分组成(如图所示),甲是将废水中乙二胺[H2N(CH2)2NH2]氧化为环境友好物质所形成的化学电源;乙利用装置甲模拟工业电解法来处理含Cr2O72-废水,电解过程中溶液发生反应:Cr2O72-+6Fe2++14H+=2Cr3++6Fe3++7H2O。当电池工作时,下列说法错误的是
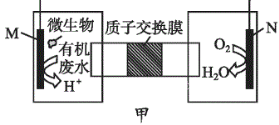
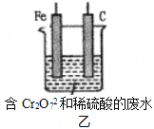
A.甲中H+透过质子交换膜由左向右移动
B.乙池中Fe棒应与甲池中的M极相连
C.M极电极反应式:H2N(CH2)2NH2+4H2O-16e-=2CO2↑+N2↑+16H+
D.若溶液中减少了0.0lmolCr2O72-,则电路中至少转移了0.12 mol电子
-
电化学在日常生活中用途广泛,图①是镁-次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O=Cl-+Mg(OH)2↓,图②是Cr2O72-的工业废水的处理。下列说法正确的是( )

A. 图②中Cr2O72-离子向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去
B. 图②的电解池中,有0.084 g阳极材料参与反应,阴极会有336mL的气体产生(标况)
C. 图①中发生的还原反应是:Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓
D. 若图①中3.6g镁溶解产生的电量用以图②废水处理,理论可产生10.7g氢氧化铁沉淀
-
电化学在日常生活中用途广泛,图①是镁-次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O=Cl-+Mg(OH)2↓,图②是Cr2O72-的工业废水的处理。下列说法正确的是( )

A. 图②中Cr2O72-离子向惰性电极移动,与该极附近的OH-结合转化成Cr(OH)3除去
B. 图②的电解池中,有0.084 g阳极材料参与反应,阴极会有336mL的气体产生(标况)
C. 图①中发生的还原反应是:Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓
D. 若图①中3.6g镁溶解产生的电量用以图②废水处理,理论可产生10.7g氢氧化铁沉淀
-
电化学在日常生活中用途广泛,图甲是镁—次氯酸钠燃料电池,电池总反应为:Mg+ClO-+H2O=Cl-+Mg(OH)2↓,图乙是含Cr2O72-的工业废水的处理。下列说法正确的是( )
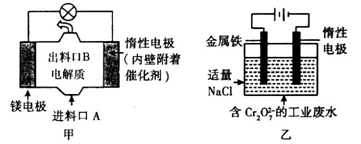
A. 图甲中发生的还原反应是Mg2++ClO-+H2O+2e-=Cl-+Mg(OH)2↓
B. 图乙中Cr2O72-向惰性电极移动,与该极附近的OH-结合,转化成Cr(OH)3除去
C. 图乙电解池中,若有0.84 g阳极材料参与反应,则阴极会有168 mL(标准状况)的气体产生
D. 若图甲燃料电池消耗0.36 g镁产生的电量用以图乙废水处理,理论上可产生1.07g氢氧化铁沉淀

Cr3+(aq)+3OH-(aq),常温下 Cr(OH)3 的溶度积 K=c(Cr3+)•c(3OH-)=1.0×10-32,要使 c(Cr3+)降至 10-5mol•L-1,溶液的 pH 应调至___________。
Cd(OH)2+2Ni(OH)2











