-
一定条件下,2L密闭容器中,金属钠和CO2可制得金刚石:4Na+3CO2⇌2Na2CO3+C(s,金刚石)。
(1)上述反应中涉及的元素原子的半径从大到小的顺序为:___。
(2)能证明碳元素与氧元素非金属性强弱的事实是___(选填编号)。
a.最高价氧化物水化物的酸性 b.两种元素的气态氢化物的沸点
c.CO2中元素的化合价 d.与氢气反应的难易程度
(3)高压下,科学家成功地将CO2转化为具有类似SiO2结构的原子晶体,比较两种原子晶体的熔沸点:___,并说明理由:___。除了金刚石外,碳的单质还有许多同素异形体,比如石墨、C60等。石墨烯是由碳原子构成的单层片状结构的新材料,可由石墨剥离而成,是目前发现的最薄、强度最大、导电导热性能最强的一种新材料。
(4)石墨烯中的碳原子间以___键结合,下列关于石墨烯的叙述正确的是___。
A.石墨烯与石墨属于同位素
B.石墨烯与石墨完全燃烧的产物都是二氧化碳
C.石墨烯是一种烯烃。
D.12g石墨烯中含有6.02×1022个碳原子
高三化学填空题中等难度题查看答案及解析
-
(16分)Ⅰ.已知:
4Na(g)+3CO2(g)=2Na2CO3(l)+C(s,金刚石) △H=-1080.9kJ/mol
4Na(g)+CO2(g)=2Na2O(s)+C(s,金刚石) △H=-357.5kJ/mol
试写出固体Na2O与固体C(金刚石)反应得到气体Na和液态Na2CO3的热化学方程式 。
Ⅱ.硝基苯甲酸乙酯在OH— 存在下发生水解反应:O2NC6H4COOC2H5+OH-
O2NC6H4COO-+C2H5OH
两种反应物的初始浓度均为0.050mol/L ,某温度下测得O2NC6H4COOC2H5的转化率α随时间变化的数据如表所示:
t/s
0
120
180
240
330
530
600
700
800
α/%
0
33
42
49
59
73
74
75
75
回答下列问题:
(1)该反应在330~530s的平均反应速率为 (只列出算式,不做运算)。
(2)试计算某温度下该反应的平衡常数(写出计算过程)。
(3)为提高O2NC6H4COOC2H5的转化率,可以采取的措施有 ,(写2条)。
Ⅲ.(1)下图装置中,开始电解时,Al电极反应式为 ,石墨电极反应式为 。
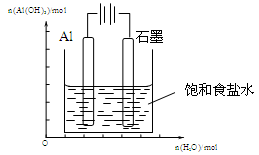
(2)通电一段时间后测得有0.6mol电子转移,作出Al(OH)3物质的量与消耗H2O的物质的量的的图象(反应物足量,作出标注)。
高三化学填空题困难题查看答案及解析
-
中国科学家用金属钠和CO2在一定条件下制得了金刚石:4 Na + 3CO2
2 Na2CO3 + C(金刚石),以下是一些物质的熔沸点数据(常压):
钠
Na2CO3
金刚石
石墨
熔点(℃)
97.8
851
3550
3850
沸点(℃)
882.9
1850(分解产生CO2)
----
4250
(1)若反应在常压、890℃下进行,写出该反应的平衡常数表达式_____________________,若3v正(Na)=4v逆(CO2),则_____(选填序号)。
a.反应肯定达到平衡 b.反应可能达到平衡 c.反应肯定未达平衡
(2)若反应在10L密闭容器、常压下进行,5min内,测得金刚石的质量增加了6 g,该时间段内v(CO2)=______________,若反应温度由890℃升高到1860℃,则容器内气体的平均相对分子质量将________(选填“增大”、“减小”或“不变”) 。
(3)反应中还有石墨生成,已知:C(石墨)
C(金刚石),若升高温度,生成的碳单质中,金刚石的含量将增大,则该反应的正反应是_________反应(填“吸热”或“放热”)。
(4)碳酸钠溶液中滴入盐酸的反应过程如右图所示,反应至A点时,未产生二氧化碳,请用离子方程式解释原因:_________________,继续滴加盐酸,反应至B点,B点溶液中溶质的化学式是__________。

高三化学综合题中等难度题查看答案及解析
-
二氧化碳和钠在一定条件下可制得金刚石,其化学方程式为3CO2+4Na=2X+C(金刚石)。设NA为阿伏加德罗常数的值,下列有关此反应的叙述不正确的是
A.金刚石是自然界最坚硬的单质
B.1 mol CO2中含有的共用电子对数目为2NA
C.46g Na完全反应需要标准状况下CO2的体积为33.6L
D.当有0.4mo1 Na参与反应时,被还原的CO2的分子数目为0.1 NA
高三化学选择题中等难度题查看答案及解析
-
利用“ Na-CO2”电池将CO2变废为宝。我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,放电反应方程式为4Na+3CO2 =2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图所示,下列说法中错误的是( )
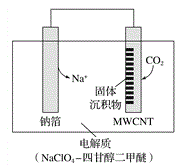
A. 电流流向为:MWCNT→导线→钠箔
B. 放电时,正极的电极反应式为 3CO2+4Na++4e-===2Na2CO3+C
C. 原两电极质量相等,若生成的Na2CO3和C全部沉积在电极表面,当转移0.2 mol e-时,两极的质量差为11.2g
D. 选用髙氯酸钠-四甘醇二甲醚做电解液的优点是导电性好,与金属钠不反应,难挥发
高三化学单选题中等难度题查看答案及解析
-
利用“ Na-CO2”电池将CO2变废为宝。我国科研人员研制出的可充电“ Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总反应为4Na+3CO2
 2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图所示:
2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图所示: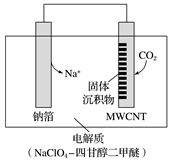
(1)放电时,正极的电极反应式为______________________________________________。
(2)若生成的Na2CO3和C全部沉积在电极表面,当转移0.2 mol e-时,两极的质量差为________ g。
(3)选用高氯酸钠-四甘醇二甲醚作电解液的优点是___________________________________(至少写两点)。
高三化学填空题中等难度题查看答案及解析
-
利用“Na-CO2”电池将CO2变废为宝。我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,放电反应方程式为4Na+3CO2=2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图3所示,下列说法中错误的是( )
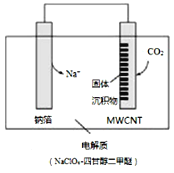
A. 电流流向为:MWCNT→导线→钠箔
B. 放电时,正极的电极反应式为 3CO2+4Na++4e-=2Na2CO3+C
C. 原两电极质量相等,若生成的Na2CO3和C全部沉积在电极表面,当转移0.2 mole-时,两极的质量差为11.2g
D. 选用髙氯酸钠-四甘醇二甲醚做电解液的优点是导电性好,与金属钠不反应,难挥发
高三化学单选题中等难度题查看答案及解析
-
利用“Na-CO2”电池将CO2变废为宝。我国科研人员研制出的可充电“Na-CO2”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,放电反应方程式为4Na+3CO2=2Na2CO3+C。放电时该电池“吸入”CO2,其工作原理如图3所示,下列说法中错误的是( )
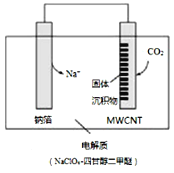
A.电流流向为:MWCNT→导线→钠箔
B.放电时,正极的电极反应式为 3CO2+4Na++4e-=2Na2CO3+C
C.原两电极质量相等,若生成的Na2CO3和C全部沉积在电极表面,当转移0.2 mole-时,两极的质量差为11.2g
D.选用髙氯酸钠-四甘醇二甲醚做电解液的优点是导电性好,与金属钠不反应,难挥发
高三化学单选题中等难度题查看答案及解析
-
中国科学家用金属钠和CO2在一定条件下制得了金刚石:
(1)配平上述反应的化学方程式: ___ Na + _____CO2
_____Na2CO3 + _____C(金刚石)。若反应过程中有0.15mol CO2反应,则电子转移的数目为:____________。
(2)CO2的电子式为:_________________,Na原子核外电子有_______个能级。
(3)已知:
常压下
钠
Na2CO3
金刚石
石墨
熔点(℃)
97.8
851
3550
3850
沸点(℃)
882.9
1850(分解产生CO2)
----
4250
若反应在常压、890℃下进行,写出该反应的平衡常数表达式______________________。若3v正(Na)=4v逆(CO2),则________(选填序号)。
a.反应肯定达到平衡 b.反应可能达到平衡 c.反应肯定未达平衡
(4)副产物Na2CO3溶于水后溶液呈碱性,请结合平衡移动的原理,用文字描述所得溶液呈碱性的原因:______________________________________________________________________________________。若在10升容器中,反应进行了5min, 金刚石的质量增加了6g,则5min里CO2的平均反应速率 为______________。
高三化学综合题简单题查看答案及解析
-
科学家最近研究出一种环保、安全的制取金刚石的方法,其原理可表示为: 4Na + 3CO2
2Na2CO3 + C ,下列有关说法正确的是
A.该反应为吸热反应 B.CO2中含α键又含π键
C.Na2CO3为离子晶体,只含离子键 D.每消耗2.24LCO2生成0.4克金刚石
高三化学选择题中等难度题查看答案及解析