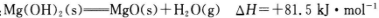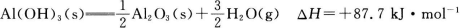-
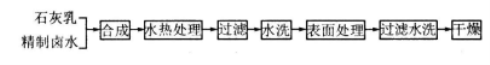
往有机聚合物中添加阻燃剂,可增加聚合物的使用安全性,扩大其应用范围。Mg(OH)2是一种常用的阻燃剂,生产工艺如下:

完成下列填空:
(1)精制卤水中的MgCl2与适量石灰乳反应合成碱式氯化镁[Mg(OH)2-xClx•mH2O],反应的化学方程式为___。
(2)合成反应后,继续在393K~523K下水热处理8h,发生反应:Mg(OH)2-xClx•mH2O→(1- )Mg(OH)2+
)Mg(OH)2+ MgCl2+mH2O,水热处理后,进行过滤、水洗。水洗的目的是___。
MgCl2+mH2O,水热处理后,进行过滤、水洗。水洗的目的是___。
(3)阻燃型Mg(OH)2具有晶粒大,易分散、与高分子材料相容性好等特点。上述工艺流程中与此有关的步骤是___。
(4)已知热化学方程式:Mg(OH)2(s)→MgO(s)+H2O(g)-81.5kJ•mol-1
Al(OH)3(s)→ Al2O3(s)+
Al2O3(s)+ H2O(g)-87.7kJ•mol-1
H2O(g)-87.7kJ•mol-1
Mg(OH)2和Al(OH)3起阻燃作用的主要原因是___。等质量Mg(OH)2和Al(OH)3相比,阻燃效果较好的是___,原因是___。
(5)该工业生产的原料还可以用来提取金属镁。请设计提取金属镁的工艺流程(框内写产物名称,箭头上标明转化条件):___

-
选考[化学——化学与技术](15分)往有机聚合物中添加阻燃剂,可增加聚合物的使用安全性,扩大其应用范围。Mg(OH)2是一种常用的阻燃剂,生产工艺如下:
完成下列填空:
(1)精制卤水中MgCl2的与适量石灰乳反应合成碱式氯化镁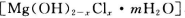 ,反应的化学方程式为_________。
,反应的化学方程式为_________。
(2)合成反应后,继续在393K~523K下水热处理8h,发生反应:
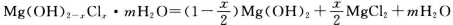 ,水热处理后,进行过滤、水洗。水洗的目的是_________。
,水热处理后,进行过滤、水洗。水洗的目的是_________。
(3)阻燃型 Mg(OH)2具有晶粒大,易分散、与高分子材料相容性好等特点。上述工艺流程中与此有关的步骤是________。
(4)已知热化学方程式: 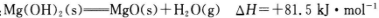
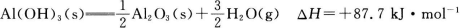
Mg(OH)2和Al(OH)3起阻燃作用的主要原因是_________。
等质量 Mg(OH)2和Al(OH)3 相比,阻燃效果较好的是_________,原因是____________________。
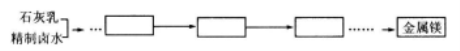
(5)该工业生产的原料还可以用来提取金属镁。请设计提取金属镁的工艺流程(框内写产物名称,箭头上标明转化条件):
-
向有机聚合物中添加阻燃剂,可增大聚合物的使用安全性,扩大其应用范围。Mg(OH)2是一种常用的阻燃剂,其生产工艺如图1所示:
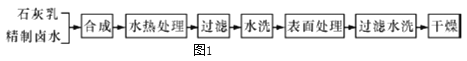
请完成下列填空:
(1)精制卤水中的MgCl2与适量石灰乳反应合成碱式氯化镁[Mg(OH)2-xClx⋅mH2O],发生反应的化学方程式为___。
(2)合成反应后,继续在393~523K下水热处理8h,发生反应Mg(OH)2-xClx⋅mH2O=(1- )Mg(OH)2+
)Mg(OH)2+ MgCl2+mH2O,水热处理后,进行过滤、水洗。水洗的目的是___。
MgCl2+mH2O,水热处理后,进行过滤、水洗。水洗的目的是___。
(3)阻燃型Mg(OH)2具有晶粒大、易分散、与高分子材料相容性好等特点。上述工艺流程中与此有关的步骤是___和___。
(4)已知热化学方程式:
Mg(OH)2(s)=MgO(s)+H2O(g) △H=+81.5kJ⋅mol-1
Al(OH)3(s)⇌ Al2O3(s)+
Al2O3(s)+ H2O(g) △H=+87.7kJ⋅mol-1
H2O(g) △H=+87.7kJ⋅mol-1
Mg(OH)2和A1(OH)3起阻燃作用的主要原因是:___
(5)该工业生产的原料还可以用来提取金属镁。请设计提取金属镁的工艺流程图2(框内写产物的化学式,箭头上下标明转化条件或操作名称):___、___、___、___。
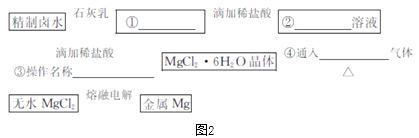
-
镁、铝、钙的某些化合物在生产、生活中有着重要应用。请按要求回答下列问题。
Ⅰ.化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时有如下分解反应:2Mg5Al3(OH)19(H2O)4 27H2O↑+10MgO+3Al2O3
27H2O↑+10MgO+3Al2O3
(1)除去固体产物中Al2O3的离子方程式为_________________。
(2)常温,MgO可溶于NH4Cl溶液的化学方程式为_______________。
Ⅱ.过氧化钙(CaO2)是一种白色、无毒、难溶于水的固体消毒剂。工业生产过程如下:①在NH4Cl溶液中加入Ca(OH)2;②不断搅拌的同时加入30% H2O2溶液(弱酸性),生成CaO2·8H2O沉淀;③经过陈化、过滤、水洗得到CaO2·8H2O,再脱水干燥得到CaO2。
(1) 可循环使用的物质是______。工业生产中常选用过量的反应物是Ca(OH)2而不是H2O2,这是因为__________________。
(2) 检验CaO2·8H2O是否洗净的操作是________。
(3) 测定产品中CaO2含量:取m g样品,与足量稀硫酸反应充分,生成的H2O2用c mol·L-1的KMnO4溶液滴定,消耗标准液的体积为V mL,则该样品中CaO2质量百分数为(含m、c、V的表达式)__________。
-
Mg(OH)2可用作塑料的阻燃剂。现以某矿石(主要成分为3MgO·2SiO2·2H2O,还有少量Fe2O3、FeO、CaO和Al2O3)为原料生产,其工艺流程如下:
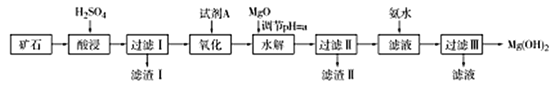
已知:
表1生成氢氧化物沉淀的pH
| 物质 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Mg(OH)2 |
| 开始沉淀的pH | 7.6 | 1.9 | 3.4 | 9.1 |
| 完全沉淀的pH | 9.6 | 3.2 | 4.7 | 11.1 |
表2原料价格表
| 物质 | 价格(元•吨-1) |
| 漂液(含25.2% NaClO) | 450 |
| 双氧水(含30%H2O2) | 2400 |
回答下列问题:
(1)酸浸时,为提高矿石的浸出率可采取的措施为_________(任写一条)。该过程H2SO4适当过量的目的是_______________、_________________。
(2)工业生产要求生产成本较低,产品尽量不含杂质。试剂A的最佳选择是______,写出其发生反应的离子方程式_______________________。
(3)水解过程需调节溶液pH,a的取值范围为______,滤渣II的成分是______(填化学式)。
(4)向过滤II所得滤液中加入一定量氨水,写出镁离于沉淀的离子方程式____________,该过程温度不宜过高的原因是_____________________。
(5)实际生产中,可由Mg(OH)2为原料制备单质镁,简述制备方法_____________
-
下列对于各种物质的应用说法错误的是
A. 硅胶作袋装食品的吸氧剂
B. 二氧化硫作纸浆的漂白剂
C. Al(OH)3可添加到塑料中作阻燃剂
D. ClO2是一种比Cl2更安全的自来水消毒剂
-
(本题共16分)锰是冶炼工业中常用的添加剂。以碳酸锰矿(主要成分为MnCO3,还含有铁、镍、钴等碳酸盐杂质)为原料生产金属锰的工艺流程如下:

已知25℃,部分物质的溶度积常数如下:
| 物质 | Mn(OH)2 | Co(OH)2 | Ni(OH)2 | MnS | CoS | NiS |
| Ksp | 2.1×10-13 | 3.0×10-16 | 5.0×10-16 | 1.0×10-11 | 5.0×10-22 | 1.0×10-22 |
(1)步骤Ⅰ中,MnCO3与硫酸反应的化学方程式是 。
(2)步骤Ⅱ中,MnO2在酸性条件下可将Fe2+离子氧化为Fe3+,反应的离子方程式是 ,加氨水调节溶液的pH为5.0~6.0,以除去Fe3+。
(3)步骤Ⅲ中,滤渣2的主要成分是 。
(4)步骤Ⅳ中,在 (填“阴”或“阳”)极析出Mn,电极反应方程式为 。
(5)电解后的废水中还含有Mn2+,常用石灰乳进行一级沉降得到Mn(OH)2沉淀,过滤后再向滤液中加入适量Na2S,进行二级沉降。为了将Mn2+降到1.0×10-9mol/L,则c(Na2S)至少是 mol/L。
-
下列物质性质与相应结果或应用的对应关系正确的是
A.酸性越强的含氧酸跟铁片反应产生氢气越快
B.将草木灰和硫铵混合施用,可使肥效更高
C.Mg(OH)2和Al(OH)3受热易分解,常用它们作阻燃剂
D.某地雨水经过一段时间,其pH由4.68降为4.28,因为水中溶解了较多的CO2
-
用碱式溴化镁废渣[主要成分为Mg(OH)Br,还含有少量有机溶剂及高分子化合物]生产C2H5Br(不溶于水,密度为1.46g/cm3)和MgCl2·6H2O,既可减少污染又可得化工原料,有关工艺流程如图所示:

回答下列问题:
(1)碱式溴化镁溶于盐酸时,1molMg(OH)Br消耗0.5mol/L的盐酸体积为_______________。
(2)分离Ⅰ操作为_______________(操作名称);分离Ⅱ操作时所需的玻璃仪器为_______________。
(3)提溴时,溶液预热至60℃时开始通入氯气,一段时间后,溶液的温度会自然升高到100℃,说明提溴反应为_______________(填“放热”或“吸热”)反应。提溴废液需减压蒸发浓缩,目的是_______________。
(4)在浓硫酸催化下,合成溴乙烷粗品的化学方程式为_______________;
(5)精制溴乙烷的步骤为水洗、Na2SO3溶液洗涤、水洗及干燥,其中Na2SO3溶液洗涤的目的是_______________。
(6)用惰性电极在一定条件下电解MgCl2溶液可制取催熟剂氯酸镁,该电解反应的化学方程式为_______________。
-
I.化合物Mg5Al3(OH)19(H2O)4可作环保型阻燃材料,受热时按如下化学方程式分【解析】
2Mg5Al3(OH)19(H2O)4 27H2O↑+10MgO+3A12O3
27H2O↑+10MgO+3A12O3
(1)写出该化合物作阻燃剂的两条依据____________________________________。
(2)用离子方程式表示除去固体产物中A12O3的原理________________________。
II.以冶铝的废弃物铝灰为原料制取超细α-氧化铝,既降低环境污染又可提高铝资源的利用率。已知铝灰的主要成分为A12O3(含少量杂质SiO2、FeO、Fe2O3),其制备实验流程如下:
(1)用图中“滤渣”和NaOH 焙烧制备硅酸钠,可采用的装置为_______(填选项编号)。
焙烧制备硅酸钠,可采用的装置为_______(填选项编号)。
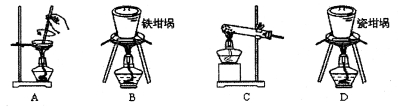
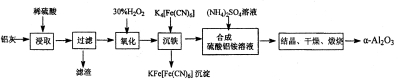
(2)验证“沉铁”后,溶液中是否还含有铁离子的操作方法为____________________。
(3)若用调节溶液的pH“沉铁”,则得到Fe(OH)3,己知:
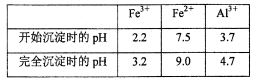
为保证产品的纯度,最好选用下列物质中的_______调节pH(填字母), 调节pH的范围为_____。
调节pH的范围为_____。
a.A12O3
B.H2SO4
C.NaOH
D.Na2CO3
(4)煅烧硫酸铝铵晶体,发生的主要反应为:
4[NH4Al(SO4)2·12H2O] 2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,
2Al2O3+2NH3↑+N2↑+5SO3↑+3SO2↑+53H2O,
将产生的气体通过下图所示的装置。
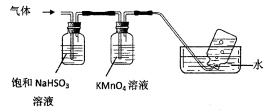
①集气瓶中收集到的气体是_____________________(填化学式)。
②KMnO4溶液褪色,发生的离子反应方程式为_________________________________。

)Mg(OH)2+
MgCl2+mH2O,水热处理后,进行过滤、水洗。水洗的目的是___。
Al2O3(s)+
H2O(g)-87.7kJ•mol-1

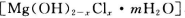 ,反应的化学方程式为_________。
,反应的化学方程式为_________。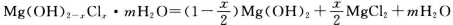 ,水热处理后,进行过滤、水洗。水洗的目的是_________。
,水热处理后,进行过滤、水洗。水洗的目的是_________。