-
醋酸、氢硫酸、碳酸在常温下的电离常数如下表:
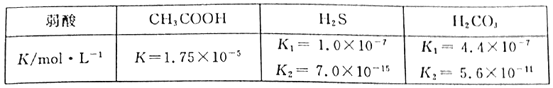
(1)能证明CH3COON是弱酸的事实是___。
A.CH3COOH易挥发
B.常温下,0.1mol·L-1CH3COONa溶液的pH大于7
C.醋酸不易腐蚀衣服
D.pH=3的CH3COOH溶液稀释10倍,溶液pH<4
E.等体积等浓度的CH3COOH溶液和盐酸,分别与足量镁粉反应,产生氢气一样多
F.将一定量的CH3COOH溶液加入Na2CO3溶液中,有气泡产生
(2)煤的气化过程中产生的H2S可用足量的Na2CO3溶液吸收,该反应的离子方程式为___。
(3)t℃时,0.0lmol·L-1NaOH溶液的pH=11,则该温度下,水的离子积Kw=___mol2·L-2;该温度下,将pH之和为13的NaOH溶液和CH3COOH溶液等体积混合,所得溶液呈___(填“酸”、“碱”或“中”)性。
(4)在室温下,用蒸馏水稀释0.0lmol·L-1CH3COOH溶液,下列各项呈减小趋势的是___。
A.
B.
C.溶液中c(H+)和c(OH-)的乘积
D.溶液导电性
E.水的电离程度
(5)25℃时,向1m30.1mol·L-1H2S溶液(pH=4)中加入FeSO4·7H2O晶体,当开始生成沉淀时,加入FeSO4·7H2O晶体的质量为___g。
[已知:Ksp(FeS)=6.3×10-18mol-1·L-2,忽略混合过程中的体积变化]
-
已知部分弱酸的电离平衡常数如下表:
| 弱酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
| 电离平衡常数(25℃) | Ka=1.75×10-5 | Ka=2.98×10-8 | Ka1=4.30×10-7
Ka2=5.61×10-11 | Ka1=1.54×10-2
Ka2=1.02×10-7 |
下列离子方程式正确的是
A.少量CO2通入NaClO溶液中:CO2+H2O+2ClO-=CO +2HClO
+2HClO
B.少量的SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
C.少量的SO2通入Na2CO3溶液中:SO2+H2O+2 CO =SO
=SO +2HCO3-
+2HCO3-
D.相同浓度NaHCO3溶液与NaHSO3溶液等体积混合:H++HCO3-=CO2↑+H2O
-
已知部分弱酸的电离平衡常数如下表:
| 弱酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
| 电离平衡常数 | Ka=1.75×10﹣5 | Ka=2.98×10﹣8 | Ka1=4.3×10﹣7 Ka2=5.61×10﹣11 | Ka1=1.54×10﹣2 Ka2=1.02×10﹣7 |
下列离子方程式正确的是( )
A.少量的CO2通入NaClO溶液中:CO2+H2O+2ClO﹣═CO32﹣+2HClO
B.少量的SO2通入Na2CO3溶液中:SO2+H2O+2CO32﹣═SO32﹣+2HCO3﹣
C.少量的SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO﹣═CaSO3↓+2HClO
D.相同浓度的NaHCO3溶液与NaHSO3溶液等体积混合:H++HCO3﹣═CO2↑+2H2O
-
已知部分弱酸的电离平衡常数如表:
| 弱酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
| 电离平衡常数(25℃) | 1.75×10−5 | 2.95×10−8 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.54×10−2 K2=1.02×10−7 |
下列选项正确的是( )
A. 少量CO2通入NaClO溶液中:CO2+H2O+2ClO−═CO32−+2HClO
B. 少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO−═CaSO3↓+2HClO
C. 少量SO2通入Na2CO3溶液中:SO2+H2O+2CO32−═SO32−+2HCO3−
D. 相同浓度NaHCO3溶液与NaHSO3溶液等体积混合:H++HCO3−═CO2↑+H2O
-
已知部分弱酸的电离平衡常数如表:
| 弱酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
| 电离平衡常数(25℃) | Ka=1.75×10-5 | Ka=2.98×10-8 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
下列离子方程式正确的是( )
A.少量CO2通入NaClO溶液中:CO2+H2O+2ClO-═CO +2HClO
+2HClO
B.少量SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-═CaSO3↓+2HClO
C.少量SO2通入Na2CO3溶液中:SO2+H2O+2CO ═SO
═SO +2HCO
+2HCO
D.相同浓度NaHCO3溶液与醋酸溶液等体积混合:H++HCO ═CO2↑+H2O
═CO2↑+H2O
-
已知部分弱酸的电离平衡常数如表所示:
| 弱酸 | 醋酸 | 次氯酸 | 碳酸 | 亚硫酸 |
| 电离平衡常数(25 ℃) | Ka=1.75×10-5 | Ka=2.98×10-8 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Ka1=1.54×10-2 Ka2=1.02×10-7 |
下列离子方程式正确的是
A.少量CO2通入NaClO溶液中:CO2+H2O+2ClO-=CO32-+2HClO
B.少量的SO2通入Ca(ClO)2溶液中:SO2+H2O+Ca2++2ClO-=CaSO3↓+2HClO
C.少量的SO2通入Na2CO3溶液中:SO2+H2O+2CO32-=SO32-+2HCO3-
D.相同浓度NaHCO3溶液与NaHSO3溶液等体积混合:H++HCO3-=CO2↑+H2O
-
常温下,几种弱酸的电离常数如下;
| 弱酸 | HF | CH3COOH | H2C2O4 |
| 电离常数(25℃) | 6.6×10-4 | 1.8×10-5 | K1=5.4×10-2 K2=5.4×10-5 |
25℃时,下列说法正确的是 ( )
A.pH相同的NaF、CH3COONa、Na2C2O4三种溶液,所含溶质的物质的量浓度为c(NaF)<c(Na2C2O4)<c(CH3COONa)
B.将HF溶液与Na2C2O4溶液混合,不发生化学反应
C.将V1亳升pH=3的CH3COOH溶液与V2毫升pH=11的NaOH溶液混合,所得溶液c(Na+)<c(CH3COO-),则V1一定大于V2
D.将等体积、等浓度的Na2C2O4溶液与NaHC2O4溶液混合,所得溶液中一定存在

-
常温下,部分弱酸的电离平衡常数如下表:
| 弱酸 | CH3COOH | HCN | H2CO3 |
| 电离平衡常数(25℃) | K1=1.76×10-5 | K1=4.9×10-10 | K1=4.3×10-7 K2=5.6×10-11 |
下列选项错误的是
A.中和等体积、等pH的CH3COOH溶液和HCN溶液消耗NaOH的量前者大于后者
B.可发生反应:2CH3COOH+CO32-=2CH3COO-+H2O+CO2↑
C.Na+、CN-、CH3COO-、HCO3-等离子能大量共存
D.等浓度的CH3COONa和NaCN溶液pH前者小于后者
-
下列说法正确的是
A.常温下,pH=9的碳酸钠溶液中由水电离出的c(OH-)=1×10-9mol·L-1
B.温度相同时,在弱酸溶液和强碱稀溶液中,水的离子积常数Kw相同
C.将pH=4的醋酸溶液稀释后,溶液中所有离子的浓度均降低
D.中和等体积pH相同的H2SO4和HCl溶液,消耗NaOH的物质的量为2:1
-
下表1是常温下几种弱酸的电离常数(K),表2是常温下几种难(微)溶物的溶度积常数(Ksp)。
表1几种弱酸的电离常数(25℃)
| 酸 | 电离常数(K) |
| CH3COOH | 1.8×10-5 |
| HNO2 | 5.1×10-4 |
| HCN | 6.2×10-10 |
| HClO | 3×10-8 |
表2几种难溶电解质的溶度积(25℃)
| 难(微)溶物 | 溶度积常数(Ksp) |
| BaSO4 | 1.1×10-10 |
| MgCO3 | 6.8×10-6 |
| CaSO4 | 9.1×10-6 |
| CaCO3 | 2.8×10-9 |
请回答下列问题:
(1)表1四种酸中,酸性最强的是____________(用化学式表示)。会使醋酸溶液中CH3COOH的电离程度增大,而电离常数不变的操作是__________。
A.升高温度 B.加水稀释
C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)常温下,相同物质的量浓度的表1中4种酸的钠盐pH由大到小的顺序是______________________________ (填钠盐的化学式)。若将pH=3的CH3COOH溶液与pH=11的NaOH溶液等体积混合,溶液中各离子浓度由大到小的排列顺序是______________________________。
(3)①根据表2四种难(微)溶物的溶度积常数计算 BaSO4的溶解度_______________(单位用g/L)表示,(已知 )。
)。
②在含有100mL0.2mol/L Ba2+、Ca2+、Mg2+的混合溶液中加入100mL0.1mol/LNa2SO4溶液,反应后溶液中生成的沉淀是_________,此时SO42-的浓度是_________。