-
基态原子的核外电子排布式为[Kr]4d105s1 的元素在元素周期表中的位置是
A.p 区、第五周期第ⅠB 族 B.ds 区、第五周期第Ⅷ族
C.d 区、第四周期第ⅠB 族 D.ds 区、第五周期第ⅠB 族
高二化学单选题简单题查看答案及解析
-
基态原子的核外电子排布为[Kr]4d105s1的元素属于的区、周期和族为
A.p区、第五周期、ⅠB族 B.ds区、第五周期、ⅠB族
C.d区、第四周期、ⅠB族 D.ds区、第五周期、Ⅷ族
高二化学选择题中等难度题查看答案及解析
-
基态原子的核外电子排布为[Kr]4d105s1的元素属于的区、周期和族为
A. p区、第五周期、ⅠB族 B. ds区、第五周期、ⅠB族
C. d区、第四周期、ⅠB族 D. ds区、第五周期、Ⅷ族
高二化学单选题简单题查看答案及解析
-
基态原子的核外电子排布为[Kr]4d105s1的元素属于的区、周期和族为
A.p区、第五周期、ⅠB族 B.ds区、第五周期、ⅠB族
C.d区、第四周期、ⅠB族 D.ds区、第五周期、Ⅷ族
【答案】B
【解析】
因为核外电子排布为[Kr]4d105s1的故为第五周期、ⅠB族,价电子轨道是sd,故为ds区,B项正确;答案选B。
考点:考查原子排布
【题型】选择题
【适用】较易
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】已知X、Y是主族元素,I为电离能,单位kJ/mol。根据下表所列数据判断错误的是
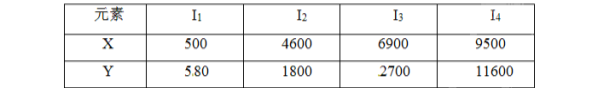
A.元素X的常见化合物价是+1价
B.若元素Y处于第3周期,它可与冷水剧烈反应
C.元素X与氯形成化合物时,化学式可能是XCl
D.元素Y是ⅢA族的元素
【答案】B
【解析】
A、由电离能数据可知,X可失去1个电子,原子最外层电子数为1,常见化合价是+1,A项正确;B、若Y为Al,与冷水不反应,B项错误;C、由电离能数据可知,X可失去1个电子,原子最外层电子数为1,常见化合价是+1,元素X与氯形成化合物时,化学式可能是XCl,C项正确;D、Y可失去3个电子,原子最外层有3个电子,是ⅢA族元素,D项正确;答案选B。
考点:考查元素性质
【题型】选择题
【适用】较易
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】电子层数相同的三种元素X、Y、Z,已知最高价氧化物对应水化物的酸性HXO4 、H2YO4、H3ZO4,则下列判断错误的是
A.原子半径X>Y>Z B.气态氢化物的稳定性HX>H2Y>ZH3
C.非金属性X>Y>Z D.气态氢化物的还原性HX<H2Y<ZH3
【答案】A
【解析】
非金属性越强,最高价氧化物对应水化物的酸性越强,最高价氧化物对应水化物的酸性是:HXO4>H2YO4>H3ZO4,则非金属性X>Y>Z,A、同周期元素的原子从左到右,原子半径逐渐减小,非金属性增强,所以原子半径:X<Y<Z,A项错误;B、非金属性越强,氢化物越稳定,由于非金属性X>Y>Z,所以气态氢化物的稳定性:HX>H2Y>ZH3,B项正确;C、非金属性越强,最高价氧化物对应水化物的酸性越强,最高价氧化物对应水化物的酸性是:HXO4>H2YO4>H3ZO4,则非金属性X>Y>Z,C项正确;D、元素非金属性越强,阴离子的还原性越弱,由于非金属性X>Y>Z,所以气态氢化物的还原性HX<H2Y<ZH3,D项正确;答案选A。
考点:考查非金属强弱判断
【题型】选择题
【适用】一般
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】现有四种元素的基态原子的电子排布式如下:① [Ne]3s23p4; ②1s22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是
A.最高正化合价:③>②>① B.第一电离能:③>②>①
C.电负性:③>②>① D.原子半径:③>②>①
高二化学选择题中等难度题查看答案及解析
-
基态原子的核外电子排布为[Kr]4d55s2的元素属于的区、周期和族为( )
A.p区、第五周期、ⅠB族 B.d区、第五周期、ⅦB族
C.d区、第四周期、ⅠB族 D.ds区、第五周期、ⅠB族
高二化学选择题简单题查看答案及解析
-
【答案】B
【解析】
因为核外电子排布为[Kr]4d105s1的故为第五周期、ⅠB族,价电子轨道是sd,故为ds区,B项正确;答案选B。
考点:考查原子排布
【题型】选择题
【适用】较易
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】已知X、Y是主族元素,I为电离能,单位kJ/mol。根据下表所列数据判断错误的是
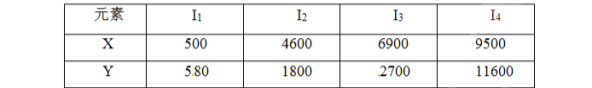
A.元素X的常见化合物价是+1价
B.若元素Y处于第3周期,它可与冷水剧烈反应
C.元素X与氯形成化合物时,化学式可能是XCl
D.元素Y是ⅢA族的元素
【答案】B
【解析】
A、由电离能数据可知,X可失去1个电子,原子最外层电子数为1,常见化合价是+1,A项正确;B、若Y为Al,与冷水不反应,B项错误;C、由电离能数据可知,X可失去1个电子,原子最外层电子数为1,常见化合价是+1,元素X与氯形成化合物时,化学式可能是XCl,C项正确;D、Y可失去3个电子,原子最外层有3个电子,是ⅢA族元素,D项正确;答案选B。
考点:考查元素性质
【题型】选择题
【适用】较易
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】电子层数相同的三种元素X、Y、Z,已知最高价氧化物对应水化物的酸性HXO4 、H2YO4、H3ZO4,则下列判断错误的是
A.原子半径X>Y>Z B.气态氢化物的稳定性HX>H2Y>ZH3
C.非金属性X>Y>Z D.气态氢化物的还原性HX<H2Y<ZH3
【答案】A
【解析】
非金属性越强,最高价氧化物对应水化物的酸性越强,最高价氧化物对应水化物的酸性是:HXO4>H2YO4>H3ZO4,则非金属性X>Y>Z,A、同周期元素的原子从左到右,原子半径逐渐减小,非金属性增强,所以原子半径:X<Y<Z,A项错误;B、非金属性越强,氢化物越稳定,由于非金属性X>Y>Z,所以气态氢化物的稳定性:HX>H2Y>ZH3,B项正确;C、非金属性越强,最高价氧化物对应水化物的酸性越强,最高价氧化物对应水化物的酸性是:HXO4>H2YO4>H3ZO4,则非金属性X>Y>Z,C项正确;D、元素非金属性越强,阴离子的还原性越弱,由于非金属性X>Y>Z,所以气态氢化物的还原性HX<H2Y<ZH3,D项正确;答案选A。
考点:考查非金属强弱判断
【题型】选择题
【适用】一般
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】现有四种元素的基态原子的电子排布式如下:① [Ne]3s23p4; ②1s22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是
A.最高正化合价:③>②>① B.第一电离能:③>②>①
C.电负性:③>②>① D.原子半径:③>②>①
【答案】B
【解析】
由四种元素基态原子电子排布式可知,①[Ne]3s23p4是S元素、②1s22s22p63s23p3是P元素、;③1s22s22p5是F元素,A、F无最高正化合价,A项错误;B、第一电离能:③>②>①,B项正确;C、电负性:③>①>②,C项错误;D、原子半径:②>①>③,D项错误;答案选B。
考点:考查核外电子排布
【题型】选择题
【适用】一般
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】下列说法中正确的是
A.基态原子是处于最低能量状态的原子
B.基态C原子的电子排布式是1s22s12p3
C.焰色反应是金属原子的电子从基态跃迁到激发态时产生的光谱
D.同一原子处于激发态时的能量一定低于基态时的能量
高二化学选择题简单题查看答案及解析
-
【答案】B
【解析】
因为核外电子排布为[Kr]4d105s1的故为第五周期、ⅠB族,价电子轨道是sd,故为ds区,B项正确;答案选B。
考点:考查原子排布
【题型】选择题
【适用】较易
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】已知X、Y是主族元素,I为电离能,单位kJ/mol。根据下表所列数据判断错误的是

A.元素X的常见化合物价是+1价
B.若元素Y处于第3周期,它可与冷水剧烈反应
C.元素X与氯形成化合物时,化学式可能是XCl
D.元素Y是ⅢA族的元素
【答案】B
【解析】
A、由电离能数据可知,X可失去1个电子,原子最外层电子数为1,常见化合价是+1,A项正确;B、若Y为Al,与冷水不反应,B项错误;C、由电离能数据可知,X可失去1个电子,原子最外层电子数为1,常见化合价是+1,元素X与氯形成化合物时,化学式可能是XCl,C项正确;D、Y可失去3个电子,原子最外层有3个电子,是ⅢA族元素,D项正确;答案选B。
考点:考查元素性质
【题型】选择题
【适用】较易
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】电子层数相同的三种元素X、Y、Z,已知最高价氧化物对应水化物的酸性HXO4 、H2YO4、H3ZO4,则下列判断错误的是
A.原子半径X>Y>Z B.气态氢化物的稳定性HX>H2Y>ZH3
C.非金属性X>Y>Z D.气态氢化物的还原性HX<H2Y<ZH3
【答案】A
【解析】
非金属性越强,最高价氧化物对应水化物的酸性越强,最高价氧化物对应水化物的酸性是:HXO4>H2YO4>H3ZO4,则非金属性X>Y>Z,A、同周期元素的原子从左到右,原子半径逐渐减小,非金属性增强,所以原子半径:X<Y<Z,A项错误;B、非金属性越强,氢化物越稳定,由于非金属性X>Y>Z,所以气态氢化物的稳定性:HX>H2Y>ZH3,B项正确;C、非金属性越强,最高价氧化物对应水化物的酸性越强,最高价氧化物对应水化物的酸性是:HXO4>H2YO4>H3ZO4,则非金属性X>Y>Z,C项正确;D、元素非金属性越强,阴离子的还原性越弱,由于非金属性X>Y>Z,所以气态氢化物的还原性HX<H2Y<ZH3,D项正确;答案选A。
考点:考查非金属强弱判断
【题型】选择题
【适用】一般
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】现有四种元素的基态原子的电子排布式如下:① [Ne]3s23p4; ②1s22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是
A.最高正化合价:③>②>① B.第一电离能:③>②>①
C.电负性:③>②>① D.原子半径:③>②>①
【答案】B
【解析】
由四种元素基态原子电子排布式可知,①[Ne]3s23p4是S元素、②1s22s22p63s23p3是P元素、;③1s22s22p5是F元素,A、F无最高正化合价,A项错误;B、第一电离能:③>②>①,B项正确;C、电负性:③>①>②,C项错误;D、原子半径:②>①>③,D项错误;答案选B。
考点:考查核外电子排布
【题型】选择题
【适用】一般
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】下列说法中正确的是
A.基态原子是处于最低能量状态的原子
B.基态C原子的电子排布式是1s22s12p3
C.焰色反应是金属原子的电子从基态跃迁到激发态时产生的光谱
D.同一原子处于激发态时的能量一定低于基态时的能量
【答案】A
【解析】
A、基态原子是处于最低能量状态的原子,A项正确;B、基态C原子的电子排布式是1s22s22p2,
B项错误;C、是金属原子电子受热激发后再回到较低能级时将多余能量以光能释放, C项错误;D、同一原子处于激发态时的能量一定大于基态时的能量,D项正确;答案选A。
考点:考查原子能量
【题型】选择题
【适用】较易
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】下列各项中的X和Y两种原子,化学性质一定相似的是
A.X原子和Y原子最外层都只有一个电子
B.X原子的核外电子排布为1s2,Y原子的核外电子排布为1s22s2
C.X原子的2p能级上有三个电子,Y原子的3p能级上有三个电子
D.X原子核外M层上仅有两个电子,Y原子核外N层上仅有两个电子
高二化学选择题中等难度题查看答案及解析
-
【答案】B
【解析】
因为核外电子排布为[Kr]4d105s1的故为第五周期、ⅠB族,价电子轨道是sd,故为ds区,B项正确;答案选B。
考点:考查原子排布
【题型】选择题
【适用】较易
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】已知X、Y是主族元素,I为电离能,单位kJ/mol。根据下表所列数据判断错误的是
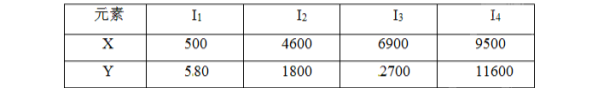
A.元素X的常见化合物价是+1价
B.若元素Y处于第3周期,它可与冷水剧烈反应
C.元素X与氯形成化合物时,化学式可能是XCl
D.元素Y是ⅢA族的元素
【答案】B
【解析】
A、由电离能数据可知,X可失去1个电子,原子最外层电子数为1,常见化合价是+1,A项正确;B、若Y为Al,与冷水不反应,B项错误;C、由电离能数据可知,X可失去1个电子,原子最外层电子数为1,常见化合价是+1,元素X与氯形成化合物时,化学式可能是XCl,C项正确;D、Y可失去3个电子,原子最外层有3个电子,是ⅢA族元素,D项正确;答案选B。
考点:考查元素性质
【题型】选择题
【适用】较易
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】电子层数相同的三种元素X、Y、Z,已知最高价氧化物对应水化物的酸性HXO4 、H2YO4、H3ZO4,则下列判断错误的是
A.原子半径X>Y>Z B.气态氢化物的稳定性HX>H2Y>ZH3
C.非金属性X>Y>Z D.气态氢化物的还原性HX<H2Y<ZH3
【答案】A
【解析】
非金属性越强,最高价氧化物对应水化物的酸性越强,最高价氧化物对应水化物的酸性是:HXO4>H2YO4>H3ZO4,则非金属性X>Y>Z,A、同周期元素的原子从左到右,原子半径逐渐减小,非金属性增强,所以原子半径:X<Y<Z,A项错误;B、非金属性越强,氢化物越稳定,由于非金属性X>Y>Z,所以气态氢化物的稳定性:HX>H2Y>ZH3,B项正确;C、非金属性越强,最高价氧化物对应水化物的酸性越强,最高价氧化物对应水化物的酸性是:HXO4>H2YO4>H3ZO4,则非金属性X>Y>Z,C项正确;D、元素非金属性越强,阴离子的还原性越弱,由于非金属性X>Y>Z,所以气态氢化物的还原性HX<H2Y<ZH3,D项正确;答案选A。
考点:考查非金属强弱判断
【题型】选择题
【适用】一般
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】现有四种元素的基态原子的电子排布式如下:① [Ne]3s23p4; ②1s22s22p63s23p3;③1s22s22p5。则下列有关比较中正确的是
A.最高正化合价:③>②>① B.第一电离能:③>②>①
C.电负性:③>②>① D.原子半径:③>②>①
【答案】B
【解析】
由四种元素基态原子电子排布式可知,①[Ne]3s23p4是S元素、②1s22s22p63s23p3是P元素、;③1s22s22p5是F元素,A、F无最高正化合价,A项错误;B、第一电离能:③>②>①,B项正确;C、电负性:③>①>②,C项错误;D、原子半径:②>①>③,D项错误;答案选B。
考点:考查核外电子排布
【题型】选择题
【适用】一般
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】下列说法中正确的是
A.基态原子是处于最低能量状态的原子
B.基态C原子的电子排布式是1s22s12p3
C.焰色反应是金属原子的电子从基态跃迁到激发态时产生的光谱
D.同一原子处于激发态时的能量一定低于基态时的能量
【答案】A
【解析】
A、基态原子是处于最低能量状态的原子,A项正确;B、基态C原子的电子排布式是1s22s22p2,
B项错误;C、是金属原子电子受热激发后再回到较低能级时将多余能量以光能释放, C项错误;D、同一原子处于激发态时的能量一定大于基态时的能量,D项正确;答案选A。
考点:考查原子能量
【题型】选择题
【适用】较易
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】下列各项中的X和Y两种原子,化学性质一定相似的是
A.X原子和Y原子最外层都只有一个电子
B.X原子的核外电子排布为1s2,Y原子的核外电子排布为1s22s2
C.X原子的2p能级上有三个电子,Y原子的3p能级上有三个电子
D.X原子核外M层上仅有两个电子,Y原子核外N层上仅有两个电子
【答案】C
【解析】
A、最外层都只有一个电子,例如H和Na,A项错误;B、X为He,Y为Be,两者性质不同,B项错误;C、X为N,Y为P,同主族元素性质相似,C项错误;D、X为Mg,Y的M层电子数不确定,元素种类很多,D项错误;答案选C。
考点:考查化学性质
【题型】选择题
【适用】一般
【标题】2015-2016学年吉林省汪清六中高二3月月考化学试卷(带解析)
【关键字标签】
【结束】下列关于元素电负性大小的比较中,不正确的是
A.O<S<Se<Te B.C<N<O<F
C.P<S<O<F D.K<Na<Mg<Al
高二化学选择题中等难度题查看答案及解析
-
下列说法正确的是( )
A. 电子云表示电子在原子核外运动的轨迹
B. Fe3+的最外层电子排布式:3s23p63d5
C. 基态原子的核外电子排布为[Kr]4d105s1的元素属于d区
D. 基态铜原子的外围电子轨道表示式:

高二化学单选题中等难度题查看答案及解析
-
下列说法正确的是
A. 电子由低能级跃迁至较高能级时,可通过光谱仪直接摄取原子的发射光谱
B. 基态原子的核外电子排布为[Kr]4d105s1的元素属于d区
C. NH3和CH4的中心原子都是sp3杂化
D. SO2和CO2都是直线形分子,其中心原子都是sp杂化
高二化学单选题简单题查看答案及解析