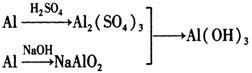-
(12分)目前,全世界镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍行业发展蕴藏着巨大潜力。
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于
晶体;Ni元素在元素周期表中的位置是第 周期,第 族;镍有 Ni和 Ni两种原子,它们互称为 。
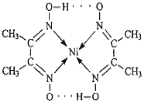
(2)如图所示配合物分子内的作用力有 (填编号)。
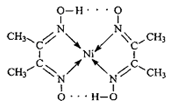
A.氢键
B.离子键
C.共价键
D.金属键
E.配位键
(3)很多不饱和有机物在Ni催化下可以与H2发生加成反应。
如①CH2=CH2、②CH≡CH、③ 、④HCHO等,其中分子属于平面结构的有 (填物质序号),预测HCHO分子的立体结构为 形。
、④HCHO等,其中分子属于平面结构的有 (填物质序号),预测HCHO分子的立体结构为 形。
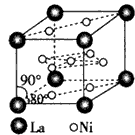
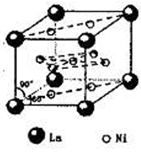
(4)氢气是新型清洁能源,镧(La)和镍(Ni)的合金可做储氢材料。该合金的晶胞如图所示,晶胞中心有一个镍原子,其他镍原子都在晶胞面上,镧原子都在晶胞顶点上。该晶体的化学式为 。
-
(8分)目前,全世界镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位。镍行业发展蕴藏着巨大潜力。
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于________晶体;基态Ni原子的电子排布式为________。
(2)下图中配合物分子内的作用力有________(填编号)。
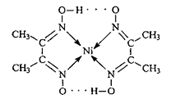
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键
(3)很多不饱和有机物在Ni催化下可以与H2发生加成反应。如
 ①CH2=CH2、 ②CH≡CH、 ③ 、④HCHO等,其中分子属于平面结构的有
①CH2=CH2、 ②CH≡CH、 ③ 、④HCHO等,其中分子属于平面结构的有
________(填物质序号),预测HCHO分子的立体结构为________形。
(4)氢气是新型清洁能源,镧(La)和镍(Ni)的合金可做储氢材料。该合金的晶胞如图所示,晶胞中心有一个镍 原子,其他镍原子都在晶胞面上,镧原子都在晶胞顶点上。该晶体的化学式为________。
-
有色金属行业发展蕴藏着巨大潜力。目前,全世界消费量排在前五位为铜、铝、铅、锌、镍。
(1)配合物Ni(CO)4常温下为液态,易溶于CCl4、苯等有机溶剂。固态Ni(CO)4属于___晶体;基态Ni原子的价电子电子排布式为____。
(2)铜原子的电子占有____种能量不同的原子轨道。
(3)配合物分子内(如图)的作用力有_____(填编号)。
A.氢键 B.离子键 C.共价键 D.金属键 E.配位键
(4)很多不饱和有机物在Ni催化下可以与H2发生加成反应。如 ①CH2=CH2、②CH≡CH、③ 、④HCHO等,其中分子中C原子为SP2杂化的有____(填物质序号),预测HCHO分子的立体结构为_____形。
、④HCHO等,其中分子中C原子为SP2杂化的有____(填物质序号),预测HCHO分子的立体结构为_____形。
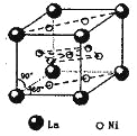
(5)氢气是新型清洁能源,镧(La)和镍(Ni)的合金可做储氢材料。该合金的晶胞如右图所示,晶胞中心有一个镍原子,其他镍原子都在晶胞面上,镧原子都在晶胞顶点上。该晶体的化学式为______。
(6)邻羟基苯甲醛的沸点____(填大于,小于或等于)对羟基苯甲醛的沸点。
-
铝是国民经济发展的重要材料,铝在地壳中的含量约占8%,目前我国铝消费量超过430万吨,在众多的金属中仅次于铁。请回答下问题:
(I )实验室中用金属铝制备少量氢氧化铝,有以下3种方案:
方案1:
方案3 :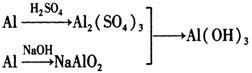
制备相同物质的量的氢氧化铝消耗酸和碱最少的是方案_____________________。
(II)工业上冶炼铝的流程图如图所示:
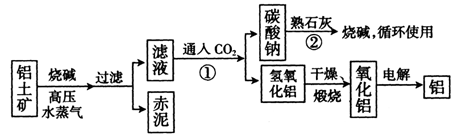
在制取氧化铝的过程中,分析铝土矿和赤泥中所含Al2O3、Fe203质量分数的数据如下:
| Al2O3 | Fe2O3 | 其他杂质 |
| 铝土矿 | 55% | 16% | — |
| 赤泥 | 15% | 48% | 一 |
(1) 书写化学方程式,反应①_______________,
反应②________________________
(2) 电解氧化铝生产铝时,阳极的电极反应式为_____________________。
(3) 假设其它杂质不参加反应,则每生产3.4t纯净的氧化铝,需铝土矿________________t
-
(9分)镁是一种轻金属,其合金强度高、机械性能好。这些特性使金属镁成为制造汽车、飞机、火箭的重要材料,从而获得”国防金属”的美誉。海水矿物质中镁的浓度仅次于氯和钠,居第三位。由于对镁的需求非常巨大,很多沿海国家都建有大型海水提镁工厂。
下表是有关物质的K :
:
回答下列问题:
(1)能否直接把贝壳研磨成粉末,撒入海水中使 转化为
转化为 沉淀,并解释原因:。
沉淀,并解释原因:。
(2)实际生产中是把 转化为
转化为 沉淀,而不是转化为
沉淀,而不是转化为 沉淀,其理由是;请你推测应将贝壳进行怎样的加工处理。
沉淀,其理由是;请你推测应将贝壳进行怎样的加工处理。
(3)某同学在实验室条件下模拟该生产过程,在加试剂时,误将纯碱溶液加入海水中,他思考了一下,又在得到的混合体系中加入过量的烧碱溶液,你觉得他________(填”能”或”不能”)将 转化为
转化为 沉淀,理由是。
沉淀,理由是。
-
铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制造、国防等领域。回答下列问题:
(1)用晶体的X射线衍射法可以测得阿伏加德罗常数。对金属铜的测定得到以下结果:晶胞为面心立方最密堆积,边长为361 pm。又知铜的密度为9.00 g·cm-3,阿伏加德罗常数为__________ (列式计算,已知Ar(Cu)=63.6);
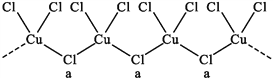
(2)氯和钾与不同价态的铜可生成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子均为无限长链结构(如下图),a位置上Cl原子的杂化轨道类型为______。已知其中一种化合物的化学式为KCuCl3,另一种的化学式为_______;
(3)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应,其原因是___________,反应的化学方程式为______________。
-
铜在我国有色金属材料的消费中仅次于铝,广泛地应用于电气、机械制造、国防等领域.一项科学研究成果表明,铜锰氧化物(CuMn2O4)能在常温下催化氧化空气中的一氧化碳和甲醛(HCHO)。
(1)Cu+基态的电子排布式可表示为____________。
(2)1mol甲醛(HCHO)中含有的σ键数目为______________。
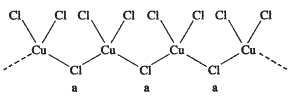
(3)氯和钾与不同价态的铜可生成两种化合物,这两种化合物都可用于催化乙炔聚合,其阴离子均为无限长链结构(如图),a位置上Cl原子的杂化轨道类型为______________。这两种不同化合物的化学式分别为________________、_______________。
(4)金属铜单独与氨水或单独与过氧化氢都不能反应,但可与氨水和过氧化氢的混合溶液反应生成铜氨离子Cu(NH3)42+,①反应的离子方程式为_________;②[Cu(NH3)4]2+中存在的化学键类型有_______(填序号)。
A.配位键 B.离子键 C.极性共价键 D.非极性共价键
(5)金属铍与氯气也可以形成化合物,在气态二氯化铍中有单体BeCl2和二聚体(BeCl2)2;在晶体中变形成多聚体(BeCl2)n。试画出各种存在形式的结构式,并指出对应Be原子的杂化轨道类型。
结构式_________杂化轨道类型________
结构式_________杂化轨道类型________
结构式_________杂化轨道类型________
-
海洋中蕴藏着巨大的化学资源。下列有关海水综合利用的说法正确的是
A. 蒸发海水可以生产单质碘 B. 蒸馏海水可以得到淡水
C. 电解海水可以得到单质镁 D. 电解海水可以制得金属钠
-
氢能是极具发展潜力的清洁能源,氢气的开发和综合利用是目前全球重要的科研项目之一。回答下列问题:
(1)T℃时,向体积均为1L的甲、乙两个恒容容器中分别加入足量碳和0.1molH2O(g),发生反应:H2O(g)+C(s)⇌CO(g)+H2(g) △H>0。甲容器控制绝热条件,乙容器控制恒温条件,两容器中压强随时间的变化如图所示。
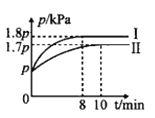
①图中代表甲容器的曲线为__(填“Ⅰ”或“Ⅱ”)。
②下列关于甲容器反应体系的说法错误的是__。
A.当水蒸气的体积分数不再发生变化,反应达到平衡状态
B.从密闭容器中分离出部分固体碳,H2的体积分数减小
C.缩小容器体积,平衡逆向移动,平衡常数减小
D.向平衡体系中充入少量水蒸气,再次平衡后,容器中c(CO)增大
③乙容器中,从反应开始到达平衡,v(H2O)=__mol•L-l•min-l;T℃下,该反应的平衡常数Kp=___(用含p的代数式表示)。
(2)对于反应aA(g)+bB(g)⇌cC(g)+dD(g),速率方程v═kcm(A)•cn(B),k为速率常数(只受温度影响),m+n为反应级数。已知H2(g)+CO2(g)⇌CO(g)+H2O(g),CO的瞬时生成速率=kcm(H2)•c(CO2)2。一定温度下,控制CO2起始浓度为0.25mol•L-1,改变H2起始浓度,进行以上反应的实验,得到CO的起始生成速率和H2起始浓度呈如图所示的直线关系。
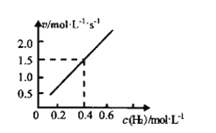
①该反应的反应级数为__。
②速率常数k=__。
③当H2的起始浓度为0.2mol•L-1,反应进行到某一时刻时,测得CO2的浓度为0.2mol•L-1,此时CO的生成瞬时速率v=__mol•L-l•s-1。
-
有机金属化合物的应用研究是目前科学研究的前沿之一。二茂铁[(C5H5)2Fe]的发现是有机金属化合物研究中具有里程碑意义的事件,它开辟了有机金属化合物研究的新领域。二茂铁分子是一种金属有机配合物,熔点173℃,沸点249℃,100℃以上能升华;不溶于水,易溶于苯、乙醚、汽油等有机溶剂。环戊二烯和二茂铁的结构如图所示。回答下列问题。


环戊二烯二茂铁
(1)环戊二烯分子中σ键和π键的个数比为___。
(2)下列关于环戊二烯和二茂铁的说法不正确的是__(填字母序号)。
A.环戊二烯分子中五个碳原子均发生sp2杂化
B.在一定的条件下,环戊二烯能与氢气发生加成反应生成环戊烷
C.二茂铁晶体是分子晶体
D.环戊二烯的同分异构体可能是含两个碳碳三键的炔烃
(3)环戊二烯能使溴的四氯化碳溶液褪色。写出环戊二烯与足量的溴的四氯化碳溶液反应的化学方程式___。
(4)已知环戊二烯阴离子(C5H5-)的结构与苯分子相似,具有芳香性。二茂铁[(C5H5)2Fe]晶体中存在的微粒间的作用力有___(填字母序号)。
a.离子键 b.σ键 c.π键 d.氢键 e.配位键
(5)金刚烷可用于抗病毒、抗肿瘤等特效药物的合成。工业上用环戊二烯合成金刚烷的流程如图所示:
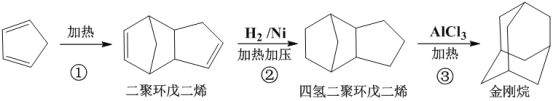
①金刚烷的分子式为____,反应①的反应类型是___。
②金刚烷的二氯代物有__种(不考虑立体异构)。
③二聚环戊二烯有多种同分异构体。写出符合下列条件的二聚环戊二烯的同分异构体的结构简式___。
(a)属于芳香烃且能使溴的四氯化碳溶液褪色;
(b)苯环上有三个取代基;
(c)苯环上的一氯代物有2种。

、④HCHO等,其中分子属于平面结构的有 (填物质序号),预测HCHO分子的立体结构为 形。