-
一位同学在复习时遇到这样一道习题:某无色溶液中可能含有“H+、OH-、Na+、NO3-”,加入铝粉后,只产生H2,问该无色溶液中能大量存在哪几种离子。
(1)加入铝粉产生H2,说明铝具有__________(填“氧化性”或“还原性”)。
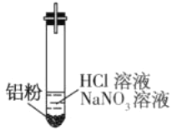
(2)该同学若H+大量存在,则NO3-就不能大量存在。 设计实验证实如下:
| 装 置 | 现 象 |
| 
| ⅰ. 实验初始,未见明显现象 ⅱ. 过一会儿,出现气泡,液面上方呈浅棕色 ⅲ. 试管变热,溶液沸腾 |
①盐酸溶解Al2O3薄膜的离子方程式是_______________________________。
②根据现象ⅱ,推测溶液中产生了NO,为进一步确认,进行如下实验:
| 实 验 | 内 容 | 现 象 |
| 实验1 | 将湿润KI—淀粉试纸置于空气中 | 未变蓝 |
| 实验2 | 用湿润KI—淀粉试纸检验浅棕色气体 | 试纸变蓝 |
a.浅棕色气体是____________。
b.实验1的目的是_______________________________。
c.实验1、2说明反应生成了NO,将生成NO的离子方程式补充完整:
______Al +______NO3- +_____ _ ==______Al 3++______NO +______ ,_______
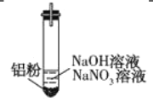
(3)再假设:若OH-大量存在,NO3-也可能不能大量存在。重新设计实验证实如下:
| 装 置 | 现 象 |
| 
| ⅰ. 实验初始,未见明显现象 ⅱ. 过一会儿,出现气泡,有刺激性气味 |
为确认“刺激性气味”气体,进行如下实验:用湿润KI—淀粉试纸检验,未变蓝;用湿润红色石蕊试纸检验,试纸变蓝。
①刺激性气味的气体是____________。
②产生该气体的离子方程式是____________________________________。
(4)在NaOH溶液中加入铝粉,结果只检验出有H2生成,其化学方程式是_________________________________。
(5)实验结果证实:NO3-在酸、碱性环境中都有一定的氧化性,能氧化铝单质,产生含氮化合物。试题中的无色溶液一定能大量存在的是_______________。
-
(6分)某无色透明溶液中可能大量存在OH-、Cl-、Na+、Mg2+、Cu2+中的几种离子。
(1)不做任何实验就可以肯定原溶液中不存在的离子是_______。
(2)取少量原溶液加入铝粉有气体放出,说明原溶液中肯定存在的离子是___________,有关的离子方程式为:____________________________。
(3)另取少量原溶液加入过量稀硝酸,再加几滴AgNO3溶液,出现白色沉淀,说明原溶液中肯定存在的离子有_________。
(4)原溶液中_________(填“肯定存在” 、“肯定不存在”或 “无法确定”) Na+。
-
下列各组离子在常温下一定能大量共存的是
A. 无色透明的溶液中:Na+、Ba2+、AlO2-、OH-
B. 加入铝粉能放出H2的溶液中:H+、K+、SO42-、 Cl-
C. 含有大量Fe3+的溶液中:NH4+、Ca2+、SCN-、Br-
D. pH=0的溶液中:Fe2+、Mg2+、 NO3-、SO42-
-
某无色溶液中,若加入溴水,溴水褪色,若加入NH4HCO3,固体溶解并产生刺激性气味的气体,则该溶液中可能大量存在的离子组是( )
A. Na+、K+、Cl-、OH- B. Na+、Mg2+、S2-、ClO-
C. H+、Na+、SO42-、NO3- D. K+、Ca2+、OH-、SO32-
-
某无色溶液中,若加入溴水,溴水褪色,若加入NH4HCO3,固体溶解并产生刺激性气味的气体,则该溶液中可能大量存在的离子组是
A.Na+、K+、Cl-、OH- B.H+、Na+、SO42-、NO3-
C.K+、Ca2+、NO3-、SO32- D.Na+、Mg2+、S2-、MnO4-
-
下列各组离子在指定的环境中能大量存在的是 ( )
A.pH=1的无色溶液中:SO42-、Cu2+、Na+、Cl-
B.能使酚酞试液变红色的溶液中:Na+、K+、S2-、CO32-
C.加入铝粉能产生H2的溶液中:NH4+、Na+、Fe2+、NO3-
D.水电离出的c(H+)=1×10-12mol/L的溶液中:K+、Na+、Cl-、HCO3-
-
下列各组离子在指定的环境中能大量存在的是
A.pH=1的无色溶液中:SO42—、Cu2+、Na+、Cl—
B.能使石蕊试纸变蓝色的溶液中:Na+、K+、S2—、CO32—
C.加入铝粉能产生H2的溶液中:NH4+、Na+、Fe2+、NO3—
D.水电离出的c(H+)=1×10-12mol/L的溶液中:K+、Na+、Cl-、HCO3—
-
下列各组离子在指定的环境中一定能大量存在的是
A.在pH=1的无色溶液中:SO42-、Cu2+、Na+、Cl-
B.在能使紫色石蕊试纸变蓝色的溶液中:Na+、K+、S2-、CO32-
C.在加入铝粉能产生H2的溶液中:NH4+、Na+、Fe3+、NO3-
D.由水电离出的c(H+)=1×10-12 mol·L-1的溶液中:K+、Na+、Cl-、CO32-
-
下列各组离子在给定条件的溶液中可能大量共存的是 ( )
A.加入铝粉有大量氢气产生的溶液中:Mg2+、K+、NO3-、C1-
B.PH = 0的无色溶液中:Na+、K+、MnO4-、NO3-
C.在0.1mol/L的醋酸溶液中:Fe2+、Na+、ClO-、Ca2+
D.在c(OH-)= 1×10-13的溶液中:NH4+、Ca2+、C1-、K+
-
下列各组离子在指定溶液中一定能大量共存的是( )
A. 加入铝粉能产生氢气的溶液:NH4+、K+、HCO3-、Br-
B. 含有KSCN的溶液: Na+、Fe3+、SO32-、OH-
C. c(KNO3)为 1.0 mol • L-1 的溶液: H+、Fe2+、C1-、SO42-
D. pH=14的溶液:Na+、K+、NO3- 、AlO2-
 ,加入铝粉后,只产生H2,为探究该溶液中存在的离子,某学习小组进行了如下实验。
,加入铝粉后,只产生H2,为探究该溶液中存在的离子,某学习小组进行了如下实验。 就不能大量存在”,设计实验证实如下:
就不能大量存在”,设计实验证实如下: 也可能不大量存在”,重新设计实验证实如下:
也可能不大量存在”,重新设计实验证实如下: