-
氮及其化合物在化肥、医药、材料和国防工业中具有广泛应用。回答下列问题:
(1)自上个世纪德国建立了第一套合成氨装置,合成氨工业为解决人类的温饱问题作出了极大贡献。写出实验室制备氨气的方程式_________。
(2)有人设想寻求合适的催化剂和电极材料,以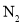 、
、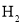 为电极反应物,以
为电极反应物,以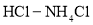 为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型燃料电池,如图所示。
为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型燃料电池,如图所示。
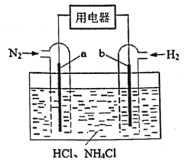
①a电极是该电池的_______(填正极或者负极);该电池正极的电极反应式是___________。
②该电池在工作过程中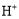 的浓度将不断_________(填增大或减小),假设放电过程中电解质溶液的体积不变,当溶液中
的浓度将不断_________(填增大或减小),假设放电过程中电解质溶液的体积不变,当溶液中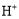 的物质的量改变
的物质的量改变 时,理论上电池能为外电路提供___________mol电子。
时,理论上电池能为外电路提供___________mol电子。
(3)肼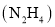 又称为联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池以20%~30%的
又称为联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池以20%~30%的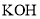 溶液为电解质溶液,总反应方程式为:
溶液为电解质溶液,总反应方程式为: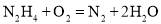 。请写出该电池放电时,负极的电极反应式:__________。
。请写出该电池放电时,负极的电极反应式:__________。
(4)为了监测空气中NOx的含量,科学家成功研制出了一种NOx传感器,其工作原理示意图如图:
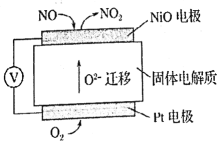
①固体电解质中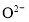 移向___________(填“正极”或“负极”)
移向___________(填“正极”或“负极”)
②写出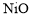 电极发生的电极反应式:________。
电极发生的电极反应式:________。
-
2013年H7N9禽流感肆虐期间为了保证卫生环境,常使用漂白液和漂白粉对环境和饮用水进行杀菌、消毒,以抑制大规模传染病爆发。钠、镁及其化合物在工业中具有广泛的应用。回答下列问题:
⑴写出钠与水反应的化学方程式____________________
⑵写出镁与二氧化碳反应的化学方程式___________________
⑶漂白粉溶于水后,与空气中CO2发生反应,即产生有漂白、杀菌作用的次氯酸,化学反应方程式为__________________
⑷某研究性学习小组对漂白液进行了如下实验探究:取漂白液少量,滴入3~5滴紫色石蕊试液,发现溶液先变蓝色后褪色,可以证明漂白液具有的性质 (填序号)。
A.酸性  B.碱性 C.漂白性
B.碱性 C.漂白性
-
锶被广泛应用于电子、化工、冶金、轻工、医药和光学等领域.下列关于锶(Sr)元素单质及其化合物的叙述中不正确的是( )
A. 锶(Sr)位于周期表中第5周期第IIA族
B. 金属锶单质呈银白色,具有良好的导电性
C. 氢氧化锶碱性弱于氢氧化镁的碱性
D. 硝酸锶是离子化合物,易溶于水
-
硫和氮及其化合物在生产生活中应用广泛。请回答:
(1)已知反应:3NO2+H2O=2HNO3+NO,该反应中的氧化剂与还原剂的质量比为_____。
(2)工业上可以通过氮气和氢气在一定条件下合成氨气。下列关于氨气的性质和用途描述正确的是____________。
A. 氨气易液化,液氨可作制冷剂 B. 可用排水法收集氨气
C. 氨气是一种无色无味的气体 D. 向氨水中滴加酚酞,溶液变红
(3)1754年,Briestly用硵砂(主要成份NH4Cl)和熟石灰共热制得了氨,化学反应方程式为______________________________。
(4)实验室用金属铜和稀硝酸制取NO的离子方程式为_____________。
(5)汽车尾气常含有NO、NO2、CO等,会污染空气。在汽车尾气排放管处安装一个催化转化器,可使尾气中有害气体CO和NO反应转化为两种无毒气体,该反应的化学方程式为__________________________。
(6)19.2 g铜投入100 mL 14 mol/L浓HNO3溶液中,充分反应后无固体剩余,收集到标准状况下气体8.96 L(气体为NO、NO2),向反应后的溶液中加入______mL 10 mol/L NaOH溶液才能使Cu2+完全沉淀。
-
硫和氮及其化合物在生产生活中应用广泛。请回答:
(1)已知反应:3NO2+H2O=2HNO3+NO,该反应中的氧化剂与还原剂的质量比为_____。
(2)工业上可以通过氮气和氢气在一定条件下合成氨气。下列关于氨气的性质和用途描述正确的是____________。
A. 氨气易液化,液氨可作制冷剂 B. 可用排水法收集氨气
C. 氨气是一种无色无味的气体 D. 向氨水中滴加酚酞,溶液变红
(3)1754年,Briestly用硵砂(主要成份NH4Cl)和熟石灰共热制得了氨,化学反应方程式为______________________________。
(4)实验室用金属铜和稀硝酸制取NO的离子方程式为_____________。
(5)汽车尾气常含有NO、NO2、CO等,会污染空气。在汽车尾气排放管处安装一个催化转化器,可使尾气中有害气体CO和NO反应转化为两种无毒气体,该反应的化学方程式为__________________________。
(6)19.2 g铜投入100 mL 14 mol/L浓HNO3溶液中,充分反应后无固体剩余,收集到标准状况下气体8.96 L(气体为NO、NO2),向反应后的溶液中加入______mL 10 mol/L NaOH溶液才能使Cu2+完全沉淀。
-
氮元素在生命活动中扮演着十分重要的角色,回答下列与氮及其化合物有关的问题.
Ⅰ.为了提高农作物的产量,德国化学家哈伯、波施等科学家成功地开发了将氮气转化为氨气的生产工艺.请用化学方程式表示工业合成氨的反应原理______高温高压2NH3
-
氮及其化合物在生产生活中应用广泛。回答下列问题:
(1)“中国制造2025”是中国政府实施制造强国战略第一个十年行动纲领。氮化铬(CrN)具有极高的硬度和力学强度、优异的抗腐蚀性能和高温稳定性能,氮化铬在现代工业中发挥更重要的作用,请写出Cr3+的外围电子排布式___;基态铬、氮原子的核外未成对电子数之比为___。
(2)过硫酸铵[(NH4)2S2O8],广泛地用于蓄电池工业、石油开采、淀粉加工、油脂工业、照相工业等,过硫酸铵中N、S、O的第一电离能由大到小的顺序为___,过硫酸铵的阳离子的空间构型为___。
(3) 是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由
是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由 和[Co(NH3)5H2O](ClO4)3反应合成的,
和[Co(NH3)5H2O](ClO4)3反应合成的,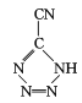 中孤电子对与π键比值为__,CP的中心Co3+的配位数为___。
中孤电子对与π键比值为__,CP的中心Co3+的配位数为___。
-
硅和氮均是自然界含量丰富的元素,其单质及其化合物在环境、能源及材料科学中有着重要影响和广泛应用.试回答下列问题:
(1) 向大气中排放NOx可能导致的环境问题有________.(答两点)已知足量NaOH溶液能完全吸收NO2生成氮的两种含氧酸盐(氮为+3、+5价).试写出该反应的离子方程式________ .
(2) 光导纤维的作用,让人们的生活更加丰富精彩,________是制备光导纤维的基本原料.
(3) 氮化硅陶瓷是一种新型无机非金属材料,其化学式为________, 可由硅粉(用Al2O3和Y2O3作助剂)在氮气中高温烧结而成,氮气在反应中既是反应物,同时又起了
________作用.由于使用的硅粉表面含二氧化硅,在反应中需加入碳粉.在烧结过程中,二氧化硅、碳、氮气以物质的量之比3∶6∶2反应生成两 种化合物,该反应的化学方程式为________.
(4) 硅燃烧放出大量热量,“硅能源”有望成为二十一世纪的新能源.与“氢能源”比较“硅能源”具有________等更加优越的特点,从而得到全球的关注和期待.
-
铁及其化合物[如FeCl3,Fe(OH)3,Na2FeO4等]在生产、生活中应用广泛,请结合所学知识,回答问题:
(1)电子工业需用30%的FeCl3溶液腐蚀敷在绝缘板上的铜箔,制造印刷电路板,检验FeCl3溶液中Fe3+存在的常用试剂是_______。FeCl3溶液腐蚀敷在绝缘板上的铜箔反应的离子方程式为________________,欲从腐蚀后的废液中回收Cu并重新获得FeCl3溶液,现有下列试剂①氯气②铁粉③浓硫酸④盐酸⑤烧碱⑥氨水,请选择试剂______,写出反应的离子方程式:废液中回收Cu_________;废液重新获得FeCl3溶液_________。
(2)沸水中逐滴加入1mol/L FeCl3溶液,继续加热至溶液呈透明的红褐色,该反应的化学方程式为____,该分散系中分散质的微粒直径为____ nm。
(3)高铁酸钠Na2FeO4是一种新型净水剂,可以通过如下反应制得2Fe(OH)3+3NaClO+4NaOH=2Na2FeO4+3X+5H2O,X的化学式为____,从化合价升降角度考虑,高铁酸钠能够杀菌是因为它具有____性。
-
铝、铁、硅的单质及化合物在工业生产中具有广泛应用,工业上常用某矿石(主要成分有Al2O3、Fe2O3、FeO、SiO2等)来制备绿矾(FeSO4·7H2O)和氧化铝,其工艺流程如图:

回答下列问题:
(1)滤渣1的成分是___,举例说明滤渣2的用途___。
(2)用离子方程式表示溶液A加入过量铁粉的目的是___。
(3)写出由滤液1生成滤液2的离子方程式___。
(4)过程1、2、3均涉及分离操作,所需玻璃仪器有___。
(5)由溶液B得到绿矾的具体操作为___、过滤、洗涤和干燥。
(6)过程3需要加入的试剂A是___,写出此过程的离子方程式___。
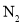 、
、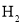 为电极反应物,以
为电极反应物,以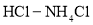 为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型燃料电池,如图所示。
为电解质溶液制造出一种既能提供电能,又能实现氮固定的新型燃料电池,如图所示。
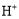 的浓度将不断_________(填增大或减小),假设放电过程中电解质溶液的体积不变,当溶液中
的浓度将不断_________(填增大或减小),假设放电过程中电解质溶液的体积不变,当溶液中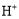 的物质的量改变
的物质的量改变 时,理论上电池能为外电路提供___________mol电子。
时,理论上电池能为外电路提供___________mol电子。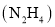 又称为联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池以20%~30%的
又称为联氨,是一种可燃性的液体,可用作火箭燃料。肼-空气燃料电池以20%~30%的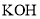 溶液为电解质溶液,总反应方程式为:
溶液为电解质溶液,总反应方程式为: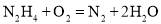 。请写出该电池放电时,负极的电极反应式:__________。
。请写出该电池放电时,负极的电极反应式:__________。
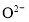 移向___________(填“正极”或“负极”)
移向___________(填“正极”或“负极”)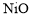 电极发生的电极反应式:________。
电极发生的电极反应式:________。 是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由
是20世纪80年代美国研制的典型钝感起爆药Ⅲ,它是由 和[Co(NH3)5H2O](ClO4)3反应合成的,
和[Co(NH3)5H2O](ClO4)3反应合成的, 中孤电子对与π键比值为__,CP的中心Co3+的配位数为___。
中孤电子对与π键比值为__,CP的中心Co3+的配位数为___。