反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如图甲所示:
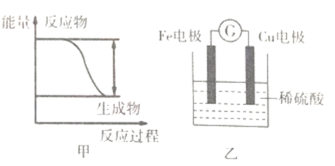
(1)该反应为______(填”吸热”或“放热”)反应。
(2)该反应____(填“是”或“否”)氧化还原反应;若将上述反应设计成原电池,装置如图乙,该装置工作时,电子沿导线流入_____(填“Cu”或“Fe”)电极,该电极为____(填“正”或“负”)极,电极反应式为____;若反应产生11.2L气体(标准状况下),则电路中应该有____mol电子发生了转移。
高一化学计算题简单题
反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如图甲所示:

(1)该反应为______(填”吸热”或“放热”)反应。
(2)该反应____(填“是”或“否”)氧化还原反应;若将上述反应设计成原电池,装置如图乙,该装置工作时,电子沿导线流入_____(填“Cu”或“Fe”)电极,该电极为____(填“正”或“负”)极,电极反应式为____;若反应产生11.2L气体(标准状况下),则电路中应该有____mol电子发生了转移。
高一化学计算题简单题
反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势,如图所示:
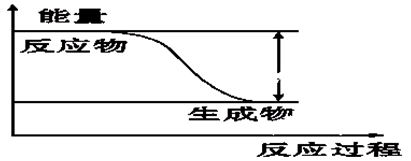
(1)该反应为 反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是 (填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜片上产生的现象为 。溶液中SO42-向 极(填“贴片”或“铜片”),外电路中电子 移动。(填“由铁片向铜片”或“由铜片向铁片”)。
高一化学填空题中等难度题查看答案及解析
反应Fe+H2SO4===FeSO4+H2↑的能量变化趋势,如图所示:
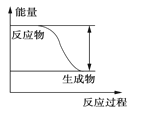
(1)该反应为________反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是_____(填字母)。
A.改铁片为铁粉 B.增大压强
C.升高温度 D.改稀硫酸为98%的浓硫酸
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为______极(填“正”或“负”)。铜片上产生的现象为________________;该极上发生的电极反应为______________;外电路中电子由 _______极向_______极移动。(填“正”或“负”)
高一化学填空题困难题查看答案及解析
反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势,如图所示:
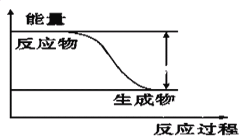
(1)该反应为______反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是______(填字母)。
A.改铁片为铁粉 B.增大压强 C.升高温度 D.将稀硫酸改为98%的浓硫酸
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为____极(填“正”或“负”)。铜片上产生的现象为______,该极上发生的电极反应为______。
高一化学综合题简单题查看答案及解析
反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如图所示:

(1)该反应为_____(填“吸热”或“放热”)反应。
(2)若要使该反应的反应速率加快,下列措施可行的是_____(填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为_____(填“正”或“负”)极。铜片上的现象为_____,该极上发生的电极反应为_____,外电路中电子由_____移动。(填“正极向负极”或“负极向正极”)
高一化学填空题简单题查看答案及解析
Ⅰ、反应Fe+H2SO4===FeSO4+H2↑的能量变化趋势,
如图所示:

(1)该反应为________反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是________(填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为_______极(填“正”或“负”); 铜电极上发生的电极反应为__________________。
Ⅱ、某温度时,在5 L的容器中,X、Y、Z三种气体的物质的量随时间的变化曲线如图所示。请通过计算回答下列问题:
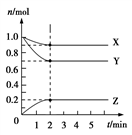
(4)反应开始至2 min,Y的平均反应速率________。
(5)分析有关数据,写出X、Y、Z的反应方程式______________________。
高一化学简答题困难题查看答案及解析
反应Fe+H2SO4===FeSO4+H2↑的能量变化趋势如下图所示:

(1)该反应为________反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是__________(填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为________极(填“正”或“负”)。铜电极上产生的现象为____________,该极上发生的电极反应为____________________,外电路中电子由____________极(填“正”或“负”,下同)向________极移动。
高一化学综合题中等难度题查看答案及解析
反应Fe+H2SO4=FeSO4+H2↑的能量变化趋势如下图所示:

(1)该反应为_______反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是_______(填字母)
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度 D.减小压强
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为_________极(填“正”或“负”)。铜片上产生的现象为_________,外电路中电子由________电极(填“Fe”或“Cu”,下同),向________电极移动。
(4)若依据氧化还原反应:Cu2++Fe=Cu+Fe2+设计的原电池如下图所示,请回答下列问题:
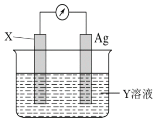
电极X的材料是________,电解质溶液Y是_________,X电极上发生的电极反应式为_________。
高一化学综合题中等难度题查看答案及解析
反应Fe+H2SO4===FeSO4+H2↑的能量变化趋势如下图所示:
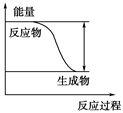
(1)该反应为________反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是__________(填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为________极(填“正”或“负”)。铜电极上产生的现象为____________,该极上发生的电极反应为____________________,外电路中电子由____________极(填“正”或“负”,下同)向________极移动。
高一化学简答题中等难度题查看答案及解析
反应Fe+H2SO4===FeSO4+H2↑的能量变化趋势如下图所示:

(1)该反应为________反应(填“吸热”或“放热”)。
(2)若要使该反应的反应速率加快,下列措施可行的是__________(填字母)。
A.改铁片为铁粉 B.改稀硫酸为98%的浓硫酸 C.升高温度
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为________极(填“正”或“负”)。铜电极上产生的现象为____________,该极上发生的电极反应为____________________,外电路中电子由____________极(填“正”或“负”,下同)向________极移动。
高一化学简答题中等难度题查看答案及解析
反应 Fe+H2SO4=FeSO4+H2↑的能量变化趋势如下图所示:
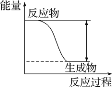
(1)该反应为___________________(填“吸热”或“放热”)反应。
(2)若要使该反应的反应速率加快,下列措施可行的是___________________(填字母)。
A.改铁片为铁粉 B.改稀硫酸为 98%的浓硫酸 C.升高温度 D.减小压强 E.加入少量的硝酸铜溶液 F.加入醋酸钠固体 G.加入氯化钠溶液
(3)若将上述反应设计成原电池,铜为原电池某一极材料,则铜为_________(填“正”或“负”)极。铜片上产生的现象为_____________________ , 该 极 上 发 生 的 电 极 反 应 为___________________________,外电路中电子由_____(填“正”或“负”,下同)极向_____________极移动。
(4)若将电解质溶液改为 FeCl3,则形成原电池的总反应式:__________________________。
高一化学综合题简单题查看答案及解析