-
(15分) 【化学 ― 选修 3 物质结构与性质】
氮的化合物在无机化工领域有着重要的地位。请回答下列问题:
(1)基态氮原子的价电子排布图为 。
(2)氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子的构型为 形,阳离子中氮的杂化方式为 。
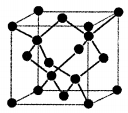
(3)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气、氧化铝和碳在一定条件下反应生成CO和X (X的晶体结构如图所示),工业制备 X 的化学方程式为 。
(4)X晶体中包含的化学键类型为 (填字母标号)。
A .离子键 B .共价键 C .配位键 D .金属键
(5)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,其原因 是 。
(6)若X的密度为ρg/cm3,则晶体中最近的两个Al 原子的距离为 cm (阿伏加德罗常数用 NA表示,不必化简)。
-
[化学——选修3物质结构与性质](15分)氮的化合物在无机化工领域有着重要的地位。请回答下列问题:
(1)基态氮原子的价电子排布图为______。氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子的构型为 形,阳离子中氮的杂化轨道类型为 。
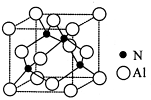
(2)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气与氧化铝和碳在一定条件下反应生成X和CO,X的晶体结构如图所示,工业制备X的化学方程式为_______。
(3)X晶体中包含的化学键类型为______。(填字母标号)
A.离子键 B.共价键 C.配位键 D.金属键
(4)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,可能的原因是______
(5)若X的密度为pg/cm3,则晶体中最近的两个N原子的距离为______cm(阿伏加德罗常数用NA表示,不必化简)。
-
【化学-物质结构与性质】氮的化合物在无机化工领域有着重要的地位。请回答下列问题:
(1)基态氮原子的价电子排布图为 。
(2)氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子的构型为 形,阳离子中氮的杂化方式为 。
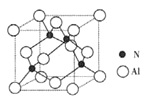
(3)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气、氧化铝和碳在一定条件下反应生成CO和X (X的晶体结构如图所示),工业制备 X 的化学方程式为 。
(4)X晶体中包含的化学键类型为 (填字母标号)。
A .离子键 B .共价键 C .配位键 D .金属键
(5)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,其原因是 。
(6)若X的密度为ρg/cm3,则晶体中最近的两个Al 原子的距离为 cm (阿伏加德罗常数用 NA表示,不必化简)。
-
【化学-物质结构与性质】氮的化合物在无机化工领域有着重要的地位。请回答下列问题:
(1)基态氮原子的价电子排布图为 。
(2)氮的最高价氧化物为无色晶体,它由两种离子构成:已知其阴离子构型为平面正三角形,则其阳离子的构型为 形,阳离子中氮的杂化方式为 。
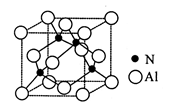
(3)某氮铝化合物X具有耐高温、抗冲击、导热性好等优良性质,广泛用于陶瓷工业等领域。工业上用氮气、氧化铝和碳在一定条件下反应生成CO和X (X的晶体结构如图所示),工业制备 X 的化学方程式为 。
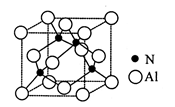
(4)X晶体中包含的化学键类型为 (填字母标号)。
A .离子键 B .共价键 C .配位键 D .金属键
(5)已知氮化硼与X晶体类型相同,且氮化硼的熔点比X高,其原因是 。
(6)若X的密度为ρg/cm3,则晶体中最近的两个Al 原子的距离为 cm (阿伏加德罗常数用 NA表示,不必化简)。
-
[化学——选修3:物质结构与性质](15分)
钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)元素K的焰色反应呈紫红色,其中紫色对应的辐射波长为_______nm(填标号)。
A.404.4 B.553.5 C.589.2 D.670.8 E.766.5
(2)基态K原子中,核外电子占据的最高能层的符号是_________,占据该能层电子的电子云轮廓图形状为___________。K和Cr属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Cr低,原因是___________________________。
(3)X射线衍射测定等发现,I3AsF6中存在I3+离子。I3+离子的几何构型为_____________,中心原子的杂化形式为________________。
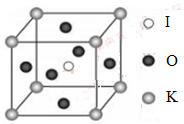
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立体结构,边长为a=0.446nm,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示。K与O间的最短距离为______nm,与K紧邻的O个数为__________。
(5)在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于______位置,O处于______位置。
-
[化学一选修3:物质结构与性质]
钾和碘的相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)元素K的焰色反应呈紫红色,其中紫色对立的辐射波长为_____________nm(填序号)。
A.589.2 B.500.3 C.650.2 D.434.4
(2) K和Fe属于同一周期,且核外最外层电子构型相同,但金属K的熔点、沸点等都比金属Fe低,原因是________________________。
(3) 基态I原子中,核外电子占据最高能层的符号为_____________________。
(4)KIO3晶体是一种性能良好的非线性光学材料,具有钙钛矿型的立方结构,边长a=0.446am,晶胞中K、I、O分别处于顶角、体心、面心位置,如图所示,K 与O间的最短距离为________nm,与K紧邻的O 个数为_____________________。
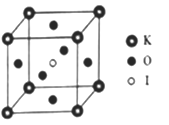
(5) 在KIO3晶胞结构的另一种表示中,I处于各顶角位置,则K处于________位置,O处于__________位置。
-
[物质结构与性质一选修3]
种类繁多的碳族元素的单质及其化合物,有着重要的研究价值。
(1)锗(Ge)的含量十分稀少,但它被广泛应用于电子、光学、化工、生物医学、能源及其他高新科技领域。
①现代化学中,常利用__________上的特征谱线来鉴定元素。基态锗原子中,核外能级最高的原子轨道上,具有的电子数为___________。
②通常状况下GeCl4是无色液体,易挥发,其熔点为-51.50C,沸点为86.55℃,能溶于乙醚。由此可推知GeCl4应属于共价化合物,其理由是_______,也即氯和锗两元素的电负性相差应该_______1.7(填“小于”或“大于”)。
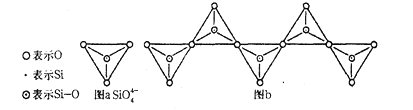
(2)在硅酸盐中, 如图a所示为四面体结构,它可以通过公用顶角0原子,形成链状层状、岛状和网状结构的不同硅酸盐。图b表示由n个四面体连接成的硅酸根,其中Si的杂化形式为_____,Si与O的原子个数比为________,化学式可表示为__________。
如图a所示为四面体结构,它可以通过公用顶角0原子,形成链状层状、岛状和网状结构的不同硅酸盐。图b表示由n个四面体连接成的硅酸根,其中Si的杂化形式为_____,Si与O的原子个数比为________,化学式可表示为__________。
(3)石墨晶体由层状石墨“分子”按ABAB方式堆积而成,如图(a)所示。图(b)是一个石墨的六方晶胞示意图。
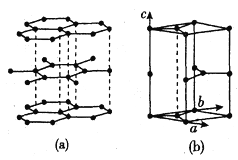
①请在图 中画出晶胞沿c轴的投影 (用“·”标出碳原子位置即可)_________。
中画出晶胞沿c轴的投影 (用“·”标出碳原子位置即可)_________。
②假设石墨晶胞高为h cm,C-C键长为r cm,则石墨晶体密度的表达式为__________g.cm-3(阿伏加德罗常数为NA)。
-
【化学一选修3:物质结构与性质】铜及其化合物在化工生产中有着广泛的应用。回答下列问题:
(1)铜元素在元素周期表中的位置为_________________,基态Cu原子核外电子占据的原子轨道数为____________________。
(2)向硫酸铜溶液中加入乙二胺(H2N-CH2-CH2-NH3)溶液后,每个Cu2+可与两个乙二胺分子形成四配位离子,导致溶液由蓝色变为紫色。
①乙二胺分子中C、N原子的杂化轨道类型分别为_______________、_________________。
②与硫酸根离子互为等电子体的分子为___________(任写一种)。
③四配位离子的结构式为_____________________,该离子中所有元素的电负性由大到小的顺序为____________________________。
(3)硫化亚铜和氧化亚铜均为离子晶体,其中熔点较高的为___________(填化学式),原因为________________________________________________。
(4)下图为铜与氧(O)、钇(Y)、钡(Ba)形成的一种超导体材料的长方体晶胞结构,其晶胞参数如图(i)所示,该结构中有平面正方形(CuO4)和四方锥(CuO6)结构单元如图(ii)所示。
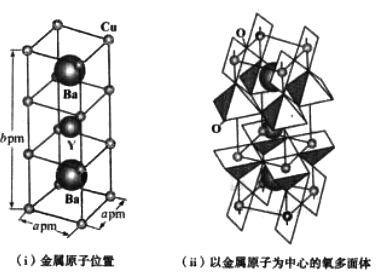
①该超导体材料的化学式为____________________________。
②已知该化合物的摩尔质量为Mg·mol-1,阿伏加德罗常数的值为NA,其密度为____g·cm-3(列出表达式即可)。
-
(化学——选修3:物质结构与性质)
镍及其化合物在工业生产和科研领域有重要的用途。请回答下列问题:
(1)基态 Ni 原子中,电子填充的能量最高的能级符号为______,价层电子排布式为________。
(2)Ni(CO)4 常用作制备高纯镍粉,其熔点为-19.3 ℃, 沸点为 43 ℃。则:
①Ni(CO)4 的熔、沸点较低的原因为________。
②写出一种与CO 互为等电子体的分子的化学式________。
③Ni(CO)4中 σ 键和 π 键的数目之比为________。
(3)NiSO4 常用于电镀工业,其中 SO42-的中心原子的杂化轨道类型为________,该离子中杂化轨道的作用是________。
(4)氧化镍和氯化钠的晶体结构相同,可看成镍离子替换钠离子,氧离子替换氯离子。 则:
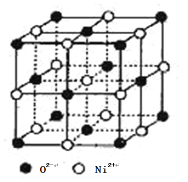
①镍离子的配位数为________。
②天然的和人工合成的氧化镍常存在各种缺陷,某缺陷氧化镍的组成为Ni0.97O(相对分子质量为73), 其中 Ni 元素只有+2 和+3 两种价态, 两种价态的镍离子数目之比为________;若阿伏加德罗常数的值为NA,晶体密度为 ρ g·cm-3,则该晶胞中最近的 O2-之间的距离为________pm(列出表达式)。
-
[化学——选修3:物质结构与性质](15分)硼(B)及其化合物在化学中有重要的地位。请回答下列问题:
(1)Ga与B同主族,Ga的基态原子核外电子排布式为 ,从原子结构的角度分析,B、N、O元素的第一电离能由大到小的顺序是 。
(2)硼酸(H3B03)是白色片状晶体(层状结构如图),有滑腻感,在冷水中溶解度很小,加热时溶解度增大。
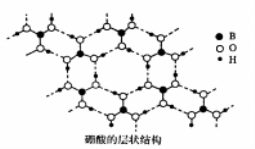
①硼酸中B原子的杂化轨道类型为 。
②硼酸晶体中存在的作用力有范德华力和 。
③加热时,硼酸的溶解度增大,主要原因是 。
④硼酸是一元弱酸,在水中电离时,硼酸结合水电离出的OHˉ而呈酸性。写出硼酸的电离方程式_ 。
(3)硼氢化钠(NaBH4)是有机化学中的一种常用还原剂,在热水中水解生成硼酸钠和氢气,用化学方程式表示其反应原理 。[BH4]-的空问构型是____。
(4)B3N3H6可用来制造具有耐油、耐高温性能的特殊材料。写出它的一种等电子体物质的分子式 。
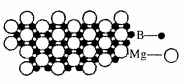
(5)硼化镁晶体在39K时呈超导性。在硼化镁晶体中,镁原子和硼原子是分层排布的,下图是该晶体微观结构的透视图,图中的硼原子和镁原子投影在同一平面上。则硼化镁的化学式为 。
(6)金刚石的晶胞如图。立方氮化硼的结构与金刚石相似,已知晶胞边长为361.5pm,则立方氮化硼的密度是____g·cmˉ3(只要求列算式,不必计算出数值,阿伏伽德罗常数用NA表示)。