目前废水处理中的除氮技术,通常是把水中的氨氮污染物先降解为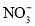 或
或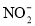 ,然后再用电解的方法除去
,然后再用电解的方法除去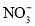 和
和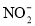 ,如图是电化学降解硝酸盐的原理,关于该原理的说法正确的是
,如图是电化学降解硝酸盐的原理,关于该原理的说法正确的是
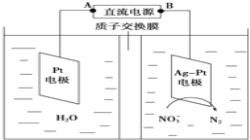
A.若以铅蓄电池做电源进行电解,Pt电极为阴极
B.电解过程中H+向左移动
C.理论上电解过程中阴、阳两极产生的气体在相同条件下体积比为2:5
D.若电解过程中转移1mol电子,则交换膜两侧电解液的质量变化差为7.4g
高二化学单选题中等难度题
目前废水处理中的除氮技术,通常是把水中的氨氮污染物先降解为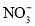 或
或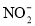 ,然后再用电解的方法除去
,然后再用电解的方法除去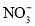 和
和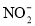 ,如图是电化学降解硝酸盐的原理,关于该原理的说法正确的是
,如图是电化学降解硝酸盐的原理,关于该原理的说法正确的是

A.若以铅蓄电池做电源进行电解,Pt电极为阴极
B.电解过程中H+向左移动
C.理论上电解过程中阴、阳两极产生的气体在相同条件下体积比为2:5
D.若电解过程中转移1mol电子,则交换膜两侧电解液的质量变化差为7.4g
高二化学单选题中等难度题
电化学降解法可用于治理水中硝酸盐的污染,其原理如图。下列说法不正确的是( )
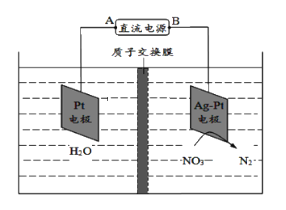
A.A为电源正极
B.在Pt电极上发生氧化反应
C.阴极的电极反应式为:2NO3- + 6H2O + 10e- = N2 + 12OH-
D.若电路转移10mol e-,质子交换膜右侧溶液质量减少18g
高二化学单选题中等难度题查看答案及解析
化学在环境保护中起着十分重要的作用,电化学降解法可用于治理水中硝酸盐的污染。电化学降解NO3-的原理图所示。下列说法不正确的是:
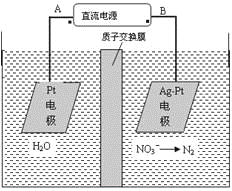
A.A为电源正极
B.阳极反应式为:2H2O-4e-=4H++O2↑
C.若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为10.4克
D.阴极反应式为:2NO3-+6H2O+10e-=N2↑+12OH-
高二化学单选题中等难度题查看答案及解析
化学在环境保护中起着十分重要的作用,电化学降解法可用于治理水中硝酸盐的污染。电化学降解NO3-的原理图所示。下列说法不正确的是:
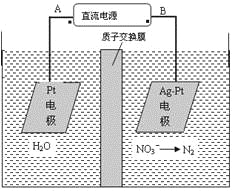
A.A为电源正极
B.阳极反应式为:2H2O-4e-=4H++O2↑
C.若电解过程中转移了2mol电子,则膜两侧电解液的质量变化差(Δm左-Δm右)为10.4克
D.阴极反应式为:2NO3-+6H2O+10e-=N2↑+12OH-
高二化学单选题中等难度题查看答案及解析
氰化氢是剧毒物质,含有氰的废水对环境的污染和人体的危害非常严重。
(1)氢氰酸(HCN)的电子式为______。
(2)用电解的方法可以除去含有CN-、Cl-废水中的CN-,其原理是控制溶液pH为9-10,利用阳极产生的ClO-将CN-氧化为两种无污染的气体。
①阳极的电极反应式:_________。
②除去CN-的离子方程式为:_________。
(3)已知25℃时,HCN的电离常数Ka=4.9×10-10,则25℃时0.1mol/L 的HCN溶液中c(H+)=_____mol/L。NaCN溶液中加入盐酸至恰好完全反应,溶液中所有离子浓度的关系为___________。
高二化学填空题中等难度题查看答案及解析
Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物pCP,探究有关因素对该降解反应速率的影响。
[实验设计]控制pCP的初始浓度相同,恒定实验温度在298 K或313 K(其余实验条件见下表),设计如下对比实验。
(1)请完成以下实验设计表(表中不要留空格)。
| 编号 | 实验目的 | T/K | pH | c/10-3 mol/L | |
| H2O2 | Fe2+ | ||||
| ① | 为以下实验作参考 | 298 | 3 | 6.0 | 0.30 |
| ② | 探究温度对降解反应速率的影响 | ____ | ____ | ____ | ____ |
| ③ | ____ | 298 | 10 | 6.0 | 0.30 |
[数据处理]实验测得pCP的浓度随时间变化的关系如图:
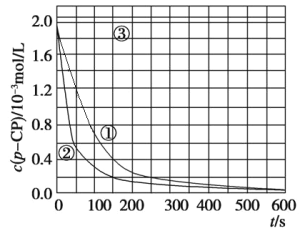
(2)请根据图中实验①曲线,列式并计算降解反应在50~150 s内的反应速率:________。
[解释与结论]
(3)实验①②表明温度升高,降解反应速率增大。但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:____________。
(4)实验③得出的结论是:pH等于10时,_________________________。
高二化学实验题中等难度题查看答案及解析
Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
[实验设计] 控制p-CP的初始浓度相同,恒定实验温度在298 K或313 K(其余实验条件见下表),设计如下对比实验:
(1)请完成以下实验设计表(表中不要留空格)
| 实验编号 | 实验目的 | T/K | pH | c/10-3 mol·L-1 | |
| H2O2 | Fe2+ | ||||
| ① | 为以下实验作参照 | 298 | 3 | 6.0 | 0.30 |
| ② | 探究温度对降解反应速率的影响 | 3 | |||
| ③ | 298 | 10 | 6.0 | 0.30 | |

[数据处理] 实验测得p-CP的浓度随时间变化的关系如上图
(2)请根据上图实验①曲线,计算降解反应50~150 s内的反应速率:
v(p-CP)=_______mol·L-1·s-1;
[解释与结论]
(3)实验①、②表明温度升高,降解反应速率增大。但后续研究表明:温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:_____________;
(4)实验③得出的结论是:pH等于10时,反应 (填“能”或“不能”)进行;
[思考与交流]
(5)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法: 。
高二化学填空题困难题查看答案及解析
Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好PH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
【实验设计】控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比试验。
(1)请完成以下实验设计表(表中不要留空格)。
| 实验 编号 | 实验目的 | T/K | pH | c/10-3mol·L-1 | |
| H2O2 | Fe2+ | ||||
| ① | 为以下实验作参考 | 298 | 3 | 6.0 | 0.30 |
| ② | 探究温度对降解反应速率的影响 | ________ | ________ | ________ | ________ |
| ③ | ________ | 298 | 10 | 6.0 | 0.30 |
【数据处理】实验测得p-CP的浓度随时间变化的关系如下图。

(2)请根据上图实验①曲线,计算降解反应在50~150s内的反应速率:
υ(p-CP)= ________mol·L-1·s-1
(3)实验①、②表明温度升高,降解反应速率增大。但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因: ________
________。
(4)实验③得出的结论是:pH等于10时,________。
(5)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法________。
高二化学实验题困难题查看答案及解析
(13分)Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好PH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
[实验设计]控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比试验。
(1)请完成以下实验设计表(表中不要留空格)。
| 实验 编号 | 实验目的 | T/K | PH | c/10-3mol·L-1 | |
| H2O2 | Fe2+ | ||||
| ① | 为以下实验作参考 | 298 | 3 | 6.0 | 0.30 |
| ② | 探究温度对降解反应速率的影响 | ||||
| ③ | 298 | 10 | 6.0 | 0.30 |
[数据处理]实验测得p-CP的浓度随时间变化的关系如下图。

(2)请根据右上图实验①曲线,计算降解反应在50~150s内的反应速率:
V(p-CP)= ________mol·L-1·s-1
[解释与结论](3)实验①、②表明温度升高,降解反应速率增大。但温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:
________
(4)实验③得出的结论是:PH等于10时,。
[思考与交流](5)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法:________
高二化学实验题中等难度题查看答案及解析
(16分)Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
[实验设计] 控制p-CP的初始浓度相同,恒定实验温度在298 K或313 K(其余实验条件见下表),设计如下对比实验:
(1)请完成以下实验设计表(表中不要留空格)
| 实验编号 | 实验目的 | T/K | pH | c/10-3 mol·L-1 | |
| H2O2 | Fe2+ | ||||
| ① | 为以下实验作参照 | 298 | 3 | 6.0 | 0.30 |
| ② | 探究温度对降解反应速率的影响 | 3 | |||
| ③ | 298 | 10 | 6.0 | 0.30 | |
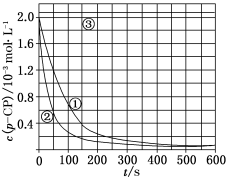
[数据处理] 实验测得p-CP的浓度随时间变化的关系如上图
(2)请根据上图实验①曲线,计算降解反应50~150 s内的反应速率:v(p-CP)=__ _____mol·L-1·s-1;
[解释与结论]
(3)实验①、②表明温度升高,降解反应速率增大。但后续研究表明:温度过高时反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因:_____________;
(4)实验③得出的结论是:pH等于10时,反应 (填“能”或“不能”)进行;
[思考与交流]
(5)实验时需在不同时间从反应器中取样,并使所取样品中的反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法: 。
高二化学实验题极难题查看答案及解析
(11分)Fenton法常用于处理含难降解有机物的工业废水,通常是在调节好pH和Fe2+浓度的废水中加入H2O2,所产生的羟基自由基能氧化降解污染物。现运用该方法降解有机污染物p-CP,探究有关因素对该降解反应速率的影响。
[实验设计]控制p-CP的初始浓度相同,恒定实验温度在298K或313K(其余实验条件见下表),设计如下对比试验。http://photo.blog.sina.com.cn/showpic.html - blogid=515359c40100g2jm&url=http://static1.photo.sina.com.cn/orignal/515359c4g79a02cb3d130&690http://photo.blog.sina.com.cn/showpic.html - blogid=515359c40100g2jm&url=http://static12.photo.sina.com.cn/orignal/515359c4g79a02bac230b&690
(1)完成以下实验设计表(表中不要留空格)。
| 实验 编号 | 实验目的 | T/K | pH | c/10-3mol·L-1 | |
| H2O2 | Fe2+ | ||||
| ① | 为以下实验作参照 | 298 | 3 | 6.0 | 0.30 |
| ② | 探究温度对降解反应速率的影响 | ||||
| ③ | 298 | 10 | 6.0 | 0.30 |
[数据处理]实验测得p—CP的浓度随时间变化的关系如下图。

(2)请根据上图实验①曲线,计算降解反应在50~150s内的平均反应速率;v(p—CP)= ________mol·L-1·s-1。
[解释与结论]
(3)实验①、②表明温度升高,该降解反应速率增大。但温度过高时(如接近100℃)反而导致降解反应速率减小,请从Fenton法所用试剂H2O2的角度分析原因: ________。
(4)实验③得出的结论是:pH等于10时,。
[思考与交流]
(5)实验时需在不同时间从反应器中取样,并使所取样品中反应立即停止下来。根据上图中的信息,给出一种迅速停止反应的方法:________
高二化学实验题中等难度题查看答案及解析