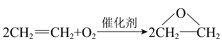-
甲醇是一种理想的液体燃料,工业上可利用CO与H2反应合成甲醇,即CO(g)+2H2(g)⇌CH3OH(g),该反应是放热反应。若在体积为2L的密闭容器中加入5molH2和一定量的CO后,CO和CH3OH(g)的浓度随时间的变化情况如图所示。
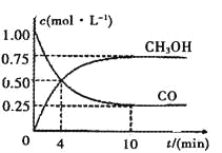
(1)该反应在0-4min内用H2表示的反应速率为:v(H2) =_____mol·L-1·s-1;10min末H2的转化率______; CO的体积分数________。
(2)该反应进行10min后,若体积不变,通入惰性气体则正应速率将______;在其他条件不变时,只升高体系的温度,则该反应的逆反应速率将______。 (填“增大”、“减小”或“不变”)
(3)当温度和体积一定时,该反应达到平衡状态的标志是______
A.混合气体的密度不变
B.CO、H2、CH3OH的反应速率之比为1: 2: 1
C.混合气体的平均相对分子质量不变
D.混合气体的质量不变
E.混合气体的压强不变
F.单位时间内生成a mol CH3OH,同时消耗2a mol H2
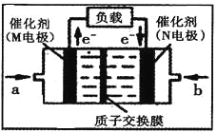
(4)如图是某研究机构开发的给笔记本电脑供电的甲醇燃料电池,甲醇在催化剂作用下提供质子(H+)和电子,M应作为原电池的_____(填“正极”或“负极”);H+通过质子交换膜移向____(填M电极或N电极);其负极的电极反应式为_______。
-
开发、使用清洁能源发展“低碳经济”正成为科学家研究的主要课题。氢气、甲醇是优质的清洁燃料,可制作燃料电池。
(1)工业上一般可采用如下反应来合成甲醇:2H2(g)+CO(g) CH3OH(g) △H= -90.8kJ•mol-1。
CH3OH(g) △H= -90.8kJ•mol-1。
①某温度下,将2mol CO和6mol H2充入2L的密闭容器中,充分反应10min后,达到平衡时测得c(CO)=0.2mol/L,则CO的转化率为____,以CH3OH表示该过程的反应速率v(CH3OH)=______。
②要提高反应2H2(g)+CO(g)⇌CH3OH(g)中CO的转化率,可以采取的措施是_______。
a.升温 b.加入催化剂 c.增加CO的浓度 d.加入H2 e.加入惰性气体 f.分离出甲醇
(2)①氢氧燃料电池是一种高效无污染的清洁电池它分碱性(用KOH做电解质)和酸性(用硫酸做电解质)燃料电池。如果是酸性燃料电池,则正极反应方程式是____________。
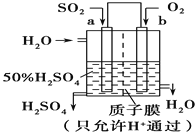
②科研人员设想用如图原电池装置生产硫酸,则负极的电极反应式为__________。
-
利用含碳化合物合成新燃料是发展低碳经济的重要方法,已知:CO(g) + 2H2(g) CH3OH(g)是合成甲醇(CH3OH)的反应,该反应过程的能量变化如图所示,下列判断正确的是( )
CH3OH(g)是合成甲醇(CH3OH)的反应,该反应过程的能量变化如图所示,下列判断正确的是( )

A. CO(g)与H2(g)反应生成1mol CH3OH(g)释放出91kJ的能量
B. 用碳制备原料气CO、H2的反应属于放热反应
C. 反应物总键能高于生成物的总键能
D. 若该反应生成液态CH3OH,则放出的能量更少
-
回收利用CO2是环境科学研究的热点课题,是减轻温室效应危害的重要途径 。
(1)工业上,利用天然气与二氧化碳反应制备合成气(CO和H2),化学方程式为CO2(g) +CH4(g)=2CO( g) +2H2O(g),上述反应的能量变化如图1所示,该反应是____(填“吸热反应”或“ 放热反应"”)。

(2)工业上用CO2生产甲醇(CH3OH)燃料,可以将CO2变废为宝。在体积为IL的密闭容器中,充入l molCO2和4mo1H2,一定条件下发生反应:CO2(g)+3H2(g)=CH3OH(g)+H2O(g),测得CO2(g)和CH3OH(g)的浓度随时间变化如图2所示。
①从反应开始到平衡,用CH3OH 表示的平均反应速率为 ______。
②若反应CO2(g) +3H2 (g) = CH3OH (g) +H2O(g)在四种不同情况下的反应速率分别为:
A.v(H2) =0.01 mol•L-1 •s-1 B.v(CO2) =0.15 mol•L-1 •s-1
C.v(CH3OH)=0.3 mol•L-1 •min-1 D.v(H2O)=0.45 mol•L-1 •min-1
该反应进行由慢到快的顺序为_______(填字母)。
③下列描述能说明反应达到最大限度的是_____(填字母)
A.混合气体的密度保持不变
B.混合气体中CH3OH 的体积分数约为21.4%
C.混合气体的总质量保持不变
D.H2、CH3OH的生成速率之比为3:1
(3)甲醇(CH3OH )是一种可再生能源,具有广阔的开发和应用前景。以甲醇、氧气和KOH溶液为原料,石墨为电极制造新型手机电池,氧气在___极反应;电极反应式为______。
-
煤的工业加工过程中,可利用CO和H2合成甲醇,能量变化如图所示。下列说法正确的是
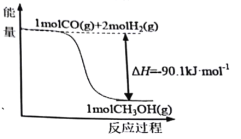
A.该反应是吸热反应
B.1molCH3OH所具有的能量为90.1kJ
C.CO(g)+2H2(g) CH3OH(l) ΔH=-90.1kJ·mol-1
CH3OH(l) ΔH=-90.1kJ·mol-1
D.1molCO和2molH2断键所需能量小于1molCH3OH断键所需能量
-
工业上由CO2和H2合成气态甲醇的化学方程式为CO2+3H2===CH3OH+H2O,已知该反应是放热反应。下面表示合成甲醇的反应的能量变化示意图,其中正确的是( )
A.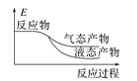 B.
B.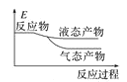
C.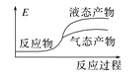 D.
D.
-
甲醇是一种重要的化工原料和新型燃料。
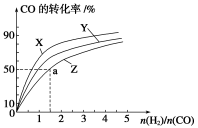
(1)工业上一般以CO和H2为原料在密闭容器中合成甲醇:CO(g)+2H2(g) CH3OH(g) ΔH=-90.8 kJ·mol-1。在容积为1 L的恒容容器中,分别研究在230 ℃、250 ℃和270 ℃三种温度下合成甲醇的规律。下图是上述三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1 mol)与CO平衡转化率的关系,则曲线Z对应的温度是________;该温度下上述反应的化学平衡常数为________;
CH3OH(g) ΔH=-90.8 kJ·mol-1。在容积为1 L的恒容容器中,分别研究在230 ℃、250 ℃和270 ℃三种温度下合成甲醇的规律。下图是上述三种温度下H2和CO的起始组成比(起始时CO的物质的量均为1 mol)与CO平衡转化率的关系,则曲线Z对应的温度是________;该温度下上述反应的化学平衡常数为________;
(2)下图是甲醇燃料电池工作的示意图,其中A、B、D均为石墨电极,C为铜电极。工作一段时间后,断开K,此时A、B两极上产生的气体体积相同。
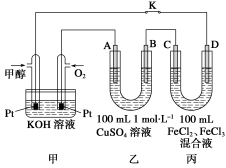
I.甲中负极的电极反应式为_________ _______
II.乙中反应的化学方程式为______ __ ________;A极析出的气体在标准状况下的体积为________________。
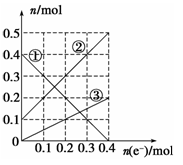
III.丙装置溶液中金属阳离子的物质的量与转移电子的物质的量变化关系如下图,则图中②线表示的是________的变化;反应结束后,要使丙装置中金属阳离子恰好完全沉淀,需要________ mL 5.0 mol·L-1 NaOH溶液。
-
(8分)甲醇是一种优质燃料,可制作燃料电池。
(1)工业上可用下列两种反应制备甲醇:
①CO(g) + 2H2(g)  CH3OH(g) ΔH1 ②CO2(g)+3H2(g)
CH3OH(g) ΔH1 ②CO2(g)+3H2(g)  CH3OH(g) + H2O(g) ΔH2
CH3OH(g) + H2O(g) ΔH2
已知:③2H2(g)+ O2(g) = 2H2O(g) ΔH3 。则2CO(g)+O2(g)=2CO2(g) 的反应热
ΔH=______(用ΔH1、ΔH2、ΔH3表示)。
(2)生产甲醇的原料CO和H2来源于:CH4(g) + H2O(g)  CO(g) + 3H2(g) ΔH4。
CO(g) + 3H2(g) ΔH4。
一定条件下CH4的平衡转化率与温度、压强的关系如图a。则ΔH4______0,P1_________P2
(填“<”、“>”或“=”)
某实验小组设计如图b所示的甲醇燃料电池装置,工作一段时间后,溶液的PH (填增大、 减小、不变)。负极的电极反应式为_______ ____。

(4)黄铜矿熔炼后得到的粗铜含少量Fe、Ag、Au等金属杂质,需进一步采用电解法精制。粗铜电解得到精铜的的电解池中,阳极材料是 ;阴极材料是 ;阳极泥为: 
-
“绿色化学”的理想状态是反应物的原子全部转化为目标产物。以下反应不符合绿色化学原则的是
A. 工业生产环氧乙烷: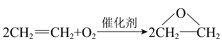
B. 水煤气合成甲醇:CO + 2H2催化剂CH3OH
C. 制取硫酸铜:Cu + 2H2SO4(浓)加热CuSO4 + SO2↑+ 2H2O
D. 合成甲基丙烯酸甲酯:CH3C≡CH + CO + CH3OH Pd CH2=C(CH3)COOCH3
-
近年来甲醇用途日益广泛,越来越引起商家的关注,工业上甲醇的合成途径多种多样。现在实验室中模拟甲醇合成反应,在2 L密闭容器内,400 ℃时发生反应:CO(g)+2H2(g) CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:
CH3OH(g),体系中甲醇的物质的量n(CH3OH)随时间的变化如表:
| 时间(s) | 0 | 1 | 2 | 3 | 5 |
| n(CH3OH) (mol) | 0 | 0.009 | 0.012 | 0.013 | 0.013 |
(1)下图中表示CH3OH的浓度变化的曲线是_________(填字母)。
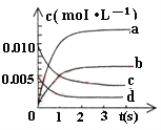
(2)用H2表示从0~2s内该反应的平均速率v(H2) =__________。随着反应的进行,该反应的速率在逐渐减慢的原因是 _____________。
(3)能说明该反应已达到平衡状态的是________。
a.容器内CO与CH3OH的浓度相等 b.v逆(CO) = v正(H2)
c.容器内气体的密度保持不变 d.容器内气体的压强不变
(4)该反应是一个放热反应,说明该反应中破坏1mol CO和2mol H2的化学键吸收的能量_________形成1mol CH3OH释放的能量(填“﹤”、“=”或“﹥”)。
(5)已知在400 ℃时,反应CO(g)+2H2(g) CH3OH(g) 生成1 mol CH3OH(g),放出的热量为116 kJ。计算上述反应达到平衡时放出的热量Q =_________kJ。
CH3OH(g) 生成1 mol CH3OH(g),放出的热量为116 kJ。计算上述反应达到平衡时放出的热量Q =_________kJ。






 B.
B.
 D.
D.