-
研究化学反应时,既要关注物质变化, 又要关注能量变化。请回答以下问题.
(1)氢气在氧气中燃烧 ,破坏1mol H-H 键吸收Q1 kJ 的热量,破坏 1 mol O=O 键吸收Q2kJ 的热量, 形成 1 mol H—O 键释放Q3kJ 的热量,则下列关系式正确的是。_____ (填字母序号)
A 2Q1+Q2>4Q3 B Q1+Q 2<Q3
C 2Q 1+ Q 2<4Q3 D 2 Q1+Q 2=4Q3
(2)用CH4催化还原氮氧化物可以消除氮氧化物的污染。
已知:①2N2(g)+ CO2(g)+ 2H2O(g)= CH4(g)+ 4NO(g) ΔH1=akJ/mol
②CH4(g)+ 4NO2(g)= 4 NO(g)+ CO2(g) + 2 H2O(g) ΔH2 = b kJ/mol
③H2O(1)= H2O(g)ΔH3 =c kJ/mol
则CH4(g)+2NO2(g)=N2(g)+ CO2(g)+ 2H2O(1) ΔH=_______kJ/mol (用含a、b、c的代数式表示)。
(3)红磷 P(s)和Cl2(g) 发生反应生成PCl3(g)和 PCl5(g), 反应过程中的热量关系如图所示(图中的ΔH表示生成 1mol 产物的数据)。
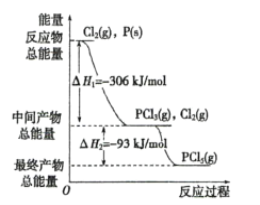
根据如图回答下列问题:
①写出P(s)和Cl2(g)反应生成PCl5(g)的热化学方程式________;
②已知:常温时红磷比白磷稳定,比较下列反应中ΔH 的大小:ΔH1 ___ ΔH2(填“> ”、“< ”或“= ”)。
i.P4(白磷,s)+5O2(g)= 2P2O5(s) ΔH1< 0
ii.4P(红磷,s)+5O2(g)=22P2O5(s) ΔH2< 0
-
氢气在氧气中燃烧产生淡蓝色火焰,在反应中,破坏1mol H-H键消耗的能量为Q1 kJ,破坏1mol O═O键消耗的能量为Q2 kJ,形成1mol H-O键释放的能量为Q3 kJ.下列关系式中正确的是( )
A.2Q1+Q2>4Q3
B.2Q1+Q2<4Q3
C.Q1+Q2<Q3
D.2Q1+Q2=4Q3
-
氢气在氧气中燃烧产生淡蓝色火焰,在反应中,破坏1mol H-H键消耗的能量为Q1kJ,破坏1mol O=O键消耗的能量为Q2kJ,形成1mol H-O键释放的能量为Q3kJ。下列关系式中正确的是( )
A. 2Q1+ Q2<4Q3 B. 2Q1+ Q2>4Q3
C. Q1+ Q2<Q3 D. Q1+ Q2=Q3
-
氢气在氧气中燃烧时产生淡蓝色火焰.在反应中,破坏1mol氢气中的化学键消耗能量为Q1KJ,破坏1mol氧气中的化学键消耗能量为Q2KJ,形成1molO﹣H化学键释放的能量为Q3KJ.下列说法正确的是( )
A.2Q1+Q2>4Q3
B.Q1+Q2<Q3
C.1mol氧气和2mol氢气的总能量高于1mol水的总能量
D.1mol氧气和2mol氢气的总能量低于1mol水的总能量
-
已知1g氢气完全燃烧生成水蒸气时放出121kJ的能量,且氧气中1molO=O键完全断裂时需要吸收496kJ的能量,水蒸气中1mol H-O键形成时放出463kJ的能量,则氢气中1mol H-H键断裂时吸收的能量为
A.920kJ B.557kJ C.436kJ D.181kJ
-
已知1g氢气完全燃烧生成水蒸气时放出121kJ的能量,且氧气中1molO=O键完全断裂时需要吸收496kJ的能量,水蒸气中1mol H-O键形成时放出463kJ的能量,则氢气中1mol H-H键断裂时吸收的能量为( )
A. 920kJ B. 557kJ C. 436kJ D. 181kJ
-
已知1g氢气完全燃烧生成水蒸气时放出121kJ的能量,且氧气中1molO=O键完全断裂时需要吸收496kJ的能量,水蒸气中1mol H-O键形成时放出463kJ的能量,则氢气中1mol H-H键断裂时吸收的能量为( )
A. 920kJ B. 557kJ C. 436kJ D. 181kJ
-
氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏1mol氢气中的化学键消耗的能量为Q1 kJ,破坏1mol氯气中的化学键消耗的能量为Q2 kJ,形成1mol氯化氢中的化学键释放的能量为Q3 kJ。下列关系式中,正确的是
A.Q1 + Q2 > Q3 B. Q1 + Q2 > 2Q3
C.Q1 + Q2 < 2Q3 D. Q1 + Q2 < Q3
-
已知氢气在氯气中燃烧时产生苍白色火焰,在反应过程中,破坏1mol氢气的化学键消耗的能量为Q1kJ,破坏1mol氯气的化学键消耗的能量为Q2kJ,破坏1mol氯化氢中的化学键消耗的能量为Q3kJ,下列关系式最准确的是
A.Q1+Q2>Q3 B.Q1+Q2>2Q3 C.Q1+Q2<Q3 D.Q1+Q2<2Q3
-
氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,破坏 1mol氢气中的化学键消耗的能量为Q1kJ,破坏1mol氯气中的化学键消耗的能量为Q2kJ,形成1mol氯化氢中的化学键释放的能量为Q3kJ。下列关系式中,正确的是( )
A. Q1+Q2>Q3 B. Q1+ Q2<2Q3 C. Q1+Q2<Q3 D. Q1+ Q2>2Q3
