-
Q、R、X、Y、Z是原子序数依次增大的前四周期元素,Q的一种单质是天然存在的最硬的物质,X原子的核外电子有八种运动状态,Y元素的离子半径是第三周期中最小的,Z是第四周期中未成对电子最多的原子。
(1)Z原子的价电子排布式为_________________。
(2)Q、R、X、Y四种元素的电负性由大到小的顺序是_______________。
(3)杂化轨道理论指出原子中能量相近的s、p或s、p、d轨道之间可以通过杂化形成种类丰富的杂化轨道。RCl3分子中心原子的杂化方式为___________,从原子结构的角度解释不存在RCl5分子的原因_______。
(4)配合物甲的分子式为ZCl3·4H2O,配位数为6。取1mol甲溶于水,加入足量的AgNO3溶液,得到143.5g白色沉淀。在酸性溶液中,甲发生水合反应转化为乙(ZCl3·6H2O)。乙的配位原子只有一种,配位数为6。
①甲的结构简式为_______________。
②甲→乙的化学方程式为______________。
(5)图a是Q的一种同素异形体和钾形成的插层化合物的晶胞图,图b是晶胞沿侧面的投影图。该插层化合物的化学式为______________。

-
X、Y、Z、Q、W为前四周期中原子序数依次增大的元素。X原子的2p能级上有两个未成对电子,且无空轨道。Y原子K层的电子数与M层的电子数的乘积等于其L层的电子数;Z与X同族,Q位于第ⅠB族;W元素最高正价和最低负价的代数和为4。根据以上信息,回答下列问题。
(1)W元素的名称是:___________;其简化的电子排布式为___________________;X的基态原子核外最高能级上有_____种不同空间运动状态的电子;已知高温下4QX→2Q2X+X2,从Q原子价层电子结构的角度分析,能生成Q2X的原因是__________________________________。
(2)Y与X可以形成多种复杂阴离子,如下图所示,若其中a对应的阴离子化学式为YX ,则c对应的阴离子的化学式为_________________(圆圈代表X原子,黑点代表Y原子)。
,则c对应的阴离子的化学式为_________________(圆圈代表X原子,黑点代表Y原子)。

(3)向盛有含Q2+的溶液中加入氨水至过量,沉淀溶解的离子方程式为___________________。写出最后所得配离子的结构式____________________________________(配位键须注明)。
(4)W、Y均能与氢元素形成气态氢化物,则它们形成的组成最简单的氢化物中,VSEPR构型____________(填“相同”或“不相同”),若“Y−H”中共用电子对偏向氢元素,氢气与W反应时单质W是氧化剂,则W与Y的电负性相对大小为______________(用元素符号作答)。
-
(物质结构与质性题)X、Y、Z、W是元素周期表前四周期中常见的元素,原子序数依次增大。其相关信息如下表:
| 元素 | 相关信息 |
| X | X的基态原子价层电子中有两个未成对电子 |
| Y | Y的基态原子最外层电子排布式为:nsnnpn+2 |
| Z | Z存在质量数为23,中子数为12的核素 |
| W | W有多种化合价,其白色氢氧化物在空气中会迅速变成灰绿色,最后变成红褐色 |
(1)X的电负性比Y的________(填“大”或“小”);
X 和Y的气态氢化物中,较稳定的是 (写化学式)。
(2)W在周期表中的位置是 ,其基态原子价电子的电子排布式为 。
(3)Z2Y2的电子式为 ,请写出Z2Y2与XY2反应的化学方程式 。
(4)在XY2分子中X原子的杂化方式为 ,其分子的空间构型为 。氢、X、Y三种元素可共同形成多种分子和一种常见无机阴离子,写出其中一种分子与该无机阴离子反应的离子方程式: 。
-
按下列要求作答。
(1)第二周期中,第一电离能介于B和N之间的元素共有_________种。
(2)第四周期中,原子核外电子排布有两个未成对电子的元素有_________种。
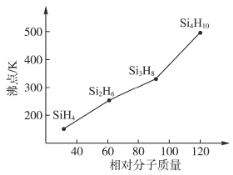
(3)硅烷(Si,H2H2n+2)的沸点与其相对分子质量的变化关系如图所示,呈现这种变化关系的原因是___________________________。
-
T、W、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大,相关信息如下表:
| 元素 | 相关信息 |
| T | T元素可形成自然界硬度最大的单质 |
| W | W与T同周期,核外有三个未成对电子 |
| X | X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/mol, I4=11575kJ/mol |
| Y | 常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质 |
| Z | Z的一种同位素的质量数为63,中子数为34 |
(1) TY2是一种常用的溶剂,是_________ (填极性分子或非极性分子),1mol TY2中存在_________个σ键。
(2)写出X与NaOH溶液反应的离子方程式_________。
(3)Z的基态原子核外电子排布式为_________,ZYO4溶液常作电镀液,其中YO42-的空间构型是_________。
(4)将WH3的水溶液逐滴滴加到ZYO4溶液中,现象为_________,相应的离子方程式为_________。
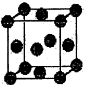
(5)已知Z的晶胞结构如下图所示,该晶体的原子堆积模型为_________,又知Z的密度为ρ g/cm3,则晶胞边长为_________ cm(用含p代数式表示)。
-
A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1 817kJ/mol,I3=2 745kJ/mol,I4=11 575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为65,中子数为35.请回答下列问题:
(1)AY2是一种常用的溶剂,为 分子(填“极性”或“非极性”),分子中存在 个σ键.(2)X形成的单质与NaOH溶液反应的离子方程式为 ,超高导热绝缘耐高温纳米XB在绝缘材料中应用广泛,其晶体与金刚石类似,属于 晶体.
(3)X、氧、B元素的电负性由大到小的顺序为 (用元素符号作答).
(4)Z的基态原子核外电子排布式为 .
-
A、B、X、Y、Z是元素周期表前四周期中的常见元素,原子序数依次增大.A元素可形成自然界硬度最大的单质;B与A同周期,核外有三个未成对电子;X原子的第一电离能至第四电离能分别是:I1=578kJ/mol,I2=1817kJ/mol,I3=2745kJ/mol,I4=11575kJ/mol;常温常压下,Y单质是固体,其氧化物是形成酸雨的主要物质;Z的一种同位素的质量数为63,中子数为34.请回答下列问题:
(1)AY2是一种常用的溶剂,为______分子(填“极性”或“非极性”),分子中存在_____个σ键。
(2)X形成的单质与NaOH溶液反应的离子方程式为_________,超高导热绝缘耐高温纳米XB在绝缘材料中应用广泛,其晶体与金刚石类似,属于晶体.B的最简单氢化物容易液化,理由是_______________。
(3)Z的基态原子核外电子排布式为_________。元素Z与人体分泌物中的盐酸以及空气反应可生成超氧酸:Z+HCl+O2=ZCl+HO2,HO2(超氧酸)不仅是一种弱酸而且也是一种自由基,具有极高的活性。下列说法或表示不正确的是______(填序号)。
①氧化剂是O2
②HO2在碱中不能稳定存在
③氧化产物是HO2
④1molZ参加反应有1mol电子发生转移
-
(18分)(一)按要求作答:
(1)第四周期中,未成对电子数最多的原子,其外围电子排布式为:________。
(2)3d能级为半充满的正三价离子,该离子的电子排布式为________。
(二)A、B、C、D、E五种元素为1~18号元素。已知:它们的原子序数依次增大,A、B两种元素的核电荷数之差等于它们的原子最外层电子数之和;B原子最外层电子数比其次外层电子数多2;C元素原子的电子层数及最外层电子数都比E元素的少1;D和E的原子序数之和为30。它们两两形成的化合物有甲、乙、丙、丁四种。这四种化合物中原子个数比如下表:
甲 乙 丙 丁
化合物中各元素原子个数比 A和C 1∶1 B和A 1∶2 D和E 1∶3 B和E 1∶4
(1)E-的结构示意图是________________。B原子核外有________个未成对电子,它们的能量______________(填“相等”或“不相等”)。
(2)向甲的水溶液中加入MnO2可用于实验室制备C的单质,其化学方程式是____________________。
(3)已知有机物乙的分子为平面结构,键角都为120°,它的结构简式为___________。
(4)丙的水溶液呈酸性,与饱和NaHCO3溶液反应会产生大量的气体和难溶物,有关离子方程式是____________________。
-
下列说法正确的是( )
A.前四周期中,原子最外层为1个电子的元素有5种
B.Fe2+的价电子排布为3d6
C.2p轨道上有1个未成对电子的原子与3p轨道上有1个未成对电子的原子化学性质相似
D.AB3型分子的中心原子A采取sp3杂化
-
下列四种元素中,其单质氧化性最强的是( )
A. 原子含有未成对电子最多的第二周期元素 B. 位于元素周期表中第三周期第ⅢA族的元素
C. 原子最外层电子排布式为2s22p6的元素 D. 原子最外层电子排布式为2s22p5的元素
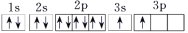 。该同学所画的电子排布图违背了________。
。该同学所画的电子排布图违背了________。


