-
元素周期表是打开物质世界奧秘之门的一把金钥匙 ,1869年,门捷列夫发现了元素周期律并发表了元素周期表。下图为元素周期表的一部分,回答下列问题。
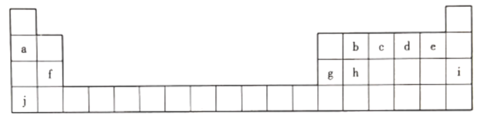
(1).上述元素中化学性质最稳定的是________(填元素符号,下同) ,非金属性最强的是_____。
(2)c的最高价氧化物对应水化物的化学式为__________。
(3)h元素的原子结构示意图为__________,写出h单质的一种用途:__________。
(4)b、d、f三种元素原子半径由大到小的顺序是__________(用元素符号表示)。
(5)a、g、j的氢氧化物中碱性最强的是__________(填化学式),写出其溶液与g的氧化物反应的离子方程式:___________________________________。
高一化学综合题中等难度题查看答案及解析
-
素周期表是打开物质世界奥秘之门的一把金钥匙 ,1869 年门捷列夫发现了元素周期律并发表了元素周期表,下表是元素周期表的一部分。
a
b
c
d
e
f
g
h
i
j
As
(1)上述元素中化学性质最稳定的是_______(填元素符号,下同 ),最轻的金属_______是制造电池的理想物质。
(2)h元素的原子结构示意图为_____,写出 h 单质的一种用途______。
(3) c、d、As 三种元素的最简单氢化物的稳定性为_____; c 、d、f、i 的简单离子半径由大到小顺序是____。
(4)e与j 组成的化合物是自然界中常见的矿石一萤石的主要成分,用电子式表示该物质______。
(5)元素f与g的最高价氧化物对应的水化物反应的化学方程式是_______。
(6)由d、f、i三种元素组成的化合物M的水溶液是一种生活中常见的消毒剂。As可与M的碱性溶液反应,当消耗lmol还原剂时,消耗2.5mol氧化剂,转移5mol电子。则该反应的离子方程式为______。
高一化学元素或物质推断题中等难度题查看答案及解析
-
元素是构成我们生活的世界中一切物质的“原材料”。
(1)1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图所示。
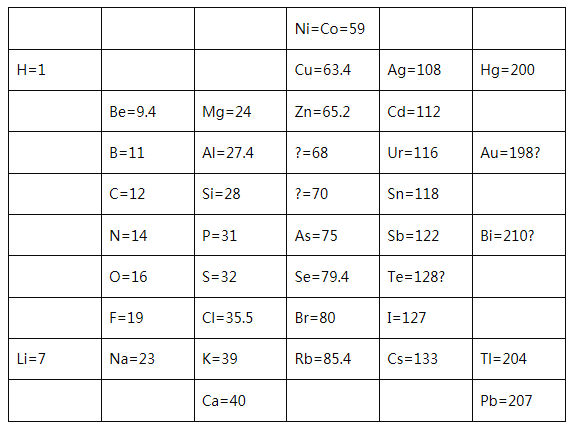
①门捷列夫将已有元素按照相对原子质量排序,同一_________(填“横行”或“纵列”)元素性质相似。结合表中信息,猜想第4列方框中“?=70”的问号表达的含义是______,第5列方框中“Te=128?”的问号表达的含义是________。
②到20世纪初,门捷列夫周期表中为未知元素留下的空位逐渐被填满。而且,随着原子结构的逐渐揭秘,科学家们发现了元素性质不是随着相对原子质量递增呈现周期性变化,而是随着原子序数(核电荷数)递增呈现周期性变化。其本质原因是_____(填字母序号)。
A. 随着核电荷数递增,元素主要化合价呈现周期性变化
B. 随着核电荷数递增,原子核外电子排布呈现周期性变化
C. 随着核电荷数递增,原子半径呈现周期性变化
(2)短周期元素A、B、D、E、G、J在周期表中的位置如下:
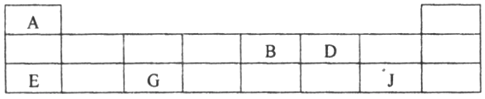
根据上表回答问题:
①第三周期的四种元素中离子半径最小的是_________ (用元素符号填答)。
②B、D的非金属性由大到小的顺序是__________ (用元素符号填答)。
③E、G、J的最高价氧化物对应水化物两两之间反应的离子方程式分别为i.H++OH-=H2O、ii.___、iii.___。
④用电子式表示A2D形成过程_______________。
(3)元素Y的一种含氧酸化学式为 H3YO3,其结构式可表示为:
。该酸为______元酸,请写出该酸与过量氢氧化钠溶液反应的化学方程式_____。(用对应元素符号填答)(已知信息:氢氧原子结合成的一种原子团“—OH”叫羟基,含氧酸中只有羟基氢才可电离出 H+。)
高一化学填空题中等难度题查看答案及解析
-
元素是构成我们生活的世界中一切物质的“原材料”。
Ⅰ.1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图所示。
Ni=Co=59
H=1
Cu=63.4
Ag=108
Hg=200
Be=9.4
Mg=24
Zn=65.2
Cd=112
B=11
Al=27.4
?=68
Ur=116
Au=198?
C=12
Si=28
?=70
Sn=118
N=14
P=31
As=75
Sb=122
Bi=210?
O=16
S=32
Se=79.4
Te=128?
F=19
Cl=35.5
Br=80
I=127
Li=7
Na=23
K=39
Rb=85.4
Cs=133
Tl=204
Ca=40
Pb=207
(1)门捷列夫将已有元素按照相对原子质量排序,同一_____(填“横行”或“纵列”)元素性质相似。
(2)结合表中信息,猜想第5列方框中“Te=128?”的问号表达的含义是___________。
Ⅱ.X、Y、Z、W是现在元素周期表中的短周期元素,它们的相对位置如下图所示,其中 Y 元素原子核外最外层电子数是其电子层数的3倍。
X
Y
Z
W
请回答下列问题:
(1)W位于周期表中的位置____________________。
(2)比较Y、Z气态氢化物的稳定性______________(用分子式表示)。
(3)科学家们认为存在含氢量最高的化合物XH5,预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,写出该反应的化学方程式___________,XH5是离子化合物,它的电子式为________。
(4)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式_______________________________。
高一化学综合题中等难度题查看答案及解析
-
元素是构成我们生活的世界中一切物质的“原材料”。
Ⅰ.1869年,门捷列夫在前人研究的基础上制出了第一张元素周期表,如图所示。
Ni=Co=59
H=1
Cu=63.4
Ag=108
Hg=200
Be=9.4
Mg=24
Zn=65.2
Cd=112
B=11
Al=27.4
?=68
Ur=116
Au=198?
C=12
Si=28
?=70
Sn=118
N=14
P=31
As=75
Sb=122
Bi=210?
O=16
S=32
Se=79.4
Te=128?
F=19
Cl=35.5
Br=80
I=127
Li=7
Na=23
K=39
Rb=85.4
Cs=133
Tl=204
Ca=40
Pb=207
(1)门捷列夫将已有元素按照相对原子质量排序,同一_____(填“横行”或“纵列”)元素性质相似。
(2)结合表中信息,猜想第5列方框中“Te=128?”的问号表达的含义是___________。
Ⅱ.X、Y、Z、W是现在元素周期表中的短周期元素,它们的相对位置如下图所示,其中 Y 元素原子核外最外层电子数是其电子层数的3倍。
X
Y
Z
W
请回答下列问题:
(1)W位于周期表中的位置____________________。
(2)比较Y、Z气态氢化物的稳定性______________(用分子式表示)。
(3)科学家们认为存在含氢量最高的化合物XH5,预测其与水剧烈反应放出气体,所得水溶液呈弱碱性,写出该反应的化学方程式___________,XH5是离子化合物,它的电子式为________。
(4)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式_______________________________。
高一化学综合题中等难度题查看答案及解析
-
1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位置、结构和性质的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
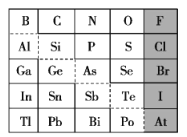
(1)Sn的最高价氧化物对应水化物的化学式为___,N、O、F对应的简单离子的半径由大到小的顺序为___。(写离子符号)
(2)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是___。(写化学式)
②H3AsO4、H2SeO4的酸性强弱:H3AsO4(填“>”“<”或“=”)___ H2SeO4。
③镓的氯化物与氨水反应的化学方程式为___。
(3)用铝和金属氧化物反应制备金属单质是工业上较常用的方法。如:2A1+4BaO
3Ba↑+BaO•A12O3
利用上述方法可制取Ba的主要原因是(________)
a.高温时A1的活泼性大于Ba
b.高温有利于BaO分解
c.高温时BaO•A12O3比Al2O3稳定
d.Ba的沸点比A1的低
(4)用铝热法还原下列氧化物,制得金属各1mo1,消耗铝最少的是___。
a.MnO2 b.WO3 c.Cr2O3 d.Co3O4
高一化学综合题中等难度题查看答案及解析
-
1869年,俄国化学家门捷列夫制作出了第一张元素周期表,揭示了化学元素间的内在联系,成为化学史上的重要里程碑之一。下列有关元素周期表的说法正确的是
A. 元素周期表有18个族 B. 元素周期表含元素最多的族是第IIIB族
C. 第I A族的元素全部是金属元素 D. 第五、六周期包含元素种类数目相同
高一化学选择题中等难度题查看答案及解析
-
1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经150年。元素周期表体现了元素位、构、性的关系,揭示了元素间的内在联系。下表是元素周期表的一部分,针对表中的①~⑩中元素,用元素符号或化学式填空回答以下问题:
主族
周期
IA
IIA
IIIA
IVA
VA
VIA
VIIA
0
2
①
②
3
③
④
⑤
⑥
⑦
⑧
⑨
4
⑩
(1)表中化学性质最不活泼的元素,其原子结构示意图为___;
(2)元素①的单质电子式为____。
(3)比较③、⑤元素的金属性强弱___>___;并写出它们最高价氧化物对应的水化物间反应的化学方程式____。
(4)上述元素的最高价氧化物对应的水化物中,酸性最强的是____。
(5)在元素③、④、⑤、⑦、⑧形成的简单离子中,半径最小的是_____;
(6)工业制取⑥的单质的反应的化学方程式为_______。
高一化学综合题中等难度题查看答案及解析
-
1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。下图是元素周期表的一部分,回答下列问题:
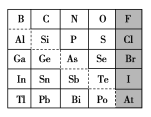
(1)元素Ga在元素周期表中的位置为:第________周期第________族。
(2)Sn的最高正价为________,Cl的最高价氧化物对应水化物的化学式为________,Bi的最高价氧化物为________。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是________元素(填元素符号)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4________(填“>”“<”或“=”)H2SeO4。
③氢化物的还原性:H2O________(填“>”“<”或“=”)H2S。
④原子半径比较:N________(填“>”“<”或“=”)Si。
(4)从下列试剂中选择最佳试剂组合,比较C、Si的非金属性强弱___________________ (可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液)
高一化学综合题困难题查看答案及解析
-
1869年俄国化学家门捷列夫制出第一张元素周期表,到现在形成的周期表经过了众多化学家的艰辛努力,历经142年。元素周期表体现了元素位构性的关系,揭示了元素间的内在联系。如图是元素周期表的一部分,回答下列问题:
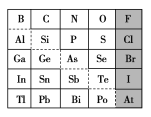
(1)元素Ga在元素周期表中的位置为:第________周期第________族。
(2)Sn的最高正价为________,Cl的最高价氧化物对应水化物的化学式为________,Bi的最高价氧化物为________。
(3)根据元素周期律,推断:
①阴影部分元素氢化物热稳定性最高的是________元素(填元素符号)。
②H3AsO4、H2SeO4的酸性强弱:H3AsO4________(填“>”“<”或“=”)H2SeO4。
③氢化物的还原性:H2O________(填“>”“<”或“=”)H2S。
④原子半径比较:N________(填“>”“<”或“=”)Si。
(4)可在图中分界线(虚线部分)附近寻找________(填序号)。
A.优良的催化剂 B.半导体材料 C.合金材料 D.农药
(5)从下列试剂中选择最佳试剂组合,比较C、Si的非金属性强弱__________________________
(可供选择的药品有:CaCO3固体、稀硫酸、盐酸、饱和NaHCO3溶液、饱和Na2CO3溶液、硅酸钠溶液.)
高一化学填空题中等难度题查看答案及解析