-
CO和H2是工业上最常用的合成气,该合成气的制备方法很多,它们也能合成许多重要的有机物。回答下列问题:
(1)制备该合成气的一种方法是以CH4和H2O为原料,有关反应的能量变化如图所示。
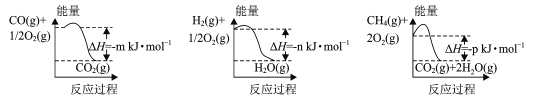
CH4 (g)与H2O(g)反应生成CO(g)和H2 (g)的热化学方程式为____。
(2)工业乙醇也可用CO和H2合成,常含一定量甲醇,各国严禁使用成本低廉的工业酒精勾兑食用酒,但一般定性的方法很难检测出食用酒中的甲醇。有人就用硫酸酸化的橙色K2Cr2O7溶液定量测定混合物中甲醇的含量,甲醇与酸性K2Cr2O7溶液反应生成CO2、Cr2(SO4)3等物质,写出其化学方程式 ___________。
(3)为了检验由CO和H2合成气合成的某有机物M的组成,进行了如下测定:将1.84gM在氧气中充分燃烧,将生成的气体混合物通过足量的碱石灰,碱石灰 增重4. 08 g,又知生成CO2和H2O的物质的量之比为3:4。则M中碳、氢、氧原子个数之比为____。
(4) CO2和H2合成甲醇涉及以下反应:CO2(g)+3H2(g)⇌CH3OH(g)+H2O(g) ∆H=-49.58kJ/mol。在反应过程中可以在恒压的密闭容器中,充入一定量的CO2和H2,测得不同温度下,体系中CO2的平衡转化率与压强的关系曲线如图所示:
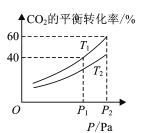
①反应过程中,表明反应达到平衡状态的标志是______;
A.生成3mol O-H键,同时断裂3mol H-H键 B.容器中气体的压强不再变化
C.容器中气体的平均摩尔质量不变 D.CH3OH的浓度不再改变
②比较T1与T2的大小关系:T1 ___T2 (填“<”、“=”或“>”)。
③在T1和P2的条件下,向密闭容器中充入1mol CO2和3mol H2,该反应在第5 min时达到平衡,此时容器的容积为2.4 L,则该反应在此温度下的平衡常数为____,保持T1和此时容器的容积不变,再充入1mol CO2和3mol H2,设达到平衡时CO2的总转化率为a,写出一个能够解出a的方程或式子 ___(不必化简,可以不带单位)。
-
氨是化肥工业和基本有机化工的主要原料,合成氨工业因此成为基本无机化工之一。回答下列问题:
(1)如何获得廉价的氢气是合成氨工业中的重要课题,目前常用戊烷跟水蒸气反应的方法 获得氢气:
C5H12(g)+5H2O(g)  5CO(g)+11H2(g)
5CO(g)+11H2(g)
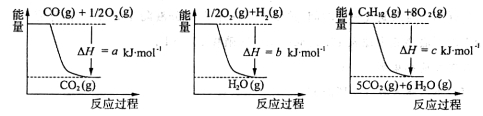
已知几个反应的能量变化如下图所示,则上述反应的△H=____________kJ·mol-1
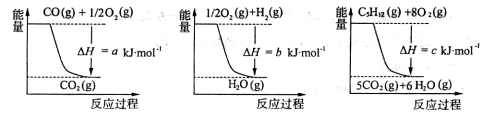
(2)合成氨的反应原理为:
3H2(g)+N2(g) 2NH3(g)
2NH3(g)
现有甲、乙、丙3个固定容积为2 L的密闭容器,在相同温度和催化剂条件下,按不同的反应物投入量进行合成氨反应,相关数据如下表所示:
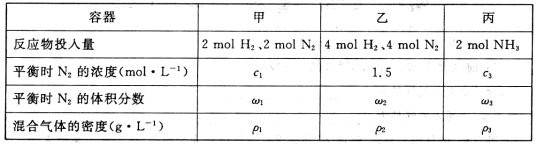
①下列描述不能说明该反应已达到平衡状态的是_____________.(填序号);
a.容器内混合气体的密度保持不变
b.3v正(N2)==v逆(H2)
c.容器内混合气体的平均相对分子质量保持不变
②乙容器中的反应在20 min后达到平衡,这段时间内NH3的平均反应速率v(NH3)=___________mol·L-1·min-1,该温度下,反应的平衡常数K=___________L2·mol-2(结果保留3位有效数字);
③分析上表中的数据,下列关系正确的是________(填序号)。
a.cl>c3 b.wl<w2 c. >
> >
>
(3)在合成氨工业中,为了提高反应物的利用率,除了要提供适宜的温度、压强和使用催化剂外,还要采取的措施是________。
-
氨是化肥工业和基本有机化工的主要原料,合成氨工业因此成为基本无机化工之一。回答下列问题:
(1)如何获得廉价的氢气是合成氨工业中的重要课题,目前常用戊烷跟水蒸气反应的方法获得氢气:C5H12(g)+5H2O(g) 5CO(g)+11H2(g)
5CO(g)+11H2(g)
已知几个反应的能量变化如下图所示,则上述反应的△H=__________kJ·mol-1
(2)合成氨的反应原理为:3H2(g)+N2(g) 2NH3(g)
2NH3(g)
现有甲、乙、丙3个固定容积为2 L的密闭容器,在相同温度和催化剂条件下,按不同的反应物投入量进行合成氨反应,相关数据如下表所示:
| 容器 | 甲 | 乙 | 丙 |
| 反应物投入量 | 2molH2、2molN2 | 4molH2、4molN2 | 2molNH3 |
| 平衡时N2的浓度(mol•L-1) | c1 | 1.5 | C3 |
| 平衡时N2的体积分数 | w1 | W2 | W3 |
| 混合气体的密度(g•L-1) | ρ1 | ρ2 | ρ3 |
①下列描述不能说明该反应已达到平衡状态的是_________.(填序号);
a.容器内混合气体的密度保持不变
b.3v正(N2)==v逆(H2)
c.容器内混合气体的平均相对分子质量保持不变
②乙容器中的反应在20 min后达到平衡,这段时间内NH3的平均反应速率v(NH3)=_________mol·L-1·min-1,该温度下,反应的平衡常数K=__________L2·mol-2(结果保留3位有效数字);
③分析上表中的数据,下列关系正确的是____________(填序号)。
a.cl>c3 b.wl<w2 c. >
> >
>
(3)在合成氨工业中,为了提高反应物的利用率,除了要提供适宜的温度、压强和使用催化剂外,还要采取的措施是__________。
-
(有机化学基础)胡椒乙酸是合成许多药用生物碱的重要中间体,以苯酚为原料制备胡椒乙酸的合成路线如图所示。
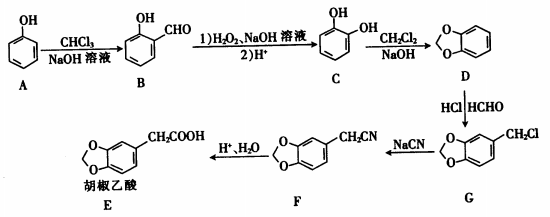
回答下列问题:
(1)下列关于有机物B的说法正确的是________(填字母)。
a.能与FeCl3溶液发生显色反应
b.核磁共振氢谱中只有3组峰
c.能发生银镜反应
d.能与溴水发生加成反应
(2)C的名称是__________,C→D的反应类型是__________。
(3)胡椒乙酸(E)中所含官能团的名称为______________。
(4)G生成F的化学方程式为____________。
(5)W是E的同分异构体,0.5molW与足量碳酸氢钠溶液反应生成1molCO2,已知W的苯环上只有2个取代基,则W的结构共有___________(不含立体异构)种,其中核磁共振氢谱有五组峰的结构简式为____________。
(6)参照上述合成路线,写出以一氯甲苯(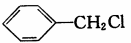 )为原料(无杌试剂任选)制备苯乙酸的合成路线:______________________。
)为原料(无杌试剂任选)制备苯乙酸的合成路线:______________________。
-
胡椒乙酸是合成许多药用生物碱的重要中间体,以苯酸为原料制备胡椒乙酸的合成路线如图所示。回答下列问题:
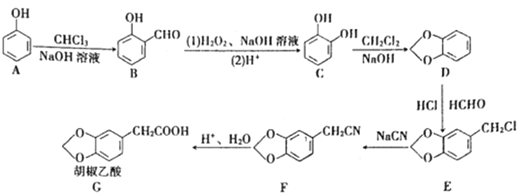
(1)下列关于有机物B的说法正确的是______ 填字母
填字母 。
。
a.能与FeCl3溶液发生显色反应 b.核磁共振氢谱中只有3组峰
c.能发生银镜反应 d.能与溴水发生加成反应
(2)有机物C的名称是______,C→D的反应类型是______。
(3)胡椒乙酸(G)的分子式为______,G所含官能团的名称为______。
(4)E生成F的化学方程式为______。
(5)W是G的芳香族化合物同分异构体,0.5mol W与足量碳酸氢钠溶液反应生成1molCO2,则W的结构共有______(不含立体异构)种,其中苯环上有2个取代基,且核磁共振氢谱有5组峰的结构简式为______。
-
胡椒乙酸是合成许多药用生物碱的重要中间体,以苯酚为原料制备胡椒乙酸的合成路线如图所示。
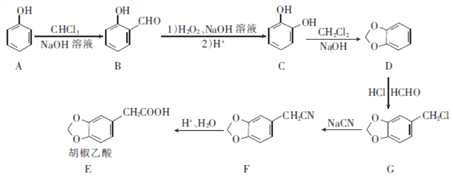
回答下列问题:
(1)下列关于有机物B的说法正确的是 ____________(填字母)。
a.能与FeCl3溶液发生显色反应
b.核磁共振氢谱中只有3组峰
c.能发生银镜反应
d.能与溴水发生加成反应
(2)C的名称是___________,C→D的反应类型是_______。
(3)胡椒乙酸(E)中所含官能团的名称为__________ 。
(4)G生成F的化学方程式为_____________。
(5)W是E的同分异构体,0.5 mol W与足量碳酸氢钠溶液反应生成1 mol C02,已知W的苯环上只有2个取代基,则W的结构共有__________(不含立体异构)种,其中核磁共振氢谱有五组峰的结构简式为_______。
(6)参照上述合成路线,写出以一氯甲苯( )为原料(无机试剂任选)制备苯乙酸的合成路线:____________________。
)为原料(无机试剂任选)制备苯乙酸的合成路线:____________________。
-
香料甲和G在生活中有很多用途,工业上利用有机物A( )来制备,其合成路线如图:
)来制备,其合成路线如图:
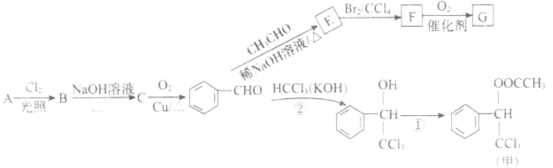
已知:

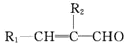
 、
、 代表烃基或氢原子
代表烃基或氢原子
回答下列问题:
(1)C的名称是______,F中官能团的名称是______。
(2)②的反应类型是______,E的结构简式为______。
(3)下列关于E的叙述正确的是______。
A.分子式为
B. 1mol最多能与 发生加成反应
发生加成反应
C. 自身能发生加聚、缩聚反应
D. 最多有9个碳原子位于同一平面
(4)C有多种同分异构体,其中属于芳香族化合物的有______种。
(5)写出反应①的化学方程式______。
(6)F的同分异构体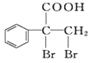 是一种重要的药物中间体,其合成路线与G相似,请以为原料设计它的合成路线
是一种重要的药物中间体,其合成路线与G相似,请以为原料设计它的合成路线 其他所需原料自选
其他所需原料自选 。____________
。____________
-
香料甲和G在生活中有很多用途,工业上利用有机物A( )来制备,其合成路线如下:
)来制备,其合成路线如下:
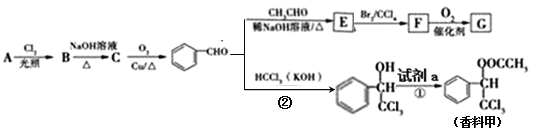
已知:R1—CHO+R2—CH2—CHO 
 (R1、R2代表烃基或氢原子)
(R1、R2代表烃基或氢原子)
回答下列问题:
(1)C的名称是____,G中官能团的名称是__________。
(2)②的反应类型是________,F的结构简式为_______________。
(3)下列关于C的叙述正确的是___________.
A. 分子式为C9H10O B. 1mol E最多能与5molH2发生加成反应
C. 自身能发生加聚、缩聚反应 D. 最多有9个碳原子位于同一平面
(4)C有多种同分异构体,其中属于芳香族化合物的有____种。
(5)写出反应①的化学方程式__________________________________。
(6)F的同分异构体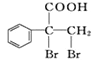 是一种重要的药物中间体,其合成路线与G相似,请以为原料设计它的合成路线(其他所需原料自选)。____________
是一种重要的药物中间体,其合成路线与G相似,请以为原料设计它的合成路线(其他所需原料自选)。____________
-
苯乙烯是工业上是合成树脂、离子交换树脂及合成橡胶等的重要单体,工业上可用乙苯催化脱氢方法制备苯乙烯: (g)
(g)
 (g)+H2(g) △H=+QkJ·mol-1
(g)+H2(g) △H=+QkJ·mol-1
请回答下列问题:
(1)已知乙苯(g)、苯乙烯(g)的燃烧热分别为a kJ·mol-1、bkJ·mol-1,则氢气的燃烧热为________kJ·mol-1(用含有Q、b、c的表达式表示,其中Q、b、c均大于0)。
(2)673 K时,在一恒容密闭容器中充入5 mol乙苯(g),反应达到平衡后容器内气体的压强为p1;若再充入amol的乙苯(g),重新达到平衡后容器内气体的压强为2p1,则a________5。
(3)在实际生产中,在恒压条件下常以高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),此时乙苯的平衡转化率与水蒸气的用量、压强(p)的关系如图所示。
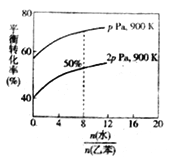
①加入水蒸气稀释剂能提高乙苯转化率的原因是___________________________。
②用平衡分压代替平衡浓度计算,其中,分压=总压×物质的量分数,则900K时的平衡常数Kp=________。
③改变下列条件,能使乙苯的反应速率和转化率一定增大的是________(填标号)。
A.恒容时加入稀释剂水蒸气 B.压强不变下,温度升至1500 K
C.在容积和温度不变下充入Ar D.选用催化效果更好的催化剂
(4)已知苯乙烯可催化氧化生成苯乙醛: (g)+2O2→
(g)+2O2→ + CO2+H2O,若把该反应设计为酸性燃料电池,则电池负极的电极反应式为_________________,若该电池消耗标准状况下11.2 L的O2,则外电路中理论上应转移电子的物质的量为________mol。
+ CO2+H2O,若把该反应设计为酸性燃料电池,则电池负极的电极反应式为_________________,若该电池消耗标准状况下11.2 L的O2,则外电路中理论上应转移电子的物质的量为________mol。
-
苯乙烯是工业上是合成树脂、离子交换树脂及合成橡胶等的重要单体,工业上可用乙苯催化脱氢方法制备苯乙烯: (g)
(g)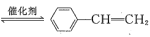 (g)+H2(g) △H=+QkJ·mol-1
(g)+H2(g) △H=+QkJ·mol-1
请回答下列问题:
(1)已知乙苯(g)、苯乙烯(g)的燃烧热分别为a kJ·mol-1、bkJ·mol-1,则氢气的燃烧热为_____kJ·mol-1(用含有Q、b、c的表达式表示,其中Q、b、c均大于0)。
(2)673 K时,在一恒容密闭容器中充入5 mol乙苯(g),反应达到平衡后容器内气体的压强为p1;若再充入amol的乙苯(g),重新达到平衡后容器内气体的压强为2p1,则a____________5。
(3)在实际生产中,在恒压条件下常以高温水蒸气作为反应体系的稀释剂(水蒸气不参加反应),此时乙苯的平衡转化率与水蒸气的用量、压强(p)的关系如图所示。
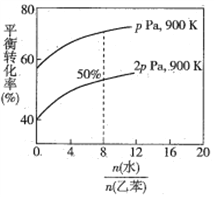
①加入水蒸气稀释剂能提高乙苯转化率的原因是________________________________。
②在实际生产过程中,当控制反应温度为900 K时生产效率最佳,选用此温度进行生产的原因为________ (答两点)。
③用平衡分压代替平衡浓度计算,其中,分压=总压×物质的量分数,则900K时的平衡常数Kp=_______。
④改变下列条件,能使乙苯的反应速率和转化率一定增大的是________ (填标号)。
A.恒容时加入稀释剂水蒸气 B.压强不变下,温度升至1500 K
C.在容积和温度不变下充入Ar D.选用催化效果更好的催化剂
(4)已知苯乙烯可催化氧化生成苯乙醛:  (g) + 2O2→
(g) + 2O2→ + CO2 + H2O,若把该反应设计为酸性燃料电池,则电池负极的电极反应式为___________________,若该电池消耗标准状况下11.2 L的O2,则外电路中理论上应转移电子的物质的量为________ mol。
+ CO2 + H2O,若把该反应设计为酸性燃料电池,则电池负极的电极反应式为___________________,若该电池消耗标准状况下11.2 L的O2,则外电路中理论上应转移电子的物质的量为________ mol。






 )为原料(无杌试剂任选)制备苯乙酸的合成路线:______________________。
)为原料(无杌试剂任选)制备苯乙酸的合成路线:______________________。



 是一种重要的药物中间体,其合成路线与G相似,请以为原料设计它的合成路线
是一种重要的药物中间体,其合成路线与G相似,请以为原料设计它的合成路线
 是一种重要的药物中间体,其合成路线与G相似,请以为原料设计它的合成路线(其他所需原料自选)。____________
是一种重要的药物中间体,其合成路线与G相似,请以为原料设计它的合成路线(其他所需原料自选)。____________
 (g)+H2(g) △H=+QkJ·mol-1
(g)+H2(g) △H=+QkJ·mol-1