常温下,用 0.1000 mol·L-1NaOH溶液滴定 20.00mL某未知浓度的CH3COOH溶液,滴定曲线如图所示。已知在点③处恰好中和。下列说法错误的是

A.该温度下CH3COOH的电离平衡常数约为1.8 ×10-5
B.点①处溶液中c(CH3COO-)<c(CH3COOH)
C.点③处溶液中c(OH-)= c(CH3COOH)+c(H+)
D.滴定过程中不可能出现:c(CH3COOH) >c(CH3COO-)> c(OH-)> c(Na+)> c(H+)
高二化学单选题中等难度题
常温下,用 0.1000 mol·L-1NaOH溶液滴定 20.00mL某未知浓度的CH3COOH溶液,滴定曲线如图所示。已知在点③处恰好中和。下列说法错误的是

A.该温度下CH3COOH的电离平衡常数约为1.8 ×10-5
B.点①处溶液中c(CH3COO-)<c(CH3COOH)
C.点③处溶液中c(OH-)= c(CH3COOH)+c(H+)
D.滴定过程中不可能出现:c(CH3COOH) >c(CH3COO-)> c(OH-)> c(Na+)> c(H+)
高二化学单选题中等难度题
常温下,用 0.1000 mol·L-1NaOH溶液滴定 20.00mL某未知浓度的CH3COOH溶液,滴定曲线如图所示。已知在点③处恰好中和。下列说法错误的是

A.该温度下CH3COOH的电离平衡常数约为1.8 ×10-5
B.点①处溶液中c(CH3COO-)<c(CH3COOH)
C.点③处溶液中c(OH-)= c(CH3COOH)+c(H+)
D.滴定过程中不可能出现:c(CH3COOH) >c(CH3COO-)> c(OH-)> c(Na+)> c(H+)
高二化学单选题中等难度题查看答案及解析
室温下,用0.1000 mol·L-1NaOH溶液滴定20.00 mL未知浓度的盐酸(酚酞作指示剂)的滴定曲线如图所示。下列说法正确的是( )
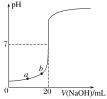
A.溶液中的氢离子浓度:a<b
B.盐酸的物质的量浓度为0.0100mol·L-1
C.指示剂变色时,说明盐酸与NaOH恰好完全反应
D.当滴加NaOH溶液10.00mL时(忽略反应前后体积变化),该混合液的pH=1+lg3
高二化学单选题中等难度题查看答案及解析
下图是用0.1000 mol·L-1NaOH溶液滴定20.00mL未知浓度盐酸(酚酞做指示剂)的滴定曲线。下列说法正确的是
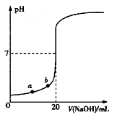
A.水电离出的氢离子浓度:a > b
B.盐酸的物质的量浓度为0.0100 mol·L-1
C.当指示剂由红色变为无色时,达滴定终点
D.当滴加NaOH溶液10.00 mL时,该混合液的pH= l+lg3
高二化学选择题简单题查看答案及解析
常温下,用0.1000mol·L-1盐酸滴定20.00mL未知浓度一元弱碱MOH溶液,滴定曲线如图所示。下列有关说法错误的是( )
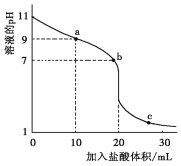
A.该一元碱溶液浓度为0.1000mol·L-1
B.a、b、c点水的电离程度逐渐增大
C.b点:c(M+)=c(Cl-)
D.常温下,MOH的电离常数Kb=1×10-5
高二化学单选题中等难度题查看答案及解析
常温下,用酚酞作指示剂,用 0.10mol·L-1NaOH 溶液分别滴定 20.00mL 浓度均为0.10mol·L-1的CH3COOH 溶液和 HCN 溶液所得滴定曲线如图。(已知电离平衡常数:CH3COOH> HCN)
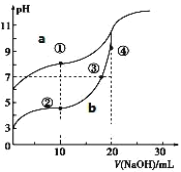
(1)图_____(a 或 b)是 NaOH 溶液滴定 HCN 溶液的 pH 变化的曲线。
(2)点③所示溶液中所含离子浓度的从大到小的顺序:_____ 。
(3)点①和点②所示溶液中:c(CH3COO-)-c(CN-)_____c(HCN)-c(CH3COOH)(填“>、<或=”)
(4)25 ℃时,用 0.1 mol·L-1的醋酸溶液滴定 20 mL 0.1 mol·L-1 的 NaOH 溶液,当滴加V mL 该醋酸溶液时, 混合溶液的 pH = 7 。已知醋酸的电离平衡常数为 Ka , 则Ka=________________
高二化学综合题中等难度题查看答案及解析
常温下,用0.10 mol·L—1NaOH溶液分别滴定20.00 mL浓度均为0.10 mol·L—1 CH3COOH溶液和HCN溶液所得滴定曲线如图。下列说法正确的是
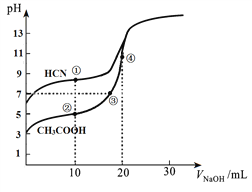
A. 点①和点②所示溶液中: c(CH3COO-)+c(CN-)=c(HCN)+c(CH3COOH)
B. 点③和点④所示溶液中:c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
C. 点①和点②所示溶液中:c(CH3COO-)>c(CN-)
D. 点②和点③所示溶液中都有:c(CH3COO-)+c(OH-)=c(CH3COOH)+c(H+)
高二化学单选题困难题查看答案及解析
常温下,用0.1000 mol·L-1NaOH溶液滴定20.00 mL 0.1000 mol·L-1HA溶液,滴定曲线如图。下列说法不正确的是
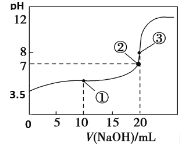
A.常温下,HA电离常数为1.0×10-6
B.点②所示溶液中:c(Na+)< c(HA)+c(A-)
C.点③所示溶液中:c(Na+)> c(A-)> c(OH-)>c(H+)
D.从点①到点③的滴定过程中,水的电离程度不变
高二化学单选题困难题查看答案及解析
常温下,用0.1000mol•L-1NaOH溶液滴定20.00mL 0.1000mol•L-1CH3COOH溶液所得滴定曲线如图:
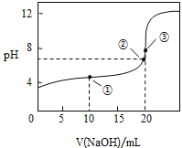
(1)在整个实验过程中,不需要的仪器是 ______ (填序号).
a.100mL容量瓶 b.锥形瓶 c.滴定管夹 d.漏斗 e.玻璃棒 f.滴定管
(2)点②所示溶液为中性:c(Na+)________c(CH3COO-)(填“>”“<”或“=”)。
(3)盛装标准NaOH溶液选择图中滴定管_________(填标号)。
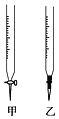
(4)滴定时边滴边摇动锥形瓶,眼睛应注意观察____________。
(5)下列操作会导致测定结果偏低的是______。
A.碱式滴定管在装液前未用标准NaOH溶液润洗
B.滴定过程中,锥形瓶摇荡得太剧烈,锥形瓶内有液滴溅出
C.碱式滴定管尖嘴部分在滴定前没有气泡,滴定终点时发现气泡
D.达到滴定终点时,仰视读数
(6)氧化还原滴定实验与酸碱中和滴定类似(用已知浓度的氧化剂溶液滴定未知浓度的还原剂溶液或反之)。测血钙的含量时,进行如下实验:
①可将4mL血液用蒸馏水稀释后,向其中加入足量草酸铵(NH4)2C2O4晶体,反应生成CaC2O4沉淀,将沉淀用稀硫酸处理得H2C2O4溶液。
②将①得到的H2C2O4溶液,再用酸性KMnO4溶液滴定,氧化产物为CO2,还原产物为Mn2+。
③终点时用去20mL l.0×l0-4mol/L的KMnO4溶液。
Ⅰ、滴定终点的现象是_________________________________。
Ⅱ、计算:血液中含钙离子的浓度为______mol/L。
高二化学实验题中等难度题查看答案及解析
常温下,用 0.1000mol•L-1NaOH溶液滴定 20.00mL 0.1000mol•L-1CH3COOH溶液所得滴定曲线如图.下列说法不正确的是
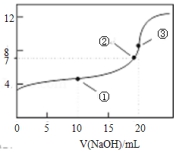
A.点①所示溶液中:c(CH3COO-)+c(CH3COOH)=2c(Na+)
B.点②所示溶液中:c(Na+)=c(CH3COO-)
C.点③所示溶液中:c(Na+)=c(CH3COOH)+c(CH3COO-)
D.滴定过程中可能出现:c(CH3COOH)>c(H+)>c(CH3COO-)>c(Na+)>c(OH-)
高二化学选择题中等难度题查看答案及解析
常温下,用0.10 mol·L—1NaOH溶液分别滴定20.00 mL浓度均为0.10 mol·L—1 CH3COOH溶液和HCN溶液所得滴定曲线如右图。下列说法正确的是

A. 点①和点②所示溶液中:c(CH3COO—)< c(CN—)
B. 点③和点④所示溶液中:c(Na+)>c(OH—) >c(CH3COO—) >c(H+)
C. 点①和点②所示溶液中:c(CH3COO—)-c(CN—) = c(HCN)- c(CH3COOH)
D. 点②和点③所示溶液中都有: c(CH3COO—)+c(OH—)= c(CH3COOH) +c(H+)
高二化学单选题中等难度题查看答案及解析