-
A、B、D、E、F、G六种元素的原子序数依次增大,除F、G为第四周期过渡元素外,其余四种均是短周期元素。已知:F的单质为生活中最常见的金属之一,原子最外层有2个电子;E原子的价电子排布为msnmpn,B原子的核外L层电子数为奇数;A、D原子p轨道的电子数分别为2和4;G基态原子的最外层电子半充满,内层全充满。请回答下列问题:
(1)F的稳定价态离子的电子排布式是___,A、B、D、E四种元素的第一电离能由大到小的顺序为__(用元素符号表示)。
(2)对于B的简单氢化物,其中心原子的轨道杂化类型是___,分子的立体构型为___,该氢化物易溶于D的简单氢化物的主要原因是___。
(3)D原子分别与A、B原子形成的单键中,键的极性较强的是___(用具体的化学键表示)。
(4)如图所示的晶胞是由A、D两元素组成的,下列有关该晶体的说法中正确的是__。
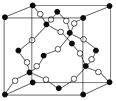
a.该晶体的化学式为AD
b.该晶体中A、D原子间形成的是双键
c.该晶体熔点可能比SiO2晶体高
d.该晶体可溶于水
(5)G的硫酸盐溶液滴加少量氨水的离子方程式为___,继续滴加过量氨水的离子方程式为___,再加一定体积乙醇溶液析出深蓝色晶体的化学式为___,该晶体中包含的化学键有___。
-
A、B、C为原子序数依次增大的同一周期短周期元素,已知A元素的单质既可与盐酸反应,又可与NaOH溶液反应,且均产生氢气;B元素原子次外层电子数比最外层电子数多3,C元素的单质溶于水具有漂白性。
①A元素的元素符号是__________,B的最高价氧化物的化学式为__________;
②B、C两种元素所形成的气态氢化物中最稳定的是__________(用化学式表示);
③写出A、C最高价氧化物对应水化物相互反应的离子方程式__________。
-
已知A、B、C、D、E、F、G为七种短周期主族元素,原子序数依次增大。已知:A、F的最外层电子数分别等于各自的电子层数,其中A的单质在常温下为气体。C与B、G在元素周期表中处于相邻位置,这三种元素原子的最外层电子数之和为17,质子数之和为31。D与F同周期,且在该周期中D元素的原子半径最大。根据以上信息回答下列问题:
(1)B、C、G的氢化物中稳定性最强的是__________(填化学式),G的某种氧化物能使溴水褪色,写出该反应的化学方程式__________________________________________。
(2)B、C、D、E、F形成的简单离子半径由大到小的顺序为__________________(用离子符号表示)。
(3)A与B能形成离子化合物A5B,A5B中既含离子键又含共价键,其电子式为________,该物质能与水剧烈反应生成两种气体,这两种气体的化学式是__________。
(4)D、A、C和碳元素组成的化合物的水溶液呈________性,用离子方程式解释其原因________________________________________________________。
-
已知A、B、C、D、E、F、G为七种短周期主族元素,原子序数依次增大。已知:A、F的最外层电子数分别等于各自的电子层数,其中A的单质在常温下为气体。C与B、G在元素周期表中处于相邻位置,这三种元素原子的最外层电子数之和为17,质子数之和为31。D与F同周期,且在该周期中D元素的原子半径最大。根据以上信息回答下列问题:
(1)B、C、G的氢化物中稳定性最强的是__________(填化学式),G的某种氧化物能使溴水褪色,写出该反应的化学方程式__________________________________________。
(2)B、C、D、E、F形成的简单离子半径由大到小的顺序为__________________(用离子符号表示)。
(3)A与B能形成离子化合物A5B,A5B中既含离子键又含共价键,其电子式为________,该物质能与水剧烈反应生成两种气体,这两种气体的化学式是__________。
(4)D、A、C和碳元素组成的化合物的水溶液呈________性,用离子方程式解释其原因________________________________________________________。
-
有A、B、C、D、E五种短周期元素,它们的原子序数依次增大。已知A和B原子具有相同的电子层数,且A的最外层电子数是次外层电子数的两倍,C是该周期中原子半径最大的元素,C的单质在加热下与B的单质充分反应,可以得到与D单质颜色相同的淡黄色固态化合物,E与D相邻。试根据以上叙述回答:
(1)元素符号:B______ ;C______ ; E______ ;
(2)画出D的离子结构示意图_______________;AB2的结构式_______________;
(3)写出 C2B2与AB2反应的化学方程式___________________________________________;在该反应中,1mol C2B2参与反应,则转移电子数目为______;
(4)D、E的气态氢化物的稳定性_________大于_________ (填化学式)。
-
结构决定性质,性质决定用途;已知X、Y、Z、W是元素周期表中短周期中的四种非金属元素,它们的原子序数依次增大,X元素的原子形成的阳离子就是一个质子,Z、W在元素周期表中处于相邻的位置,Z的单质在常温下均为无色气体,W原子的最外层电子排布是nSn npn+2,Y原子的最外层电子数是内层电子数的2倍。试回答:
(1)写出W元素的元素符号和该原子基态的电子排布式:__ _____
(2)写出Z元素的原子结构示意图和该原子基态的电子排布图:_ _____
(3)X单质和Z单质在一定条件下反应生成化合物E,则E的电子式是:________。E可以进行喷泉实验的主要原因是:________。
(4)仅由X、Z、W三种元素组成的某种盐是一种速效肥料,但长期施用会使土壤酸化,有关的离子反应方程式为___________ __________________ ________
(5)这四种元素可组成原子个数比为5∶1∶1∶3的化合物(按X、Y、Z、W的顺序)为(写名称)________,该化合物的浓溶液与足量NaOH热浓溶液反应的离子方程式为:____________ __ __
-
已知短周期的主族元素X、Y、Z、W、M的原子序数依次增大,X是空气中含量最
多的元素,其单质的化学性质非常稳定,Y原子的最外层只有2个电子,Z单质可制成半导体材料,W元素形成的单质为淡黄色的固体,M元素形成的单质为黄绿色气体.请回答以下问题:
(1)X元素的符号是 ,它在周期表的位置为 ;
(2)Z的氧化物晶体类型为 ,化学式是: ;
(3)X与Y能形成离子化合物,该化合物的电子式为 ;
(4)X的最高价氧化物的水化物与Y的氧化物反应的化学方程式为 ;
(5)X、W形成的氢化物分别为甲和乙,且甲、乙所含的电子数相等,则甲的结构式为 ;
(6)W和M都是较活泼的非金属元素,用实验事实表明这两种元素的非金属性强弱(用方程式书写或文字说明) 。
-
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素C、D原子的最外层上均有一个未成对电子。下列说法正确的是
A.C、D分别与E形成的化合物的晶体类型相同
B.B与E形成的分子BE4为非极性分子
C.一定条件下,元素C、D的最高价氧化物对应的水化物之间能发生反应
D.化合物AE与CE含有相同类型的化学键
-
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素C、D原子的最外层上均有一个未成对电子.下列说法正确的是( )
A.C、D分别与E形成的化合物的晶体类型相同
B.B与E形成的分子BE4为非极性分子
C.一定条件下,元素C、D的最高价氧化物对应的水化物之间能发生反应
D.化合物AE与CE含有相同类型的化学键
-
已知A、B、C、D、E是短周期中原子序数依次增大的5种主族元素,其中元素A、E的单质在常温下呈气态,元素B的原子最外层电子数是其电子层数的2倍,元素C在同周期的主族元素中原子半径最大,元素C、D原子的最外层上均有一个未成对电子。下列说法正确的是
A.C、D分别与E形成的化合物的晶体类型相同
B.B与E形成的分子BE4为非极性分子
C.一定条件下,元素C、D的最高价氧化物对应的水化物之间能发生反应
D.化合物AE与CE含有相同类型的化学键
