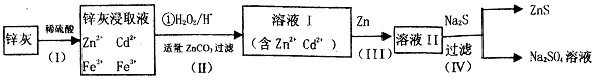-
一种利用含AgCl的废渣制取AgNO3的工艺流程如下:
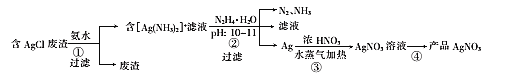
(1)步骤①用氨水浸取时,温度不宜超过35℃,其原因是 ___。在氨水浓度、固液质量比和温度均一定时,为提高银的浸取率还可采取的措施是____;浸取时发生反应的离子方程式为____。
(2)步骤②中发生反应的离子方程式为______。
(3)步骤③中,银与浓硝酸反应生成等物质的量的NO和NO2,当消耗了10.8g Ag时,有______molHNO3参与了反应。
(4)步骤④的操作为______,100℃下烘干得产品AgNO3。
(5)上述流程中发生了氧化还原反应的步骤有______(用“①”“②”“③”“④”填空)。
-
硫化锌 是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取,其工艺流程如图所示。
是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取,其工艺流程如图所示。
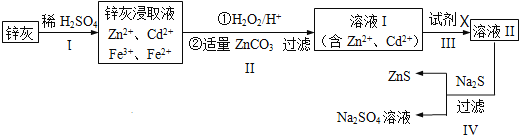
 为提高锌灰的浸取率,不宜采用的方法是______
为提高锌灰的浸取率,不宜采用的方法是______ 填序号
填序号 。
。
 研磨
研磨  多次浸取
多次浸取  升高温度
升高温度  加压
加压  搅拌
搅拌
 步骤Ⅱ中
步骤Ⅱ中 的作用是______,所得滤渣的主要成分是______
的作用是______,所得滤渣的主要成分是______ 写化学式
写化学式 。
。
 步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂X应为______。
步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂X应为______。
 步骤Ⅳ还可以回收
步骤Ⅳ还可以回收 来制取
来制取 。
。
 检验ZnS固体是否洗涤干净的方法是______。
检验ZnS固体是否洗涤干净的方法是______。
 可由等物质的量的
可由等物质的量的 和
和 在高温、催化剂条件下制取,化学反应方程式为______。
在高温、催化剂条件下制取,化学反应方程式为______。
 若步骤Ⅱ加入的
若步骤Ⅱ加入的 为b mol,步骤Ⅲ所得Cd为d mol,最后得到V L,c
为b mol,步骤Ⅲ所得Cd为d mol,最后得到V L,c  的
的 溶液。则理论上所用锌灰中含有锌元素的质量为______。
溶液。则理论上所用锌灰中含有锌元素的质量为______。
-
硫化锌 (ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取,其工艺流程如下图所示。
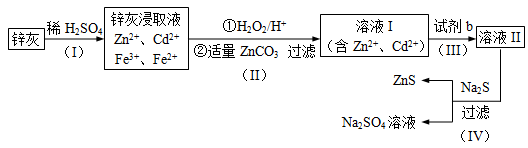
(1)为提高锌灰的浸取率,可采用的方法是 (填序号)。
①研磨 ②多次浸取 ③升高温度 ④加压 ⑤搅拌
(2)步骤Ⅱ所得滤渣中的物质是 (写化学式)。
(3)步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂b应为____________。
(4)步骤Ⅳ还可以回收Na2SO4来制取Na2S。
①检验ZnS固体是否洗涤干净的方法是 ;
②Na2S可由等物质的量的Na2SO4和CH4在高温、催化剂条件下制取。化学反应方程式为________;
③已知Na2SO4·10H2O及Na2SO4的溶解度随温度变化曲线如图。从滤液中得到Na2SO4·10H2O的操作方法是 。
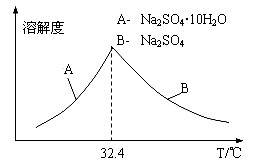
(5)若步骤Ⅱ加入的ZnCO3为b mol,步骤Ⅲ所得Cd为d mol,最后得到VL、物质的量浓度为c mol/L的Na2SO4溶液。则理论上所用锌灰中含有锌元素的质量为____________。
-
硫化锌(ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取t,其工艺流程如下图所示。
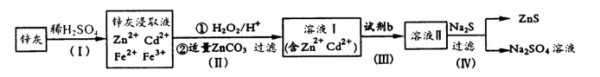
(1)为提高锌灰的浸取率,可采用的方法是 (填序号)。
①研磨 ②多次浸取 ③升高温度 ④加压 ⑤搅拌
(2)步骤Ⅱ所得滤渣中的物质是 (写化学式)。
(3)步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂b应为____________。
(4)步骤Ⅳ还可以回收Na2SO4来制取Na2S。
①检验ZnS固体是否洗涤干净的方法是 ,
②Na2S可由等物质的量的Na2SO4和CH4在高温、催化剂条件下制取。化学反应方程式为______________;
③已知Na2SO4.10H2O及Na2SO4的溶解度随温度变化曲线如图。从滤液中得到Na2SO4.10H2O的操作方法是________________。
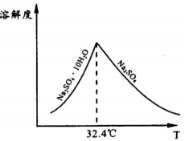
(5)若步骤Ⅱ加入的ZnCO3为b mol,步骤Ⅲ所得Cd为d mol,最后得到VL、物质的量浓度为c mol/L的Na2SO4溶液。则理论上所用锌灰中含有锌元素的质量为____________。
-
硫化锌(ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取,其工艺流程如下图所示。
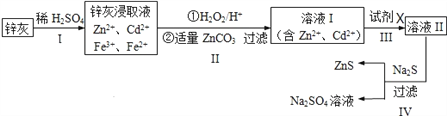
(1)为提高锌灰的浸取率,可采用的方法是____________(填序号)。
①研磨 ②多次浸取 ③升高温度 ④加压 ⑤搅拌
(2)步骤Ⅱ所得滤渣中的物质是_______________(写化学式)。
(3)步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂X应为____________。
(4)步骤Ⅳ还可以回收Na2SO4来制取Na2S。
①检验ZnS固体是否洗涤干净的方法是_________________。
②Na2S可由等物质的量的Na2SO4和CH4在高温、催化剂条件下制取。化学反应方程式为_______________________________;
(5)若步骤Ⅱ加入的ZnCO3为bmol,步骤Ⅲ所得Cd为dmol,最后得到VL、物质的量浓度为cmol/L的Na2SO4溶液。则理论上所用锌灰中含有锌元素的质量为____________。
-
硫化锌(ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取t其工艺流程如下图所示。
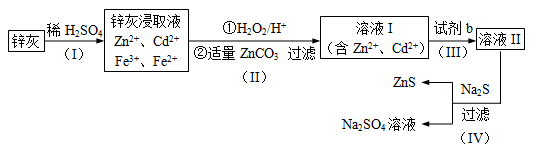
(1)为提高锌灰的浸取率,可采用的方法是____________(填序号)。
①研磨 ②多次浸取 ③升高温度 ④加 压 ⑤搅拌
压 ⑤搅拌
(2)步骤Ⅱ所得滤渣中的物质是_______________(写化学式)。
(3)步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂b应为____________ 。
(4)步骤Ⅳ还可以回收Na2SO4来制取Na2S。
①检验ZnS固体是否洗涤干净的方法是______________,
②Na2S可由等物质的量的Na2S04和CH4在高温、催化剂条件下制取。化学反应方式为_________________;
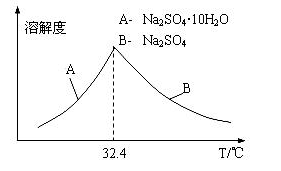
③已知Na2SO4.10H2O及Na2SO4的溶解度随温度变化曲线如图。从滤液中得到Na2SO4.10H2O的操作方法是________________________.
(5)若步骤Ⅱ加入的ZnCO3为b mol,步骤Ⅲ所得Cd为d mol,最后得到VL、物质的量浓度为c mol/L的Na2SO4溶液。则理论上所用锌灰中含有锌元素的质量为______________。
-
硫化锌(ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取其工艺流程如图所示.
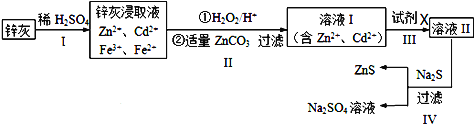
(1)为提高锌灰的浸取率,可采用的方法是______________(填序号)。
①研磨 ②多次浸取 ③升高温度 ④加压 ⑤搅拌
(2)步骤Ⅱ所得滤渣中的物质是(写化学式)_____________。
(3)步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂X应为________。
(4)步骤Ⅳ还可以回收Na2SO4来制取Na2S。
①检验ZnS固体是否洗涤干净的方法是__________________;
②Na2S可由等物质的量的Na2SO4和CH4在高温、催化剂条件下制取,化学反应方程式为_______;
③已知Na2SO4·10H2O及Na2SO4的溶解度随温度变化曲线如图,从滤液中得到Na2SO4·10H2O的操作方法是_________________________________。
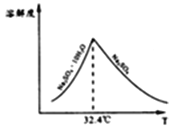
(5)若步骤Ⅱ加入的ZnCO3为b mol,步骤Ⅲ所得Cd为d mol,最后得到VL、物质的量浓度为c mol/L的Na2SO4溶液.则理论上所用锌灰中含有锌元素的质量为__________。
-
【化学——选修2化学与技术】硫化锌(ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取,其工艺流程如下图所示。
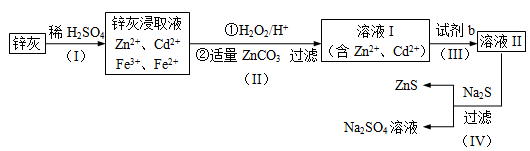
(1)为提高锌灰的浸取率,可采用的方法是 (填序号)。
①研磨 ②多次浸取 ③升高温度 ④加压 ⑤搅拌
(2)步骤Ⅱ所得滤渣中的物质是 (写化学式)。
(3)步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂b应为____________。
(4)步骤Ⅳ还可以回收Na2SO4来制取Na2S。
①检验ZnS固体是否洗涤干净的方法是 ,
②Na2S可由等物质的量的Na2SO4和CH4在高温、催化剂条件下制取。化学反应方程式为_______________________________;
③已知Na2SO4·10H2O及Na2SO4的溶解度随温度变化曲线如图。从滤液中得到Na2SO4·10H2O的操作方法是 。
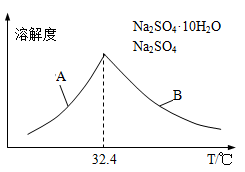
(5)若步骤Ⅱ加入的ZnCO3为b mol,步骤Ⅲ所得Cd为d mol,最后得到VL、物质的量浓度为c mol/L的Na2SO4溶液。则理论上所用锌灰中含有锌元素的质量为____________。
-
硫化锌(ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取,其工艺流程如下图所示。
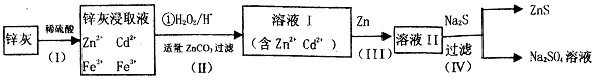
(1)为提高锌灰的浸取率,可采用的方法是___________(填序号)。
① 研磨 ② 多次浸取 ③ 升高温度 ④ 加压 ⑤ 搅拌
(2)步骤II中加入ZnCO3的作用是________、___________(用离子方程式表示),所得滤渣中的物质是________(写化学式)。
(3)步骤IV还可以回收Na2SO4来制取Na2S及Na2SO4·10H2O。
①等物质的量的Na2SO4和CH4在高温、催化剂条件下可以制取Na2S,化学反应方程式为___________;
②已知Na2SO4·10H2O及Na2SO4的溶解度随温度变化曲线如图所示。从滤液中得到Na2SO4·10H2O晶体的操作方法是______________。
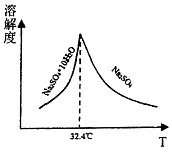
(4)若步骤II加入的ZnCO3为bmol,步骤Ⅲ所得Cd为dmol,最后得到VL、物质的量浓度为cmol/L的Na2SO4溶液。则理论上所用锌灰中含有锌元素的质量为________。
-
【化学―选修2:化学与技术】硫化锌是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取,其工艺流程如下图所示。
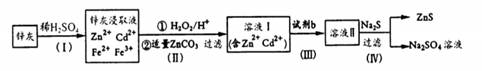
(1)为提高锌灰的浸取率,可采用的方法是_________(填序号)。
①研磨 ②多次浸取 ③升高温度 ④加压 ⑤搅拌
(2)步骤Ⅱ所得滤渣中的物质是 ______(写化学式)。
(3)步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂b应为__________。
(4)步骤Ⅳ还可以回收Na2SO4来制取Na2S。
①检验ZnS固体是否洗涤干净的方法是 ___________,
②Na2S可由等物质的量的Na2S04和CH4在高温、催化剂条件下制取。化学反应方程式为__________;
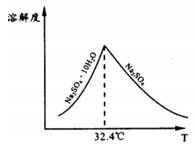
③已知Na2SO4.10H2O及Na2SO4的溶解度随温度变化曲线如右图。从滤液中得到Na2SO4.10H2O的操作方法是____________。
(5)若步骤Ⅱ加入的ZnCO3为b mol,步骤Ⅲ所得Cd为d mol,最后得到VL、物质的量浓度为c mol/L的Na2SO4溶液。则理论上所用锌灰中含有锌元素的质量为___________。