用下列方法均可制得氯气:①MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O②KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。若要制得相同质量的氯气,①②③反应中电子转移数目之比为( )
A.15∶5∶3 B.1∶3∶5 C.6∶5∶6 D.1∶6∶10
高二化学单选题中等难度题
用下列方法均可制得氯气:①MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O②KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。若要制得相同质量的氯气,①②③反应中电子转移数目之比为( )
A.15∶5∶3 B.1∶3∶5 C.6∶5∶6 D.1∶6∶10
高二化学单选题中等难度题
用下列方法均可制得氯气:①MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O②KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O③2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O。若要制得相同质量的氯气,①②③反应中电子转移数目之比为( )
A.15∶5∶3 B.1∶3∶5 C.6∶5∶6 D.1∶6∶10
高二化学单选题中等难度题查看答案及解析
实验室所用少量氯气是用下列方法制取的
4HCl(浓)+MnO2 == Cl2↑+ MnCl2+2H2O
该反应氧化剂是________,氧化产物是________,
离子方程式________。
高二化学填空题简单题查看答案及解析
实验室制取O2和Cl2的化学反应方程式分别为①2KClO32KCl+3O2↑ ②MnO2+4HCl(浓)
MnCl2+Cl2↑+2H2O,则( )
A. ①中,反应前后MnO2化学性质改变
B. ②中,MnO2为催化剂
C. ①中,反应前后MnO2质量不发生变化
D. ②中,MnO2为氧化剂
高二化学选择题中等难度题查看答案及解析
实验室制氯气的化学方程式为:MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O,现用足量浓盐酸在加热条件下跟150g含MnO2的软锰矿石反应(杂质不参加反应),制得的氯气在标准
状况下体积为33.6L。求:
(1)参加反应的HCl的物质的量
(2)这种软锰矿石中MnO2的质量分数
(3)化合价改变的氯元素的质量
高二化学计算题困难题查看答案及解析
如图是一套制取并验证氯气部分化学性质的实验装置.
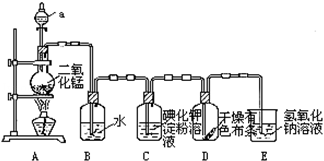
回答下列问题:反应的方程式:MnO2+4HCl(浓)MnCl2+2H2O+Cl2↑
(1)装置A中,仪器a的名称叫 ,该仪器中盛有的试剂为 .
(2)当Cl2气流通过一段时间后,装置B中溶液的pH值 7(填“>”“<”或“=”),写出Cl2与水反应的方程式
(3)当有少量Cl2气流通过后,观察到装置C中的溶液变为 色,反应的离子方程式为 .
(4)当Cl2气流持续通过时,装置D中干燥的有色布条能否褪色?为什么? .
(5)装置E的作用是 .
高二化学实验题困难题查看答案及解析
实验室制取氯气的反应为:MnO2 + 4HCl(浓) MnCl2 + Cl2↑+ 2H2O,回答下列问题:
⑴该反应中的氧化剂是___________(填写物质的化学式);
⑵8.7g的二氧化锰和足量的浓盐酸反应,制得的氯气在标准状况下的体积为________L。
⑶用200mL 8moL/L的浓盐酸与足量的二氧化锰加热时反应,得到氯气的量_______0.4mol(填写“>”、“=”或“<”)。
高二化学填空题中等难度题查看答案及解析
(18分)某化学研究性学习小组设计制取氯气及探究其性质的方案,并按下图所示装置完成实验。(A中发生反应的化学方程式为:MnO2 + 4HCl(浓) ==== MnCl2 + Cl2↑ + 2H2O)
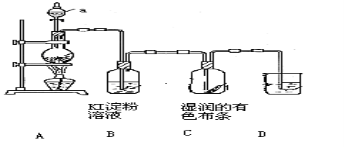
【实验探究】
(1)装置A中,仪器a的名称是 。
(2)装置B中无色溶液将变为 色,该反应的化学方程式是 。
(3)装置C中湿润的有色布条 (填“褪色”或“不褪色”),其原因是氯气与水反应生成了 (填化学式)
(4)为了吸收多余的氯气,防止造成空气污染,装置D中应盛放 ____溶液(填“NaOH”或“H2SO4”)
(5)用8.7gMnO2与足量浓盐酸反应,理论上可以生成标准状况下的Cl2 _______L。
【知识拓展】
(6)某同学查阅资料得知:高锰酸钾与浓盐酸在常温下也可以生成氯气(反应的化学方程式为:
2KMnO4 + 16HCl(浓) ==== 2KCl + 2MnCl2 + 5Cl2↑ + 8H2O),该反应的氧化剂是 (填“KMnO4”或“HCl”)
【知识应用】
(7)洪灾过后,饮用水的消毒杀菌是抑制大规模传染疾病爆发的重要措施之一。请你列举一例对饮用水进行消毒杀菌的合理方法:______________________________________________________________________
高二化学实验题中等难度题查看答案及解析
实验室用一定量MnO2固体与足量浓盐酸在加热条件下充分反应制取2.24L标准状况下的氯气,其反应的化学方程式为:MnO2+4HCl(浓)MnCl2+Cl2↑+2H2O,,(相对原子质量O-16,Mn-55)
试计算:
(1)参加反应的MnO2的质量____________;
(2)反应后溶液的体积为100mL,溶液中MnCl2的物质的量浓度____________。
高二化学计算题简单题查看答案及解析
(10分)某化学研究性学习小组设计制取氯气及探究其性质的方案,并按下图所示装置完成实验。(A中发生反应的化学方程式为:MnO2 + 4HCl(浓) ====MnCl2 + Cl2↑ + 2H2O)
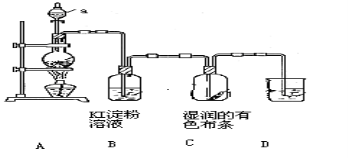
【实验探究】
(1)装置A中,仪器a的名称是 。
(2)装置B中无色溶液将变为 色,该反应的化学方程式是 。
(3)装置C中湿润的有色布条 (填“褪色”或“不褪色”),其原因是氯气与水反应生成了 (填化学式)
(4)为了吸收多余的氯气,防止造成空气污染,装置D中应盛放 溶液。
高二化学实验题中等难度题查看答案及解析
实验室制备氯气的反应原理为:
MnO2+4HCl( 浓)MnCl2+Cl2↑+2H2O
(1)上述反应中的氧化剂是_____________,还原剂是________________;
(2)通常状况下,氯气是一种__________色的气体;
(3)下图为实验室制取氯气的装置图,烧杯中盛装的试剂是________________;
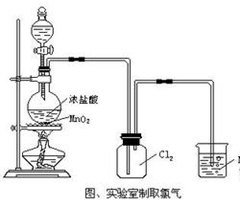
(4)将湿润的红色布条放入盛有氯气的集气瓶中,可以观察到红色布条_____________;
(5)将氯气通入KI溶液时,发生反应的离子方程式______________________________;
(6)若反应中消耗0.2mol MnO2,则生成的氯气在标准状况下的体积为____________L。
高二化学填空题中等难度题查看答案及解析