-
硼及其化合物在工业上有许多用途。工业上以铁硼矿为原料制备硼酸,铁硼矿含有Mg、Fe、Ca、Al、B、O等多种元素,它的主要成分为Mg2B2O5·H2O和Fe3O4。
(1)铁元素位于元素周期表中的第 族,在水溶液中常以Fe2+、Fe3+的形式存在,其中 更稳定。
(2)以硼酸为原料可制得NaBH4 ,B原子的杂化方式为 。
(3)工业上冶炼铝不用氯化铝,因为氯化铝易升华,其双聚物Al2Cl6结构如图所示。1mol该分子中含 个配位键,该分子 (填“是”或“否”)平面型分子。
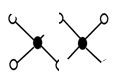
(4)Al单质为面心立方晶体,其晶胞的边长a=0.405nm,列式表示Al单质的密度:____g·cm-3。
-
硼及其化合物在工业上有许多用途。工业上以铁硼矿为原料制备硼酸,铁硼矿含有Mg、Fe、Ca、Al、B、O等多种元素,它的主要成分为Mg2B2O5·H2O和Fe3O4。
(1)铁元素位于元素周期表中的第 族,在水溶液中常以Fe2+、Fe3+的形式存在,其中 更稳定。
(2)以硼酸为原料可制得NaBH4 ,B原子的杂化方式为 。
(3)工业上冶炼铝不用氯化铝,因为氯化铝易升华,其双聚物Al2Cl6结构如图所示。1mol该分子中含 个配位键,该分子 (填“是”或“否”)平面型分子。
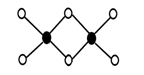
(4)Al单质为面心立方晶体,其晶胞的边长a=0.405nm,列式表示Al单质的密度:_________g·cm-3。
-
[化学——选修5物质结构与性质]
硼及其化合物在工业上有许多用途。工业上以铁硼矿为原料制备硼酸,铁硼矿含有Mg、Fe、Ca、Al、B、O等多种元素,它的主要成分为Mg2B2O5·H2O和Fe3O4。
(1)基态铁原子的外围电子层排布为 ,该元素位于元素周期表中的第 族,在水溶液中常以Fe2+、Fe3+的形式存在,其中 更稳定。
(2)以硼酸为原料可制得NaBH4, B原子的杂化方式为 。
(3)工业上冶炼铝不用氯化铝,因为氯化铝易升华,其双聚物Al2Cl6结构如图所示。1mol该分子中含 个配位键,该分子 (填“是”或“不是”)平面型分子。
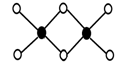
(4)依据第二周期元素第一电离能的变化规律,参照图中B、C、O、F元素的位置,用小黑点表示N元素的相对位置。
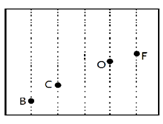
(5)Al单质为面心立方晶体,其晶体参数a=0.405nm,列式表示Al单质的密度: g·cm-3。
-
硼及其化合物在工业上有许多用途。工业上以铁硼矿为原料制备硼酸,铁硼矿含有Mg、Fe、Ca、Al、B、O等多种元素,它的主要成分为Mg2B2O5•H2O和Fe3O4。
(1)基态铁原子的外围电子层排布为_____________,该元素位于元素周期表中的第_____________族,在水溶液中常以Fe2+、Fe3+的形式存在,其中_____________更稳定。
(2)以硼酸 为原料可制得NaBH4,B原子的杂化方式为_____________。
为原料可制得NaBH4,B原子的杂化方式为_____________。
(3)第ⅤA族元素的原子R与A原子结合形成RA3气态分子,其立体结构呈三角锥形。RCl5在气态和液态时,分子结构如图所示,下列关于RCl5分子的说法中不正确的是( )
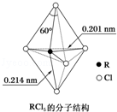
A.分子中5个R﹣Cl键键能不都相同
B.键角(Cl﹣R﹣Cl)有90°、120、180°几种
C.RCl5受热后会分解生成分子立体结构呈三角锥形的RCl3
D.每个原子都达到8电子稳定结构
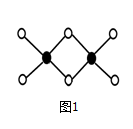
(4)因为氯化铝易升华,其双聚物Al2Cl 6结
6结 构如图1所示。1mol该分子中含__________个配位键,该分子________(填“是”或“否”)平面型分子。
构如图1所示。1mol该分子中含__________个配位键,该分子________(填“是”或“否”)平面型分子。
(5)纯叠氮酸(HN3)在常温下是一种液体,沸点较高,为308.8 K,主要原因是_________。
(6)二硫化碳属于_________(填“极性”或“非极性”)分子。
-
硼及其化合物在工业上有许多用途.工业上以铁硼矿为原料制备硼酸,铁硼矿含有Mg、Fe、Ca、Al、B、O等多种元素,它的主要成分为Mg2B2O5•H2O和Fe3O4.
(1)基态铁原子的外围电子层排布为______________,该元素位于元素周期表中的第______________族,在水溶液中常以Fe2+、Fe3+的形式存在,其中______________更稳定.
(2)以硼酸为原料可制得NaBH4,B原子的杂化方式为______________。
(3) 第ⅤA族元素的原子R与A原子结合形成RA3气态分子,其立体结构呈三角锥形.RCl5在气态和液态时,分子结构如图所示,下列关于RCl5分子的说法中不正确的是( )
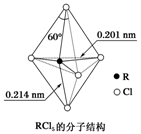
A.分子中5个R-Cl键键能不都相同
B.键角(Cl-R-Cl)有90°、120、180°几种
C.RCl5受热后会分解生成分子立体结构呈三角锥形的RCl3
D.每个原子都达到8电子稳定结构
(4)因为氯化铝易升华,其双聚物Al2Cl6结构如图1所示.1mol该分子中含______________个配位键,该分子______________(填“是”或“否”)平面型分子.
(5)纯叠氮酸(HN3)在常温下是一种液体,沸点较高,为308. 8 K,主要原因是______________。
(6)二硫化碳属于_____________ (填“极性”或“非极性”)分子。
-
硼及其化合物在工业上有许多用途。以铁硼矿(主要成分为Mg2B2O5·H2O和Fe3O4,还有少量Fe2O3、FeO、CaO、Al2O3和SiO2等)为原料制备硼酸(H3BO3)的工艺流程如图所示:
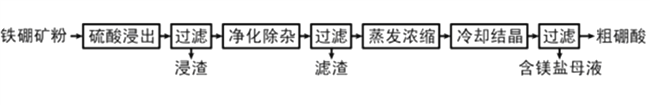
回答下列问题:
(1)写出Mg2B2O5·H2O与硫酸反应生成硼酸(H3BO3)的化学方程式_____________。为提高浸出速率,除适当增加硫酸的浓度外,还可采取的措施有_________(写出两条)。
(2)利用_______的磁性,可将其从“矿粉”中分离。“浸渣”中的物质是______(写化学式)。
(3) “净化除杂”需先加H2O2溶液,作用是(用离子方程式表示)_______。然后再调节溶液的pH约为5,目的是________。
(4)以硼酸为原料可制得硼氢化钠(NaBH4),它是有机合成中的重要还原剂,其电子式为_______。
-
锑(Sb)及其化合物在工业上有许多用途。以辉锑矿(主要成分为Sb2S3,还含有PbS、As2S3、CuO、SiO2等)为原料制备金属锑的工艺流程如图所示:
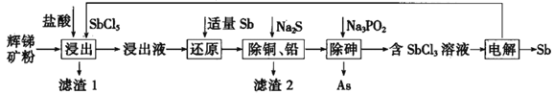
已知:① 浸出液中除含过量盐酸和SbCl5之外,还含有SbCl3、PbCl2、AsCl3、CuCl2等;
②常温下:Ksp(CuS)=1.27×10-36,Ksp(PbS)=9.04×10-29;
③溶液中离子浓度小于等于1.0×10-5mol·L-1时,认为该离子沉淀完全。
(1)滤渣1中除了S之外,还有___________(填化学式)。
(2)“浸出”时,Sb2S3发生反应的化学方程式为_________________。
(3)“还原”时,被Sb还原的物质为_____________(填化学式)。
(4)常温下,“除铜、铅”时,Cu2+和Pb2+均沉淀完全,此时溶液中的c(S2-)不低于______;所加Na2S也不宜过多,其原因为_____________。
(5)“除砷”时有H3PO3生成,该反应的离子方程式为________________。
(6)“电解”时,被氧化的Sb元素与被还原的Sb元素的质量之比为_______。
-
锑(Sb)及其化合物在工业上有许多用途。以辉锑矿(主要成分为Sb2S3,还含有PbS、As2S3、CuO、SiO2等)为原料制备金属锑的工艺流程如图所示:
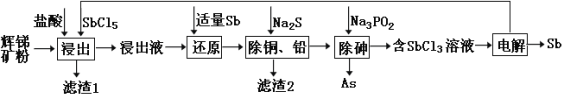
已知:① 浸出液中除含过量盐酸和SbCl5之外,还含有SbCl3、PbCl2、AsCl3、CuCl2等;
②常温下:Ksp(CuS)=1.27×10-36,Ksp(PbS)=9.04×10-29;
③溶液中离子浓度小于或等于1.0×10-5mol/L时,认为该离子沉淀完全。
(1)滤渣1中除了S之外,还有___________(填化学式)。
(2)“浸出”时,Sb2S3发生反应的化学方程式为_________。
(3)该生产流程能实现(填化学式)的循环利用__________。
(4)常温下,“除铜、铅”时,Cu2+和Pb2+均沉淀完全,此时溶液中的c(S2-)不低于______。
(5)“电解”时,被氧化的Sb元素与被还原的Sb元素的质量之比为_______。
-
锑(Sb)及其化合物在工业上有许多用途。以辉锑矿(主要成分为Sb2S3,还含有 PbS、As2S3、CuO、SiO2等)为原料制备金属锑的工艺流程如图所示:
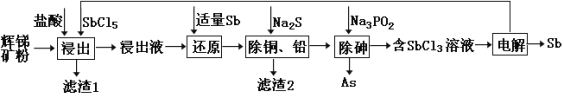
已知:① 浸出液中除含过量盐酸和SbCl5之外,还含有SbCl3、PbCl2、AsCl3、CuCl2等;
②常温下:Ksp(CuS)=1.27×10-36,Ksp(PbS)=9.04×10-29;
③溶液中离子浓度小于或等于1.0×10-5mol/L时,认为该离子沉淀完全。
(1)滤渣1中除了S之外,还有___________(填化学式)。
(2)“浸出”时,Sb2S3发生反应的化学方程式为_________。
(3)该生产流程能实现(填化学式)的循环利用 __________。
(4)常温下,“除铜、铅”时,Cu2+和Pb2+均沉淀完全,此时溶液中的c(S2-)不低于______。
所加Na2S也不宜过多,其原因为______________。
(5)“除砷”时有H3PO3生成,该反应的离子方程式为__________。
(6)“电解”时,被氧化的Sb元素与被还原的Sb元素的质量之比为_______。
-
铜及其化合物在工业生产上有许多用途。某工厂以辉铜矿(主要成分为 Cu2S,含少量 Fe2O3、SiO2 等杂质)为原料制备不溶于水的碱式碳酸铜的流程如下:
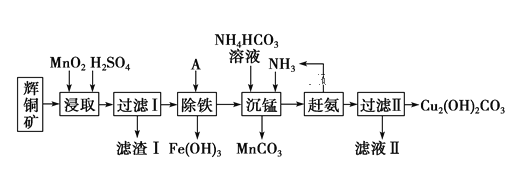
已知:
①常温下几种物质开始形成沉淀与完全沉淀时的pH如下表
| 金属离子 | Fe2+ | Fe3+ | Cu2+ | Mn2+ |
| 开始沉淀 | 7.5 | 2.7 | 5.6 | 8.3 |
| 完全沉淀 | 9.0 | 3.7 | 6.7 | 9.8 |
②Ksp[Fe(OH)3]=4.0×10-38
(1)加快“浸取”速率,除将辉铜矿粉碎外,还可采取的措施有______________________(任写一种)。
(2)常温下“除铁”时加入的试剂A可用CuO等,调节pH调的范围为_____________,若加 A 后溶液的 pH调为5,则溶液中 Fe3+的浓度为_____________mol/L。
(3)写出“沉锰”(除 Mn2+)过程中反应的离子方程式:____________________。
(4)“赶氨”时,最适宜的操作方法是______________________。











