-
某研究小组由Cu(NO3)2溶液先制得Cu(NO3)2·3H2O晶体,然后在下图所示实验装置中(夹持及控温装置省略),用Cu(NO3)2·3H2O晶体和SOCl2制备少量无水Cu(NO3)2。已知:SOCl2的熔点为-105℃、沸点为76℃、遇水剧烈水解生成两种酸性气体。
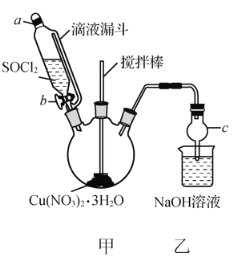
(1)由Cu(NO3)2溶液制得Cu(NO3)2·3H2O晶体的实验步骤包括蒸发浓缩、冷却结晶、抽滤等步骤。
①蒸发浓缩时当蒸发皿中出现______________________________(填现象)时,停止加热。
②为得到较大颗粒的Cu(NO3)2·3H2O晶体,可采用的方法是_______________(填一种)。
(2)①仪器c的名称是________。
②向三颈烧瓶中缓慢滴加SOCl2时,需打开活塞________(填“a”或“b”或“a和b”)。
(3)装置甲中Cu(NO3)2·3H2O和SOCl2发生反应的化学方程式为__________________________________。
(4)装置乙的作用是______________________________________。
-
某研究小组设计如图所示实验装置(夹持及控温装置省略),用Cu(NO3)2 • 3H2O晶体和SOCl2制备少量无水Cu(NO3)2。已知SOC12熔点-l05℃、沸点76℃、遇水剧烈水解生成两种酸性气体。 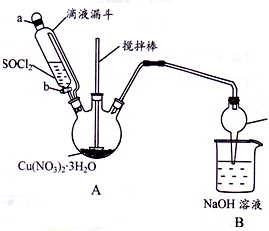 .
.
(1)①仪器c的名称是_________________。
②向三颈烧瓶中缓慢滴加SOC12时,需打开活塞_________(选填“a”、“b”或“a 和 b”)。
(2)装置A中Cu(NO3)2 • 3H2O和SOC12发生反应的化学方程式是________________。
(3)装置B的作用是________________。
(4)实验室以含铁的铜屑为原料制备Cu(NO3)2 • 3H2O的实验方案如下:
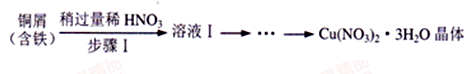
己知几种离子生成氢氧化物沉淀的pH如下表
| 开始沉淀的pH | 沉淀完全的pH |
| Fe3+ | 1.1 | 3.2 |
| Fe2+ | 5.8 | 8.8 |
| Cu2+ • | 4.2 | 6.7 |
①步骤I中所用稀HNO3稍过量的目的是_____________。
②请补充完整由溶液I制备Cu(NO3)2 • 3H2O晶体的实验方案:
向溶液I中加入__________,冰水洗涤得到Cu(NO3)2 • 3H2O晶体。
-
某研究小组在实验室以含铁的铜屑为原料制备Cu(NO3)2·3H2O晶体,并进一步探究用SOCl2制备少量无水Cu(NO3)2。设计的合成路线如下:

已知:Cu (NO3)2·3H2O  Cu(NO3)2·Cu(OH)2
Cu(NO3)2·Cu(OH)2  CuO
CuO
SOCl2熔点 -105℃、沸点76℃、遇水剧烈水解生成两种酸性气体。 请回答:
(1)第③步包括蒸发浓缩、冷却结晶、抽滤等步骤,其中蒸发浓缩的具体操作是_______。
(2)第④步中发生反应的化学方程式是_____________。
(3)第④步,某同学设计的实验装置示意图(夹持及控温装置省略,如图1有一处不合理,请提出改进方案并说明理由_______________。

(4)为测定无水Cu(NO3)2产品的纯度,可用分光光度法。
已知:4NH3·H2O + Cu2+ == Cu(NH3)42+ + 4H2O;Cu(NH3)42+ 对特定波长光的吸收程度(用吸光度A表示)与Cu2+ 在一定浓度范围内成正比。现测得Cu(NH3)42+的吸光度A与Cu2+ 标准溶液浓度关系如图2所示:准确称取0.3150g无水Cu(NO3)2,用蒸馏水溶解并定容至100 mL,准确移取该溶液10.00mL,加过量NH3 ·H2O,再用蒸馏水定容至100 mL,测得溶液吸光度A=0.620,则无水Cu(NO3)2产品的纯度是_________(以质量分数表示)。
-
硫代硫酸钠是一种重要的化工产品。某兴趣小组制备硫代硫酸钠晶体 的实验装置如下图所示(省略夹持装置):
的实验装置如下图所示(省略夹持装置):
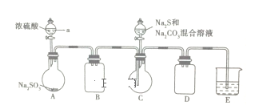
主要实验步骤为:①检查装置气密性,按图示加入试剂;②先向C中烧瓶加入 和
和 混合溶液,再向A中烧瓶滴加浓硫酸;③待
混合溶液,再向A中烧瓶滴加浓硫酸;③待 和
和 完全消耗后,结束反应。过滤C中混合物,滤液经一系列实验操作后得到产品。
完全消耗后,结束反应。过滤C中混合物,滤液经一系列实验操作后得到产品。
已知:i 是无色透明晶体,易溶于水,其稀溶液与
是无色透明晶体,易溶于水,其稀溶液与 溶液混合无沉淀生成;ii向
溶液混合无沉淀生成;ii向 和
和 混合溶液中通入
混合溶液中通入 可制得
可制得 所得产品常含有少量
所得产品常含有少量 和
和 。
。
回答下列问题:
(1)仪器a的名称是____________;B、D装置的作用是_____________。
(2)上述实验步骤③中的操作主要有_______________、冷却结晶、过滤、洗涤、干燥;E中的试剂是_____________。
(3)为检验产品中是否含有 和
和 ,该小组设计了以下实验方案(所需试剂从稀硝酸、稀硫酸、稀盐酸、蒸馏水中选择),请将方案补充完整:
,该小组设计了以下实验方案(所需试剂从稀硝酸、稀硫酸、稀盐酸、蒸馏水中选择),请将方案补充完整:
取适量产品配成稀溶液,滴加足量 溶液,有白色深沉生成,向沉淀中滴加足量的_________,若____________(填实验现象),则可以确定产品中含有
溶液,有白色深沉生成,向沉淀中滴加足量的_________,若____________(填实验现象),则可以确定产品中含有 和
和 。
。
(4)为减少装置C中生成 的量,在不改变原有装置的基础上对实验步骤②需进行改进,具体操作是_________________;写出制备
的量,在不改变原有装置的基础上对实验步骤②需进行改进,具体操作是_________________;写出制备 的总反应的化学方程式:___________________________。
的总反应的化学方程式:___________________________。
-
印刷电路板是由有机复合材料和铜箔复合构成,刻制印刷电路时,要用FeCl3溶液作为“腐蚀液”,研究其制备及性质是一个重要的课题。
(1)氯化铁晶体的制备(夹持及加热装置省略)

①实验过程中装置甲中发生反应的离子方程式_________________________________。
②为顺利达成实验目的,上述装置中甲中活塞、乙中活塞、弹簧夹1、2、3打开和关闭的顺序为__________。
③反应结束后,将乙中溶液边加入___________,边进行加热浓缩、___________、过滤、洗涤、干燥即得到产品。
(2)氯化铁的性质探究:
已知:①氯化铁的熔点为306℃、沸点为315℃,易升华,气态FeCl3会分解成FeCl2和Cl2②FeCl2熔点670℃)
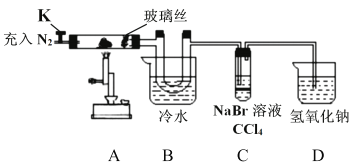
| 操作步骤 | 实验现象 | 解释原因 |
| 打开K,充入氮气 | D中有气泡产生 | ①充入N2的原因___________ |
| 关闭K,加热至600℃,充分灼烧固体 | B中出现棕黄色固体 | ②产生现象的原因___________。 |
| 实验结束,振荡C静置 | ③___________ | ④___________(用方程式解释) |
-
某研究小组在实验室以含铁的铜屑为原料制备Cu(NO3)2·H2O晶体,并进一步探究用SOCl2制备少量无水Cu(NO3)2。设计的合成路线如下:

已知:Cu(NO3)2·3H2O  Cu(NO3)2·Cu(OH)2
Cu(NO3)2·Cu(OH)2  CuO
CuO
SOCl2熔点―105℃、沸点76℃、遇水剧烈水解生成两种酸性气体。
请回答:
(1)第②步调pH适合的物质是_________(填化学式)。
(2)第③步包括蒸发浓缩、冷却结晶、抽滤等步骤,其中蒸发浓缩的具体操作是_____________。为得到较大颗粒的Cu(NO3)2·3H2O晶体,可采用的方法是___________(填一种)。
(3)第④步中发生反应的化学方程式是_______________________。
(4)第④步,某同学设计的实验装置示意图(夹持及控温装置省略,如图)有一处不合理,请提出改进方案并说明理由___________________。
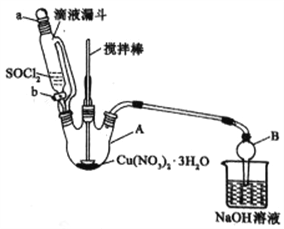
装置改进后,向仪器A中缓慢滴加SOCl2时,需打开活塞______(填“a”、“b”或“a和b”)。
(5)为测定无水Cu(NO3)2产品的纯度,可用分光光度法。
已知:4NH3·H2O + Cu2+ == Cu(NH3)42+ + 4H2O;Cu(NH3)42+ 对特定波长光的吸收程度(用吸光度A表示)与Cu2+ 在一定浓度范围内成正比。现测得Cu(NH3)42+的吸光度A与Cu2+ 标准溶液浓度关系如图所示:

准确称取0.3150g无水Cu(NO3)2,用蒸馏水溶解并定容至100 mL,准确移取该溶液10.00mL,加过量NH3·H2O,再用蒸馏水定容至100 mL,测得溶液吸光度A=0.620,则无水Cu(NO3)2产品的纯度是_________(以质量分数表示)。
-
某研究小组在实验室以含铁的铜屑为原料制备Cu(NO3)2·H2O晶体,并进一步探究用SOCl2制备少量无水Cu(NO3)2。设计的合成路线如下:

已知:Cu(NO3)2·3H2O  Cu(NO3)2·Cu(OH)2
Cu(NO3)2·Cu(OH)2  CuO
CuO
SOCl2熔点―105℃、沸点76℃、遇水剧烈水解生成两种酸性气体。
请回答:
(1)第②步调pH适合的物质是_________(填化学式)。
(2)第③步包括蒸发浓缩、冷却结晶、抽滤等步骤,其中蒸发浓缩的具体操作是_____________。为得到较大颗粒的Cu(NO3)2·3H2O晶体,可采用的方法是___________(填一种)。
(3)第④步中发生反应的化学方程式是_______________________。
(4)第④步,某同学设计的实验装置示意图(夹持及控温装置省略,如图)有一处不合理,请提出改进方案并说明理由___________________。
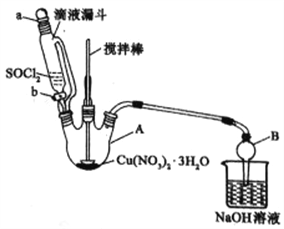
装置改进后,向仪器A中缓慢滴加SOCl2时,需打开活塞______(填“a”、“b”或“a和b”)。
(5)为测定无水Cu(NO3)2产品的纯度,可用分光光度法。
已知:4NH3·H2O + Cu2+ == Cu(NH3)42+ + 4H2O;Cu(NH3)42+ 对特定波长光的吸收程度(用吸光度A表示)与Cu2+ 在一定浓度范围内成正比。现测得Cu(NH3)42+的吸光度A与Cu2+ 标准溶液浓度关系如图所示:
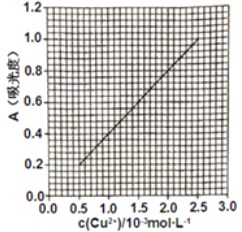
准确称取0.3150g无水Cu(NO3)2,用蒸馏水溶解并定容至100 mL,准确移取该溶液10.00mL,加过量NH3·H2O,再用蒸馏水定容至100 mL,测得溶液吸光度A=0.620,则无水Cu(NO3)2产品的纯度是_________(以质量分数表示)。
-
某研究小组在实验室以含铁的铜屑为原料制备Cu(NO3)2•3H2O晶体,并进一步探究用SOCl2制备少量无水Cu(NO3)2.设计的合成路线如下:

已知:①Cu(NO3)2•3H2O Cu(NO3)2•Cu(OH)2
Cu(NO3)2•Cu(OH)2 CuO
CuO
②SOCl2熔点﹣105℃、沸点76℃、遇水剧烈水解生成两种酸性气体、水解强烈放热,
请回答:
(1)Cu与足量稀HNO3反应的化学方程式_____
(2)第②步调pH适合的物质是_____(填化学式).
(3)第③步包括蒸发浓缩、冷却结晶、过滤等步骤,其中蒸发浓缩的具体操作是_____.为得到较大颗粒的Cu(NO3)2•3H2O晶体,可采用的方法是_____(填一种).
(4)第④步中发生的反应化学方程式是_____.
(5)第④步,某同学设计的实验装置示意图(如图1)有一处不合理,请提出改进方案并说明理由:_____;装置改进后,向仪器A中缓慢滴加SOCl2时,需打开活塞_____(填“a”、“b”或“a和b”).反应过程中,可能会因温度过高而有副反应,写出两种有效措施_____、_____.
(6)为测定无水Cu(NO3)2产品的纯度,可用分光光度法.
已知:4NH3•H2O+Cu2+═Cu(NH3)42++4H2O;Cu(NH3)42+对特定波长光的吸收程度(用吸光度A表示)与Cu2+在一定浓度范围内成正比.现测得Cu(NH3)42+的吸光度A与Cu2+标准溶液浓度关系如图2所示:

准确称取0.315 0g无水Cu(NO3)2,用蒸馏水溶解并定容至100mL,准确移取该溶液10.00mL,加过量NH3•H2O,再用蒸馏水定容至100mL,测得溶液吸光度A=0.600,则无水Cu(NO3)2产品的纯度是_____(以质量分数表示).
-
实验室用稀硝酸与铜反应制备 NO气体及硝酸铜晶体[Cu(NO3)2·3H2O],需经过铜与稀硝酸反应、收集 NO、尾气处理、制取硝酸铜晶体四个步骤,下列图示装置和原理能达到实验目的的是
A.用装置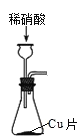 制取
制取  和 NO
和 NO
B.用装置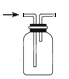 收集 NO
收集 NO
C.用装置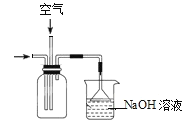 吸收尾气
吸收尾气
D.用装置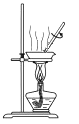 蒸干溶液制 Cu(NO3)2·3H2O
蒸干溶液制 Cu(NO3)2·3H2O
-
某研究小组在实验室以含铁的铜屑为原料制备Cu(NO3)2·3H2O晶体,并进一步探究用SOCl2制备少量无水Cu(NO3)2。设计的合成路线如下:
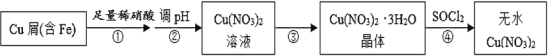
已知:SOCl2 熔点-105℃、沸点76℃、遇水剧烈水解生成两种酸性气体。请回答:
(1)写出第②步调 pH适合的一种物质______(填化学式),调 pH 后需进行的操作是_____。
(2)第③步包括蒸发浓缩、冷却结晶、抽滤等步骤,其中蒸发浓缩的具体操作是将溶液转移至蒸发皿中,缓缓加热至______。
(3)第④步中发生反应的化学方程式是______。
(4)第④步,某同学设计的实验装置示意图(如图,夹持及控温装置省略)有一处不合理,请提出改进方案并说明理由_______。
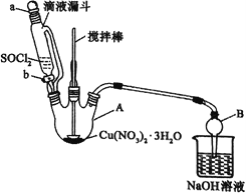
装置改进后,向仪器 A 中缓慢滴加 SOCl2 时,需打开活塞_____(填“a”“b”或“a 和 b”)。
(5)Cu(NO3)2·3H2O在170℃可失去结晶水变成Cu(NO3)2,若加热时间过长,Cu(NO3)2则会分解为一种黑色的固体,一种红棕色气体和另一种单质气体,写出反应的化学方程式:_______。
(6)为测定无水Cu(NO3)2 产品的纯度,可用分光光度法。
已知:4NH3·H2O+Cu2+=Cu(NH3)42++4H2O;Cu(NH3)42+对特定波长光的吸收程度(用吸光度A表示)与 Cu2+在一定浓度范围内成正比。现测得Cu(NH3)42+的吸光度A与 Cu2+标准溶液浓度关系如图所示:

准确称取0.3150g无水Cu(NO3)2,用蒸馏水溶解并定容至100mL,准确移取该溶液10.00mL,加过量NH3·H2O,再用蒸馏水定容至100mL,测得溶液吸光度A=0.620,则无水Cu(NO3)2产品的纯度是_______(以质量分数表示)。

 .
.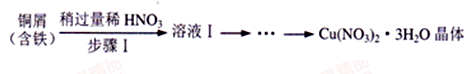














 制取
制取  收集 NO
收集 NO 吸收尾气
吸收尾气 蒸干溶液制 Cu(NO3)2·3H2O
蒸干溶液制 Cu(NO3)2·3H2O

