-
某原电池总反应为:Cu+2Fe3+==Cu2++2Fe2+ 下列能实现该反应的原电池是( )
A
B
C
D
电极材料
Cu、Zn
Cu、Ag
Cu、C
Fe、Zn
电解液
FeCl3
Fe2(SO4)3
Fe(NO3)2
CuSO4
A.A B.B C.C D.C
高一化学单选题中等难度题查看答案及解析
-
某电池总反应为 2Fe3++Cu=2Fe2++Cu2+,不能实现该反应的原电池是
A. 电极材料 Fe、Cu,电解质溶液 FeCl3 溶液
B. 电极材料石墨、Cu,电解质溶液 Fe2(SO4)3 溶液
C. 电极材料 Pt、Cu,电解质溶液 FeCl3 溶液
D. 电极材料 Ag、Cu,电解质溶液 Fe2(SO4)3 溶液
高一化学选择题中等难度题查看答案及解析
-
某电池总反应为 2Fe3++Cu=2Fe2++Cu2+,不能实现该反应的原电池是
A.电极材料 Fe、Cu,电解质溶液 FeCl3 溶液
B.电极材料石墨、Cu,电解质溶液 Fe2(SO4)3 溶液
C.电极材料 Pt、Cu,电解质溶液 FeCl3 溶液
D.电极材料 Ag、Cu,电解质溶液 Fe2(SO4)3 溶液
高一化学单选题简单题查看答案及解析
-
设计一个原电池来实现反应:2Fe3++Cu==2Fe2++Cu2+,下列各选项中,电极和电解质溶液选择均正确的是
选项
负极材料
正极材料
电解质溶液
A
Fe
Cu
Fe(NO3)2
B
Cu
Pt
FeCl2
C
Fe
石墨
Fe2(SO4)3
D
Cu
石墨
FeCl3
A.A B.B C.C D.D
高一化学单选题简单题查看答案及解析
-
Ⅰ、某同学根据离子方程式:2Fe3++Cu===2Fe2++Cu2+设计了一套原电池装置,从而实现了该反应。在下面画出该原电池的示意简图(正极材料为碳棒,标明正、负极及电极材料和电解质溶液)。
II 、锌锰干电池是应用最普遍的电池之一(如图所示),其基本反应为:
X极:Zn—2e-====Zn2+
Y极:2MnO2+2NH4++2e-====Mn2O3+2NH3+H2O
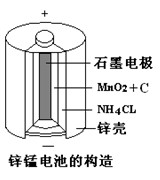
Y极是电池的_________(填“正”或“负”)极,若反应消耗16.25gZn,则电池中转移电子 的物质的是为________________。
高一化学填空题简单题查看答案及解析
-
某化学兴趣小组利用反应:Cu+2Fe3+=Cu2++2Fe2+设计的原电池实验装置如图。请回答下列问题:
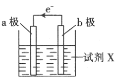
(1)b极发生___(填“氧化”或“还原”)反应,其电极材料为___,b电极反应式为:____。
(2)a极为____(填“正极”或“负极”),其电极材料可能为___,a极的电极反应式为____。
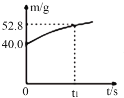
(3)该电池放电过程中,若测得电解质溶液的质量与时间的关系如图所示,则反应从开始至t1时,电路中转移电子的物质的量为_______mol。
高一化学解答题简单题查看答案及解析
-
Fe3+具有较强的氧化性,可以将Cu氧化为Cu2+,即: 2Fe3+ + Cu = 2Fe2+ + Cu2+,请将该反应设计成原电池:①画出原电池的装置图;②标出正、负极和电解质溶液;③并写出电极反应式。
高一化学计算题简单题查看答案及解析
-
原电池的发明是化学对人类的一项重大贡献。依据氧化还原反应:Cu+2Fe3+=2Fe2++Cu2+设计的原电池如图所示。
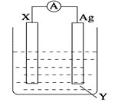
(1)电极X的材料是__;电解质溶液Y是__。
(2)Ag电极上发生的反应为:__。
高一化学填空题简单题查看答案及解析
-
关于如图所示各装置的叙述中,正确的是

A. 装置①是原电池,总反应是:Cu+2Fe3+=Cu2++2Fe2+
B. 装置①中,铁作负极,电极反应式为:Fe3++e-=Fe2+
C. 装置②通电一段时间后石墨Ⅱ电极附近溶液红褐色加深
D. 若用装置③精炼铜,则d极为粗铜,c极为纯铜,电解质溶液为CuSO4溶液
高一化学单选题中等难度题查看答案及解析
-
(1)理论上讲,任何自发的氧化还原反应都可以设计成原电池。请利用反应“Cu+2Fe3+=Cu2++2Fe2+”设计一个原电池(正极材料用碳棒),回答下列问题:
该电池的负极材料是___,发生___反应(填“氧化”或“还原”);电解质溶液是___;若导线上转移电子1mol,则被氧化的物质___克。
(2)已知拆开1molH—H键、1molN≡N分别需要吸收的能量为akJ、bkJ,形成1molN—H键需要释放ckJ能量。且已知N2和H2合成NH3的反应是放热反应,则生成1molNH3需要放出___的热量。
(3)铜与一定量浓硝酸恰好完全反应,得到硝酸铜溶液和NO2、N2O4、NO的混合气体,将这些气体与1.68LO2(标准状况)混合后通入水中,所有气体完全被水吸收生成硝酸,若向所得硝酸铜溶液中加入6mol·L-1NaOH溶液至Cu2+恰好完全沉淀,消耗NaOH溶液的体积是___mL。
高一化学综合题中等难度题查看答案及解析