-
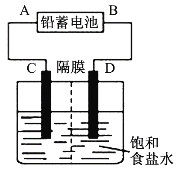
如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。
铅蓄电池充、放电时的电池反应为:Pb+PbO2+2H2SO4 2PbSO4+2H2O
2PbSO4+2H2O
(1)铅蓄电池放电时的正极反应为___。
(2)请写出电解饱和食盐水的化学方程式:____。
(3)若在电解池C极一侧滴入几滴酚酞溶液,电解一段时间后溶液变红色,说明铅蓄电池的A极为___极。
(4)用铅蓄电池电解1L饱和食盐水(食盐水足量、密度为1.15g·cm-3)时,
①若收集到11.2L(标准状况下)氯气,则至少转移电子____mol。
②若铅蓄电池消耗2molH2SO4,则可收集到H2的体积(标准状况下)为___L。
③若蓄电池消耗amol硫酸,电解后除去隔膜,所得溶液中NaOH的质量分数表达式为(假设氯气和氢气全部排出)___(用含a的代数式表示)。
-
如图是以铅蓄电池为电源,模拟氯碱工业电解饱和食盐水的装置图(C、D均为石墨电极)。电解一段时间后,若在电解池中C极一侧出来的气体无色无味,D极一侧出来的气体呈黄绿色有刺激性气味。请回答以下问题:

(1)已知铅蓄电池在放电时发生的反应:Pb+PbO2+4H++2SO42-=2PbSO4+2H2O,则A极为电源的_________极(填“正”或“负”),电极反应为___________________________;
(2)电解饱和食盐水的离子反应方程式是__________________;
(3)电极C的电极反应是_____________________________________________;
(4)电解时为防止两种气体产物混合,用阳离子交换膜做隔膜。则电解时Na+从______极区移向_____极区(填“C”或“D”);
(5)若电路上有0.2mol电子的电量通过,则铅蓄电池中消耗硫酸_________mol。
-
用酸性氢氧燃料电池电解饱和食盐水的装置如图所示 (a、b为石墨电极)。下列说法中,正确的是

A.电池工作时,正极反应式为:O2 +2 H2O + 4e-= 4OH-
B.电解时,a 电极周围首先放电的是Cl—
C.电解时,电子流动路径是:负极→外电路→阴极→溶液→阳极→正极
D.忽略能量损耗,当电池中消耗0.2g H2 时,b极周围会产生2.24L H2
-
实验室用铅蓄电池作电源电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应:负极:Pb + SO42- → PbSO4 + 2e 正极:PbO2 + 4H+ + SO42- + 2e → PbSO4 + 2H2O若为电解池提供0.1mol电子,这时电池内消耗的H2SO4的物质的量至少是( )
A、0.025mol B、0.050mol C、0.10mol D、0.20mol
-
实验室用铅蓄电池作电源电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应:负极Pb+SO42- ====PbSO4+2e-,正极PbO2+4H++SO42-+2e-===PbSO4+2H2O今若制得Cl2 0.050mol,这时电池内消耗的H2SO4的物质的量至少是( )
A. 0.025 mol B. 0.050 mol C. 0.10 mol D. 0.20 mol
-
实验室用铅蓄电池作电源电解饱和食盐水制取Cl2,已知铅蓄电池放电时发生如下反应:负极:Pb+SO-2e-===PbSO4 正极:PbO2+4H++SO+2e-===PbSO4+2H2O今欲制得Cl2 0.050 mol,这时电池内消耗的H2SO4的物质的量至少是( )
A.0.025 mol B.0.050 mol C.0.100 mol D.0.20 mol
-
实验室用铅蓄电池作电源电解饱和食盐水制取Cl2,已知铅蓄电池放电时发生如下反应:负极:Pb+SO -2e-=PbSO4,正极:PbO2+4H++SO
-2e-=PbSO4,正极:PbO2+4H++SO +2e-=PbSO4+2H2O。今欲制得Cl2 0.050 mol,这时电池内消耗的H2SO4的物质的量至少是( )
+2e-=PbSO4+2H2O。今欲制得Cl2 0.050 mol,这时电池内消耗的H2SO4的物质的量至少是( )
A.0.025 mol B.0.050 mol
C.0.10 mol D.0.20 mol
-
实验室用铅蓄电池作电源电解饱和食盐水制取Cl2,已知铅蓄电池放电时发生如下反应:
负极:Pb+SO42—-2e-=PbSO4
正极:PbO2+4H++SO42—+2e-=PbSO4+2H2O
今欲制得Cl2 0.050 mol, 这时电池内消耗的H2SO4的物质的量至少是( )。
A.0.025 mol B.0.050 mol C.0.10 mol D.0.20 mol
-
(12分)如图所示,某同学设计了一个燃料电池并探究氯碱工业原理和粗铜的精炼原理,其中乙装置中X为阳离子交换膜。请按要求回答相关问题:
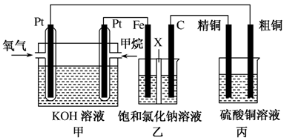
(1)甲烷燃料电池负极反应式是 ;
(2)石墨(C)极的电极反应式为 ;
(3)若在标准状况下,有2.24 L氧气参加反应,则乙装置中铁极上生成 的气体体积为________L ,丙装置中阴极析出铜的质量为________g ;
(4)某同学利用甲烷燃料电池设计电解法制取漂白液或Fe(OH)2的实验装置(如图所示)。
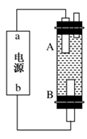
若用于制漂白液,a为电池的________极,电解质溶液最好用________;若用于制Fe(OH)2,使用硫酸钠作电解质溶液,阳极选用________作电极。
-
实验室用蓄电池电解饱和食盐水制取氯气,已知铅蓄电池放电时发生如下反应:负极:Pb+SO42-= PbSO4+2e- 正极:PbO2+4H++SO42-+2e-= PbSO4+2H2O,今若制得0.05 mol Cl2,这时电池内消耗的H2SO4的物质的量至少是( )
A.0.025 mol B.0.050 mol C.0.10 mol D.0.20 mol

2PbSO4+2H2O



