-
氧化铍(BeO)常温下为不溶于水、易溶于强酸和强碱的固体,除用作耐火材料外,还可以用于制霓虹灯和铍合金。工业上以硅铍石(主要含有BeO、SiO2、MgO,还含有少量Al2O3和Fe2O3)制备高纯度BeO的流程如图所示:
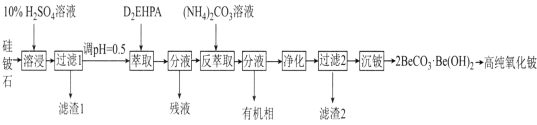
已知:①BeO为离子化合物,熔点为2350℃,BeC12和NaC1等比例混合的固体混合物在350℃即可熔化;
②不同金属阳离子在D2EHPA中的溶解性如下表所示:
| Be2+ | Mg2+ | Fe3+ | Al3+ |
| D2EHPA中的溶解性 | 易溶 | 难溶 | 微溶 | 微溶 |
请回答下列问题:
(1)“滤渣1”的主要成分为__(填化学式)。“残液”中含量最多的金属元素为__(填名称)。
(2)“萃取”后铍元素以Be(HX2)2的形式存在于有机相中,“反萃取”后以(NH4)2Be(CO3)2的形式存在于水相中,则“反萃取”时含铍微粒发生反应的化学方程式为___。
(3)“净化”时需将反萃取液加热到70℃,加热到70℃的目的为__。
(4)由2BeCO3·Be(OH)2制备高纯BeO的方法是__。
(5)BeO的电子式为__。工业上常采用电解熔融BeC12与NaC1等比例混合物的方法制备金属Be,不采用电解熔融BeO制备的主要原因为___。
-
下列说法不正确的是
A.“光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关
B. 可作阻燃剂,因此可以用于灭火
可作阻燃剂,因此可以用于灭火
C. 可用于制造光导纤维,其性质稳定,不溶于强酸、强碱
可用于制造光导纤维,其性质稳定,不溶于强酸、强碱
D.焰火的五彩缤纷是某些金属元素的性质的展现
-
下列有关说法中,不正确的是( )
A.“光化学烟雾”、“硝酸型酸雨”的形成都与氮氧化合物有关
B.根据分散质微粒直径大小可以将分散系分为溶液、胶体和浊液
C.可用于制造光导纤维,其性质稳定,不溶于强酸、强碱
D.焰火的五彩缤纷是某些金属元素性质的展现
-
下列说法不正确的是( )
A.“光化学烟雾”“硝酸型酸雨”的形成都与氮氧化合物有关
B.根据分散质微粒直径大小可以将分散系分为溶液、胶体和浊液
C.SiO2可用于制造光导纤维,其性质稳定,不溶于强酸、强碱
D.焰火的五彩缤纷是某些金属元素的性质的展现
-
下列有关说法中,不正确的是
A.“光化学烟雾”“硝酸型酸雨”的形成都与氮氧化合物有关
B.根据分散质微粒直径大小可以将分散系分为溶液、胶体和浊液
C.SiO2可用于制造光导纤维,其性质稳定,不溶于强酸、强碱
D.焰火的五彩缤纷是某些金属元素的性质的表现
-
下列说法不正确的是
A.“光化学烟雾”“硝酸型酸雨”的形成都与氮氧化合物有关
B.根据分散质微粒直径大小可以将分散系分为溶液、胶体和浊液
C.SiO2可用于制造光导纤维,其性质稳定,不溶于强酸、强碱
D.焰火的五彩缤纷是某些金属元素的性质的展现
-
下列关于物质性质的说法正确的是
A.二氧化硅既溶于强酸,又溶于强碱
B.铁在纯氧中的燃烧产物是红棕色固体
C.盐酸滴加到水玻璃中,可以产生白色胶状物质
D.铜的金属活动性比铝弱,可用铜罐代替铝罐贮运浓硝酸
-
三氧化二镍 主要用作陶瓷、玻璃等的着色颜料,也经常用于制造镍电池。查阅资料知:
主要用作陶瓷、玻璃等的着色颜料,也经常用于制造镍电池。查阅资料知:
Ⅰ 工业上利用含镍废料
工业上利用含镍废料 镍、铁、钙、镁合金为主
镍、铁、钙、镁合金为主 制取草酸镍
制取草酸镍 ,再高温煅烧草酸镍制取三氧化二镍。
,再高温煅烧草酸镍制取三氧化二镍。
Ⅱ 草酸的钙、镁、镍盐均难溶于水。
草酸的钙、镁、镍盐均难溶于水。
Ⅲ 、
、 .
.

根据下列工艺流程示意图回答问题。
 加入
加入 发生的主要反应的离子方程式为______,加入
发生的主要反应的离子方程式为______,加入 溶液调pH至
溶液调pH至 ,其目的为______,当加入过量
,其目的为______,当加入过量 后,所得滤液中
后,所得滤液中 ______。
______。
 草酸镍
草酸镍 在热空气中干燥脱水后在高温下煅烧三小时,制得
在热空气中干燥脱水后在高温下煅烧三小时,制得 ,同时获得混合气体。草酸镍受热分解的化学方程式为______。
,同时获得混合气体。草酸镍受热分解的化学方程式为______。
 工业上还可用电解法制取
工业上还可用电解法制取 用NaOH溶液调节
用NaOH溶液调节 溶液的pH至
溶液的pH至 ,加入适量
,加入适量 后采用惰性电极电解。电解过程中产生的
后采用惰性电极电解。电解过程中产生的 有
有 在弱碱性条件下生成
在弱碱性条件下生成 ,再把二价镍氧化为三价镍。
,再把二价镍氧化为三价镍。 氧化
氧化 生成
生成 的离子方程式为______。a mol二价镍全部转化为三价镍时,外电路中通过电子的物质的量为______。
的离子方程式为______。a mol二价镍全部转化为三价镍时,外电路中通过电子的物质的量为______。
 镉镍可充电电池在现代生活中有广泛的应用,其充、放电反应过程按下式进行:
镉镍可充电电池在现代生活中有广泛的应用,其充、放电反应过程按下式进行:

 ,写出该电池充电时阴极的电极反应式______。
,写出该电池充电时阴极的电极反应式______。
-
下列说法正确的是
A.镀锌铁的镀层破损后,镀层仍然对铁起保护作用
B.SiO2不溶于强酸和强碱,可用于制光导纤维
C.C12与SO2使品红溶液褪色的原理相同
D.常温下浓硫酸与铝不反应,可用铝槽车运输
-
碲(Te)广泛用于彩色玻璃和陶瓷。工业上用精炼铜的阳极泥(含有质量分数为8%的TeO2、少量Ag、Au)为原料制备单质碲的一种工艺流程如下,(已知TeO2微溶于水,易溶于强酸和强碱),下列有关说法不正确的是
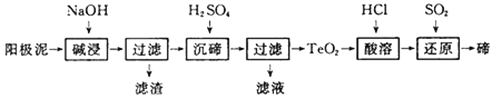
A. 将阳极泥研磨、反应适当加热都有利于提高“碱浸”的速率和效率
B. “碱浸”时发生主要反应的离子方程式为TeO2+2OH-=TeO32-+H2O
C. “沉碲”时为使碲元素沉淀充分,应加入过量的硫酸
D. 若提取过程碲元素的回收率为90%,则处理1kg这种阳极泥最少需通入标准状况下SO2 20.16L


