-
砷(33As)在元素周期表中与氮同主族,砷及其化合物被运用在农药、防腐剂、染料和医药等领域,及其多种合金中。
(1)砷原子次外层上的电子数为_____,砷化氢的电子式为_______。
(2)成语“饮鸩止渴”中的“鸩”是指放了砒霜(As2O3)的酒。As2O3是两性偏酸性的氧化物,写出As2O3溶于浓盐酸的化学方程式__________。
(3)As2O3溶于热水生成的亚砷酸(H3AsO3),具有较强的还原性,分可用于治疗白血病,其水溶液存在多种微粒形态,各微粒的分布分数与溶液pH的关系如右图:
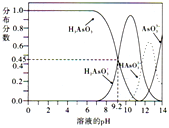
①向亚砷酸溶液中缓缓加入NaOH溶液至pH=11时,反应的离子方程式为_________。
②电离平衡常数Ka1(H3AsO3)=________。
③Na2HAsO3溶液呈碱性,该溶液中c(H2AsO3-)_____c(AsO33-)(填“>”、“<”或“=”)。
④向含有HAsO32-的溶液中滴加氯水反应的离子方程式为_________。
-
砷(33As)在元素周期表中与氮同主族,砷及其化合物被运用在农药、防腐剂、染料和医药等领域,及其多种合金中。
(1)砷化氢的电子式为________,其稳定性比NH3______(填“强”或“弱”)。
(2)成语“饮鸩止渴”中的“鸩”是指放了砒霜(As2O3)的酒。As2O3是一种两性氧化物,写出As2O3溶于浓盐酸的化学方程式__________。
(3)冶炼废水中砷元素主要以亚砷酸(H3AsO3)形式存在,可用化学沉降法处理酸性高浓度含砷废水,其工艺流程如下:
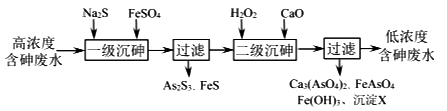
己知:I.As2S3与过量的S2-存在以下反应:As2S3(s)+3S2-(aq) 3AsS33-(aq);
3AsS33-(aq);
II.亚砷酸盐的溶解性大于相应砷酸盐。
①“一级沉砷”中FeSO4的作用是___________________________;
②“二级沉砷”中H2O2作_____剂(填“氧化”或“还原”);沉淀X为_____(填化学式)。
⑷己知砷酸(H3AsO4)是三元酸,有较强的氧化。
①常温下砷酸的Ka1=6×10-3、Ka2=1×10-7,则 NaH2AsO4溶液中c(HAsO42-)____ c(H3AsO4)(填“>”、“<”或“=”)。
②某原电池装置如图所示,C1、C2为两个石墨电极,电池总反应为:
AsO43-+2I-+H2O AsO33-+I2+2OH-。
AsO33-+I2+2OH-。

当A池中溶液由无色变成蓝色时,正极上的电极反应式为_____________。
当电流计指针归中后向B池中加入一定量的NaOH,则电子由____(填“C1”或“C2”)流出。
-
氮、磷、砷、硼的相关化合物在化工、医药、农药、材料等领域有着广泛的应用。回答下列问题:
(1)基态As原子的电子排布式为__________。N、P、As的第一电离能的大小顺序为 _______。
(2)氮化硼(BN)有多种晶体,其中立方氮化硼与金刚石的构型类似,则其晶胞中B-N-B之间的夹角是_________(填角度)。
(3)砷化硼(BAs)是Ⅲ-V族半导体材料的重要成员之一,其晶体结构与金刚石相似。
①BAs晶体中,每个As与_____个B相连,As的杂化形式为______;
②已知B原子的电负性比As原子的电负性大,则As与B之间存在的化学键有_______(填字母)。
A.离子键 B. 金属键 C.极性键 D.氢键 E.配位键F.  键G.
键G.  键
键
(4)磷化硼(BP)是一种有价值的耐磨硬涂层材料,这种陶瓷材料可作为金属表面的保护薄膜,它是通过在高温(T>750℃)氢气氛围下BBr3和PBr3反应制得的,BBr3的空间构型为______,BP晶胞的结构如图所示,当晶胞晶格参数为478pm(即图中立方体的每条边长为478pm)时,BP中B和P之间的最近距离为_____。

-
碳、 氮、磷、砷和硼的相关化合物在化工、医药、农药、材料等领域有着广泛的应用。锂、钠、铝、铁等金属在日常生活、工业生产中也占有举足轻重的地位,请回答下列问题:
(1)基态As原子的电子排布式为[Ar]______________________;
(2)氮化硼(BN)有多种晶型,其中立方氮化硼与金刚石的构型类似,则其晶胞中B—N—B之间的夹角是___________________(填角度)。
(3)砷化硼(BAs)是ⅢA一VA族半导体材料的重要成员之一,其晶体结构与金刚石相似。
①BAs晶体中,每个As与____________个B相连,As的杂化形式为_______________;
②已知B原子的电负性比As原子的电负性大,则As与B之间存在的化学键有____________(填字母)。
A.离子键 B.金属键 C.极性键 D.氢键 E.配位键 F.σ键 G.π键
(4)铁的另一种配合物Fe(CO)5熔点为-20.5℃,沸点为103℃,易溶于CCl4,据此可以判断Fe(CO)5晶体属于________________________________(填晶体类型)。
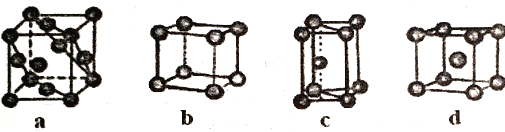
(5)金属晶体的四种堆积如下图,金属钠的晶体堆积模型为___________(填字母)。
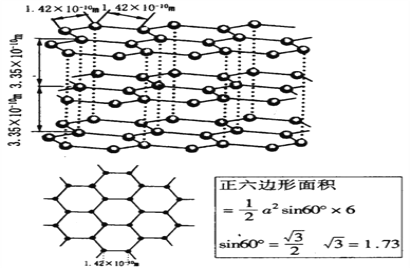
(6)石墨晶体的结构如下图,石墨的密度为________________________________(只列式不化简不计算)
-
砷(33As)在周期表中与氮同主族,砷及其化合物被运用在农药、除草剂、杀虫剂等。
(1)砷化氢的电子式为_________。
(2)成语“饮鸩止渴”中的“鸩”是指放了砒霜(As2O3)的酒。As2O3是一种两性氧化物,写出As2O3溶于浓盐酸的化学方程式_____________________。
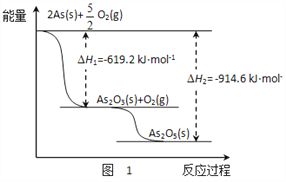
(3)砷的常见氧化物有As2O3和As2O5,其中As2O5热稳定性差。根据图1写出As2O5分解为As2O3的热化学方程式________________________________________。
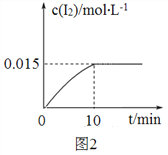
(4)砷酸钠(Na3AsO4)具有氧化性,298 K时,在100 mL烧杯中加入10 mL 0.1 mol/L Na3AsO4溶液、20 mL 0.1 mol/L KI溶液和20 mL 0.05 mol/L硫酸溶液,发生下列反应:AsO43-(无色)+2I-+2H+ AsO33-(无色)+I2(浅黄色)+H2O ΔH。测得溶液中c(I2)与时间(t)的关系如图2所示(溶液体积变化忽略不计)。
AsO33-(无色)+I2(浅黄色)+H2O ΔH。测得溶液中c(I2)与时间(t)的关系如图2所示(溶液体积变化忽略不计)。
①0~10 min内,I−的反应速率v(I−)=______________。
②在该条件下,上述反应的平衡常数K=__________。
③升高温度,溶液中AsO43-的平衡转化率减小,则该反应的ΔH______0(填“大于”“小于”或“等于”)。
(5)己知砷酸(H3ASO4)是三元酸,有较强的氧化性。
①常温下砷酸的Ka1=6×10-3、Ka2=1×10-7,则 NaH2AsO4溶液中c(HAsO42-)___c(H3AsO4)(填“>”、“<”或“=”)。
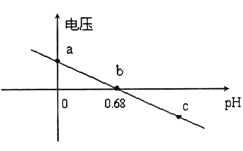
②某实验小组依据反应AsO43-+2H++2I-⇌AsO33-+I2+H2O设计如图原电池,探究pH对AsO43-氧化性的影响.测得输出电压与pH的关系如图。则a点时,盐桥中K+____移动(填“向左”、“向右”或“不”),c点时,负极的电极反应为____________________。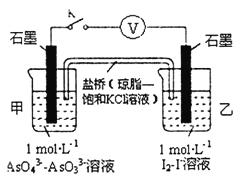
-
吲哚类化合物以其独特的化学结构使其拥有重要的生理活性,在农药、医药、化工、香料和染料等领域发挥着重要的作用。下图是合成“氮-苯甲酰基-2-甲基-3吲哚乙酸甲酯”的路线
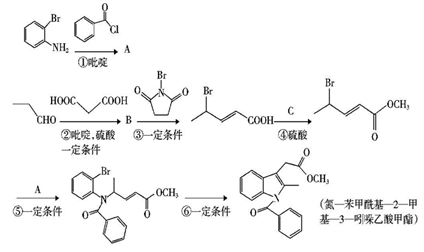
已知: 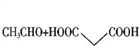
 CH3CH=CHCOOH+CO2+H2O
CH3CH=CHCOOH+CO2+H2O
回答下列问题
(1)B的结构简式为________,B分子中含有的官能团为________(填官能团名称)。
(2)反应③为取代反应,该反应的化学方程式为________。
(3)C的名称为________。
(4)A的结构简式为________,反应⑤的反应类型为________。
(5)B有多种同分异构体,其中与B含有相同官能团的同分异构体有________种。
(6)已知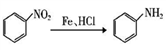
参照上述合成路线,以 为原料(无机试剂任选),设计制备
为原料(无机试剂任选),设计制备 的合成路线________。
的合成路线________。
-
氯、磷的化合物广泛用于农药、医药、染料等领域。
(1)PCl3与氯气、水反应,得到HCl气体和一种无色透明有刺激性臭味的液体X,实验测定,1 mol的H2O完全反应会生成2 mol的HCl,则X的组成元素是______________;已知X的相对分子质量为153.5,则X的化学式为________________。
(2)X在高温与O2发生反应,形成P4O10(固态)和Cl2。将3.07 g X与448 mLO2(已折算至标准状况,下同)在高温下充分反应后,生成Cl2____mol,气体的体积将变为_____mL。
(3)白磷在氯气中燃烧,一般得到PCl3和PCl5的混合物。2.48 g白磷(P4),与一定量的氯气恰好完全反应,产物的总质量为14.55 g,计算产物中PCl3的质量分数____________(保留3小数)。
-
钛、铁、砷、硒、锌等元素的单质及其化合物在化工、医药、材料等领域有着广泛的应用。
(1)基态Ti原子中,最高能层电子的电子云轮廓形状为_______,与Ti同周期的所有过渡元素的基态原子中,最外层电子数与钛不同的元素有________种。
(2)铁的第三电离能 、第四电离能
、第四电离能 分别为
分别为 和
和 ,
, 远大于
远大于 的原因是______________________。
的原因是______________________。
(3) 离子可用于
离子可用于 的检验,其对应的酸有两种,分别为硫氰酸
的检验,其对应的酸有两种,分别为硫氰酸 和异硫氰酸
和异硫氰酸 。
。
①写出与 互为等电子体的一种微粒_________
互为等电子体的一种微粒_________  分子或离子
分子或离子 ;
;
②异硫氰酸的沸点比硫氰酸沸点高的原因是_______________。
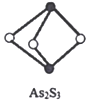
(4)成语“信口雌黄”中的雌黄分子式为 ,分子结构如图1所示,As原子的杂化方式为_______________。
,分子结构如图1所示,As原子的杂化方式为_______________。
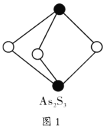
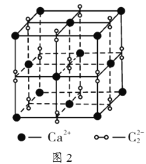
(5)离子化合物 的晶胞结构如图2所示。一个晶胞含有的
的晶胞结构如图2所示。一个晶胞含有的 键有__________个。
键有__________个。
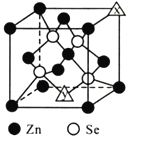
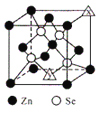
(6)硒化锌的晶胞结构如图所示,图中X和Y点所堆积的原子均为____________ 填元素符号
填元素符号 ;该晶胞中硒原子所处空隙类型为____________
;该晶胞中硒原子所处空隙类型为____________ 填“立方体”、“正四面体”或“正八面体”
填“立方体”、“正四面体”或“正八面体” ,该种空隙的填充率为____________;若该晶胞密度为
,该种空隙的填充率为____________;若该晶胞密度为 ,硒化锌的摩尔质量为
,硒化锌的摩尔质量为 。用
。用 代表阿伏加德罗常数的数值,则晶胞参数a为____________nm。
代表阿伏加德罗常数的数值,则晶胞参数a为____________nm。
-
第四周期的元素,如:钛(22Ti)、铁(26Fe)、砷、硒、锌等及其相关化合物在化工、医药、材料等领域有着广泛的应用。回答下列问题:
(1)基态Ti原子中,最高能层电子的电子云轮廓形状为___________,与Ti同周期的所有过渡元素的基态原子中,最外层电子数与钛不同的元素有______种。
(2)琥珀酸亚铁片是用于缺铁性贫血的预防和治疗的常见药物,临床建议服用维生素C促进“亚铁”的吸收,避免生成Fe3+,从结构角度来看,Fe2+ 易被氧化成Fe3+的原因是______________。
(3)SCN-离子可用于Fe3+的检验,其对应的酸有两种,分别为硫氰酸(H-S-C≡N)和异硫氰酸(H-N=C=S)。
①写出与SCN-互为等电子体的一种微粒_________________(分子或离子);
②硫氰酸分子中π键和σ键的个数之比为___________;
③异硫氰酸的沸点比硫氰酸沸点高的原因是________________________。
(4)成语“信口雌黄”中的雌黄分子式为As2S3,分子结构如图,As原子的杂化方式为____________,雌黄和SnCl2在盐酸中反应转化为雌黄(As4S4)和SnCl4并放出H2S气体,写出该反应方程式__________________________。SnCl4分子的空间构型为______________。
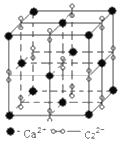
(5) 高子化合物CaC2的一种晶体结构如图所示。该物质的电子式___________。一个晶胞含有的π键平均有___________个。
(6)硒化锌的晶胞结构如图所示,图中X和Y点所堆积的原子均为___________(填元素符号);该晶胞中硒原子所处空隙类型为___________(填“立方体”、“正四面体”或正八面体”),该种空隙的填充率为___________;若该晶胞密度为pg•cm-3,硒化锌的摩尔质量为Mg•mol-1。用NA代表阿伏加德罗常数的数值,则晶胞参数a 为___________nm。
-
钛及其化合物在化工、医药、材料等领域有着广泛的应用。
(1)基态钛原子的价电子排布式为_____________,与钛同周期的元素中,基态原子的未成对电子数与钛相同的有____________种。
(2)钛比钢轻、比铝硬,是一种新兴的结构材料,钛的硬度比铝大的原因是_________。
(3)在浓的TiCl3的盐酸溶液中加入乙醚,并通入HCl至饱和,可得到配位数为6、组成为TiCl3·6H2O的绿色晶体,该晶体中两种配体的物质的量之比为1:5,则该配合离子的化学式为___________。
(4)半夹心结构催化剂M能催化乙烯、丙烯、苯乙烯的聚合,其结构如下图所示。

①组成M的元素中,电负性最大的是_________(填名称)。
②M中碳原子的杂化方式为____________。
③M中不含________(填代号)。
a.π键 b.σ键 c.离子键 d.配位键
(5)金红石(TiO2)是含钛的主要矿物之一。其晶胞结构(晶胞中相同位置的原子相同)如图所示。
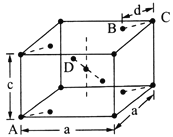
①A、B、C、D 4种微粒,其中氧原子是________(填代号)。
②若A、B、C的原子坐标分别为A(0,0,0)、B(0.69a,0.69a,c)、C(a,a,c),则D的原子坐标为D(0.19a,____,___);钛氧键的键长d=______(用代数式表示)。












 CH3CH=CHCOOH+CO2+H2O
CH3CH=CHCOOH+CO2+H2O







