-
铈是稀土中丰度最高的元素,其在电子材料、催化剂等方面的应用广泛。现以氟碳铈矿(含CeFCO3、BaO、SiO2等)为原料制备氧化铈(CeO2),并测定其纯度。其工艺流程如下:

已知:①稀土离子易和SO 形成复盐沉淀:
形成复盐沉淀:
Ce2(SO4)3+Na2SO4+nH2O==== Ce2(SO4)3·Na2SO4·nH2O↓(复盐沉淀);
②硫脲:一种有机物,结构简式为 ,酸性条件下易被氧化为(SCN2H3)2;
,酸性条件下易被氧化为(SCN2H3)2;
③Ce3+在空气中易被氧化为Ce4+;
回答下列问题:
(1)焙烧时,为了提高焙烧效率,可采取的措施有________________________________________
(2)CeFCO3中Ce元素的化合价为___________,滤渣A的主要成分是_____________
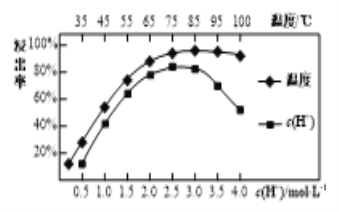
(3)焙烧后加入硫酸浸出,稀土的浸出率和硫酸浓度、温度有关,如图所示,应选择的适宜的条件为___________,硫酸浓度过大时,浸出率减小的原因是__________。
(4)加入硫脲的目的是将Ce4+还原为Ce3+,反应的化学方程式为_________。
(5)步骤③加入盐酸后,通常还需加入H2O2,其主要目的为_________。
(6)步骤④的离子方程式为________________________。
(7)取所得产品CeO2 8.0g,用30 mL高氯酸和20 mL磷酸混合液加热溶解,冷却至室温后,配成250 mL溶液。取25.00 mL溶液用0.2000 mol·L-1硫酸亚铁铵[(NH4)2Fe(SO4)2]溶液滴定,已知滴定时发生的反应为Fe2++Ce4+==== Fe3++Ce3+,达到滴定终点时消耗硫酸亚铁铵溶液20.50 mL,则该产品的纯度为____________。
-
铈是地壳中丰度最高的稀土元素,可用作催化剂、合金添加剂,也可用于医药、制革、玻璃、纺织等工业。氟碳铈矿的主要化学成分为CeFCO3,它是提取铈的重要矿物原料。氟碳铈矿的冶炼处理工艺已经发展到十数种,其中一种提取铈的工艺流程如下图所示。
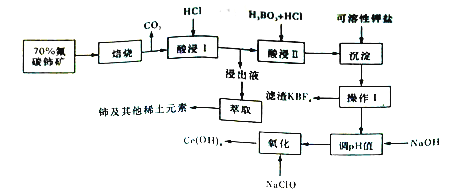
已知:焙烧后烧渣中含+4价的铈及十3 价的其他稀土氟化物和氧化物。
请回答下列问题:
(1)CeFCO3 中Ce元素的化合价为______。
(2)“焙烧”前将矿石粉碎成细颗粒的目的是___________________________________________。
(3)“酸浸I”步骤中CeO2 转化为Ce3+,且产生黄绿色气体,该过程的离子方程式为___________________。
(4)“酸浸1”步骤中CeF4 转化为难溶物Ce(BF4)3,加入可溶性钾盐的目的是__________________。
(5)“操作I”后,向溶液中加入NaOH溶液,调节溶液pH 可获得Ce(OH)3沉淀,利用pH 试纸测定溶液pH值的实验操作是__________________________________。当溶液中离子浓度小于1×10-6 mol/L 时视为沉淀完全,常温下,加入NaOH 调节溶液的pH应大于____[已知Ce(OH)3 的Ksp=8.0×10-21,1g2=0.3]。
(6)写出“氧化”步骤的化学方程式:_________________________________________。
-
氟碳铈矿的主要化学成分为CeFCO3,它是提取铈族稀土元素的重要矿物原料,二氧化铈(CeO2) 是一种重要的稀土氧化物。以氟碳铈矿为原料制备CeO2的一种工艺流程如下:
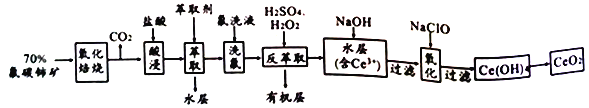
已知:①Ce 4+既能与F 结合成[CeFx](4-x)+,也能与SO42-结合成[CeSO4]2+;
②在硫酸体系中Ce4+ 能被萃取剂[(HA)2]萃取,而Ce3+不能。
回答下列问题:
(1) “氧化焙烧”的目的是______________。
(2)“酸浸”中会产生大量黄绿色气体、请写出CeO2与盐酸反应的离子方程式___________________;为避免产生上述污染,请提出一种解决方案________________________。
(3)“萃取”时存在反应:Ce4++n(HA)2 Ce+(H2a-4A2a)+4H+。实验室中萃取时用到的主要玻璃仪器为______________;若缺少 “洗氟”,则所得产品的质量将_________(填“偏大”、“偏小”或 “不变”)。
Ce+(H2a-4A2a)+4H+。实验室中萃取时用到的主要玻璃仪器为______________;若缺少 “洗氟”,则所得产品的质量将_________(填“偏大”、“偏小”或 “不变”)。
(4) “反萃取”中,加稀硫酸和H2O2的作用__________________(用离子方程式表示)。
(5)取上述流程中得到的CeO2产品0.500g,加硫酸溶解后,用0.1000mol·L-1FeSO4标准溶液滴定至终点时(铈被还原为Ce3+,其它杂质均不参加反应)消25.00mL标准溶液,该产品中CeO2的质量分数为________。
-
稀土是一种重要的战略资源。氟碳铈矿主要化学成分为CeFCO3,它是提取铈等稀土元素的重要矿物原料。氟碳铈矿的冶炼工艺流程如下:
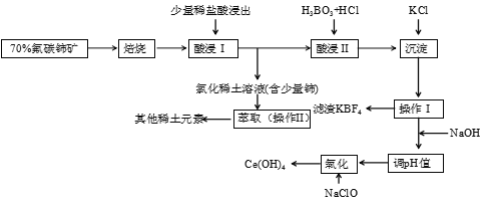
已知:i.铈的常见化合价为+3、+4。焙烧后铈元素转化成CeO2和CeF4。四价铈不易进入溶液,而三价稀土元素易进入溶液。
ii.酸浸II中发生反应:
9CeO2 + 3CeF4 + 45HCl + 3H3BO3 = Ce(BF4)3↓+ 11CeCl3 + 6Cl2↑+ 27H2O
请回答下列问题:
(1)①焙烧氟碳铈矿的目的是______________________________________。
②焙烧后产生的CeO2是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧。在尾气消除过程中发生着CeO2 CeO2(1-x)+xO2↑的循环。写出CeO2消除CO尾气的化学方程式:___________________________________________。
CeO2(1-x)+xO2↑的循环。写出CeO2消除CO尾气的化学方程式:___________________________________________。
(2)在酸浸I中用盐酸浸出时,有少量铈进入滤液,且产生黄绿色气体。少量铈进入稀土溶液发生反应的离子方程式是_________________________________________________________
(3)向Ce(BF4)3中加入KCl溶液的目的是_____________________________________。
(4)操作I的名称为__________,在实验室中进行操作II时所需要的硅酸盐仪器有______。
(5)“操作I”后,向溶液中加入NaOH 溶液来调节溶液的pH, 以获得Ce(OH) 3沉淀,常温下加入NaOH 调节溶液的pH 应大 于 _______ 即可认为Ce3 +已完全沉淀。
(已知:Ksp[Ce(OH)3]=1.0×10-20 )
(6)取上述流程中得到的Ce(OH)4产品5.000 g,加酸溶解后,向其中加入含0.03300 molFeSO4的FeSO4溶液使Ce4 +全部被还原成Ce3 +,再用0.1000 mol·L-1的酸性KMnO4标准溶液滴定至终点时,消耗20.00 mL标准溶液。则该产品中Ce(OH)4的质量分数为________(已知氧化性:Ce4+>KMnO4; Ce(OH)4的相对分子质量为208)。
-
稀土是一种重要的战略资源。氟碳铈矿主要化学成分为CeFCO3,它是提取铈等稀土元素的重要矿物原料。氟碳铈矿的冶炼工艺流程如下:
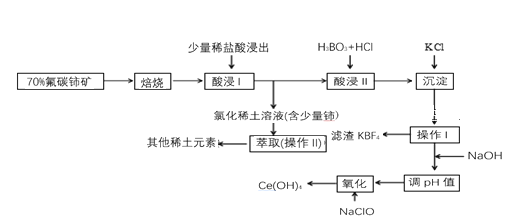
已知:i.铈的常见化合价为+3、+4。焙烧后铈元素转化成CeO2和CeF4。四价铈不易进入溶液,而三价稀土元素易进入溶液。
ii.酸浸II中发生反应:9CeO2+3CeF4+45HCl+3H3BO3=Ce(BF4)3↓+11CeCl3+6Cl2↑+27H2O
请回答下列问题:
(1)①焙烧氟碳铈矿的目的是_______。
②焙烧后产生的CeO2是汽车尾气净化催化剂的关键成分,它能在还原气氛中供氧,在氧化气氛中耗氧。在尾气消除过程中发生着CeO2 CeO2(1-x)+xO2↑的循环。写出CeO2消除CO尾气的化学方程式:________。
CeO2(1-x)+xO2↑的循环。写出CeO2消除CO尾气的化学方程式:________。
(2)在酸浸I中用盐酸浸出时,有少量铈进入滤液,且产生黄绿色气体。少量铈进入稀土溶液发生反应的离子方程式是________。
(3)向Ce(BF4)3中加入KCl溶液的目的是______。
(4)操作I的名称为_______,在实验室中进行操作II时所需要的硅酸盐仪器有_______。
(5)“操作I”后,向溶液中加入NaOH溶液来调节溶液的pH,以获得Ce(OH)3沉淀,常温下加入NaOH调节溶液的pH应大于________即可认为Ce3+已完全沉淀。(已知:Ksp[Ce(OH)3]=1.0×10-20)
(6)取上述流程中得到的Ce(OH)4产品5.000g,加酸溶解后,向其中加入含0.03300mol FeSO4的FeSO4溶液使Ce4+全部被还原成Ce3+,再用0.1000mol·L-1的酸性KMnO4标准溶液滴定至终点时,消耗20.00mL标准溶液。则该产品中Ce(OH)4的质量分数为______(已知氧化性:Ce4+>KMnO4;Ce(OH)4的相对分子质量为208,保留3位有效数字)。
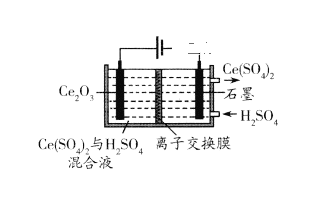
(7)在酸性条件下电解Ce2O3制备Ce(SO4)2(如下图),阳极电极反应式_______。
-
稀土是一种重要的战略资源、氟碳铈矿主要化学成分为CeFCO3,它是提取铈等稀土元素的重要矿物原料。氟碳铈矿的冶炼工艺流程如下:
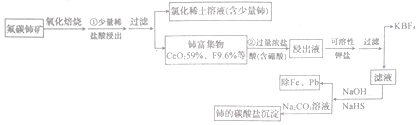
已知:Ⅰ.铈的常见化合价为+3、+4
Ⅱ.Ce4+可以与SO42-结合为[CeSO4]2+
Ⅲ. 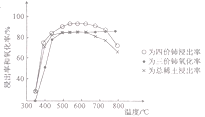
焙烧时铈被氧化成四价,四价铈不易进入溶液,而三价稀土元素易进入溶液。在盐酸浸出时,有少量铈进入滤液,且产生黄绿色气体。
回答下列问题:
(1)氟碳铈矿焙烧的目的是__________________;焙烧最适宜温度为______________(填标号)。a.350~ 4 50℃ b.550~650℃ C.750℃以上
步骤①中少量铈进入稀土溶液发生反应的离子方程式是_________________________。
(2)铈富集物用含硼酸的盐酸溶液处理,使氟转化为四氟硼酸根离子,然后用可溶性钾盐将四氟硼酸根离子转变为KBF4沉淀并过滤除去。写出生成KBF4的离子方程式:________________。此法处理铈富集物的缺点是____________________。
(3)除云氟离子后向滤液中先加入NaOH 溶液,然后再加入NaHS除去铁与铅。加入NaOH 溶液的目的是____________________。
(4)写出此流程中铈的碳酸盐沉淀的化学式:______________________。
-
氟碳铈矿主要化学成分为CeFCO3,它是提取铈族稀土元素的重要矿物原料.氟碳铈矿的冶炼处理工艺已经发展到十数种,其中一种提取铈的工艺流程如下:
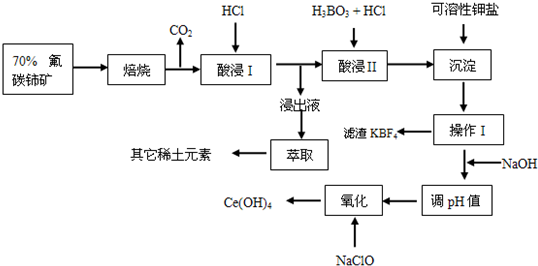
已知:焙烧后烧渣中含+4价的铈及+3价的其它稀土氟氧化物;酸浸I的浸出液中含少量的+3价的铈
请回答下列问题
(1)焙烧前将矿石粉碎成细颗粒的目的是______.
(2)酸浸II后,四价铈转化为三价,为了避免三价铈以四氟硼酸盐形式损失,用可溶性钾盐将四氟硼酸根沉淀除去,该反应的离子方程式为:______
(3)在生产过程中,酸浸I 中会产生大量黄绿色气体,污染环境、腐蚀设备,写出产生黄绿色气体的离子方程式:______,提出一种解决的方案:______.
(4)实验室中进行操作I所用玻璃仪器名称:______;在操作I后的溶液中加入NaOH溶液是为了调节溶液pH值获得Ce(OH)3,测定该溶液pH值的操作是______.
(5)写出氧化步骤的化学方程式:______,其中还原产物是______.
-
稀土金属是我国战略性资源。氟碳铈矿主要化学成分为CeFCO3,它是提取铈族稀土元素的重要矿物原料。其中一种提取铈的工艺流程如下:
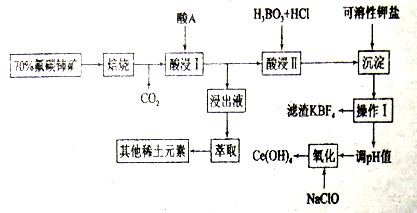
已知:焙烧后烧渣中含+4价的铈及+3价的其它稀土氟氧化物;+ 4价的铈的氧化物有很强的氧化性,通常在酸性条件下易被还原剂还原成+3价而溶于水。请回答下列问题
(1)酸浸l中所用的酸A为(用字母表示)________(a.盐酸 b.稀硫酸),原因是_______。
(2)酸浸Ⅱ后,为避免三价铈以四氟硼酸盐形式损失,需用可溶性钾盐将四氟硼酸根离子沉淀除去,该反应的离子方程式为___________。
(3)实验室中进行萃取操作所用到的主要玻璃仪器名称是________;在操作I后的溶液中加入NaOH溶液是为了调节溶液pH 获得Ce(OH)3和_______,测定该溶液pH的操作是_______。
(4)写出氧化步骤的化学方程式_______________。
-
稀土元素是宝贵的战略资源,我国的蕴藏量居世界首位,但近年来对其进行了掠夺性开采。二氧化铈(CeO2)是一种重要的稀土化合物。以氟碳铈矿(主要含CeFCO3)为原料制备CeO2的一种工艺流程如图:
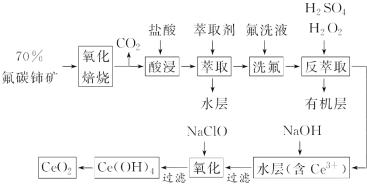
已知:①Ce4+能与F-结合成[CeFx](4-x)+,也能与SO42-结合成[CeSO4]2+;
②在硫酸体系中Ce4+能被萃取剂[(HA)2]萃取,而Ce3+不能。
回答下列问题:
(1)“氧化焙烧”中“氧化”的目的是__。
(2)“酸浸”中会产生大量黄绿色气体,写出CeO2与盐酸反应的离子方程式:__。为避免产生上述污染,请提出一种解决方案:__。
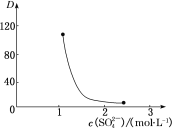
(3)“萃取”时存在反应:Ce4++n(HA)2 Ce·(H2n-4A2n)+4H+。如图中D是分配比,表示Ce(Ⅳ)分别在有机层中与水层中存在形式的物质的量浓度之比(D=
Ce·(H2n-4A2n)+4H+。如图中D是分配比,表示Ce(Ⅳ)分别在有机层中与水层中存在形式的物质的量浓度之比(D= )。保持其他条件不变,D随起始料液中c(SO42-)变化的原因:__(用平衡移动原理解释)。
)。保持其他条件不变,D随起始料液中c(SO42-)变化的原因:__(用平衡移动原理解释)。
(4)若缺少“洗氟”,则所得产品的质量将__(填“偏大”“偏小”或“不变”)。
(5)“反萃取”中,H2O2作__(填“催化剂”“氧化剂”或“还原剂”)。
(6)“氧化”步骤的化学方程式为__。
(7)取上述流程中得到的CeO2产品0.4000g,加硫酸溶解后,用0.1000mol·L-1FeSO4标准溶液滴定至终点时(铈被还原为Ce3+,其他杂质均不反应),消耗20.00mL标准溶液。该产品中CeO2的质量分数为__。滴定过程中可能造成实验结果偏低的是__(填字母)。
A.使用久置的FeSO4标准溶液
B.滴定终点时仰视读数
C.锥形瓶中溶液变色后立刻停止滴定,进行读数
D.滴定管尖嘴内滴定前无气泡,滴定终点发现气泡
-
氟碳铈矿(主要成分为CeFCO3)是提取稀土化合物、冶炼铈的重要矿物原料,以氟碳铈矿为原料提取铈的工艺流程如图所示。
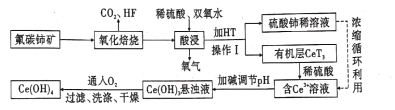
回答下列问题:
(l)CeFCO3中Ce的化合价为____ 。
(2)氧化培烧时不能使用陶瓷容器,原因是________.。
(3)氧化焙烧后的产物之一为CeO2.则酸浸时发生反应的离子方程式为____。
(4)HT是一种难溶于水的有机溶剂,则操作I的名称为 _____。
(5)为了提高酸浸率,可以适当提高反应温度,但温度偏高浸出率反而会减小,其原因是____。
(6)有机物HT能将Ce3+从水溶液中萃取出来,该过程可表示为Ce3+(水层)+3HT(有机层)  CeT3(有机层)+3H+(水层)。向CeT3(有机层)中加入稀硫酸能获得较纯的含Ce3+的水溶液,从平衡角度解释其原因________。
CeT3(有机层)+3H+(水层)。向CeT3(有机层)中加入稀硫酸能获得较纯的含Ce3+的水溶液,从平衡角度解释其原因________。
(7)写出向Ce(OH)3悬浊液中通入氧气得到产品Ce(OH)4的化学方程式:__________________________。

形成复盐沉淀:
,酸性条件下易被氧化为(SCN2H3)2;












