-
一些行业的废水中氨氮含量严重超标,废水脱氮已成为主要污染物减排和水体富营养化防治的研究热点,有多种方法可以去除。
I.电镀行业废水处理流程如下:
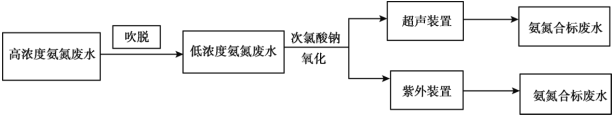
(1)吹脱法除氨氮:水中的氨氮大多数以 和游离态的
和游离态的 保持平衡状态而存在。将空气直接通入水中,使气相和液相充分接触。水中溶解的游离氨穿过气液界面,向气相转移,从而达到脱除氨的目的。氨氮废水中
保持平衡状态而存在。将空气直接通入水中,使气相和液相充分接触。水中溶解的游离氨穿过气液界面,向气相转移,从而达到脱除氨的目的。氨氮废水中 和
和 平衡态的平衡关系有________。
平衡态的平衡关系有________。
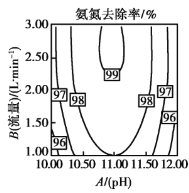
(2)温度、 值、空气流量对脱除氨有很大的影响。
值、空气流量对脱除氨有很大的影响。 值、空气流量对脱除氨影响如图所示。由图可以看出,空气流量一定时,
值、空气流量对脱除氨影响如图所示。由图可以看出,空气流量一定时, 时,吹脱率随着
时,吹脱率随着 增加而增加,请用化学平衡移动原理解释原因________。
增加而增加,请用化学平衡移动原理解释原因________。
(3)次氯酸钠氧化法:利用次氯酸钠氧化废水中氨氮的离子方程式是________。
II.对于含有 的氨氮废水还可以用电化学沉淀与阴极氧化协同去除水中的氨氮,装置如图所示。电解过程中,石墨毡电极产生
的氨氮废水还可以用电化学沉淀与阴极氧化协同去除水中的氨氮,装置如图所示。电解过程中,石墨毡电极产生 ,在通入
,在通入 的情况,又产生
的情况,又产生 ,以氧化水中的
,以氧化水中的 ,同时
,同时 还可以通过生成
还可以通过生成 沉淀而持续被除去。
沉淀而持续被除去。
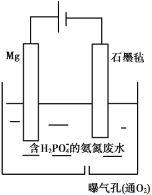
(1)阳极的电极反应式是________。
(2)废水中的 转化为
转化为 的离子方程式是________。
的离子方程式是________。
(3) 大于
大于 不利于
不利于 的生成,原因是________。
的生成,原因是________。
-
近年来,随着人类社会的快速发展,环境污染日益严重,而环境污染中的很多问题是由于氮磷富集化引起的,所以如何降低水体中的氮磷含量问题受到广泛关注。目前有两种较为有效的氨氮废水处理方法。
I.化学沉淀法
利用了Mg2+与PO43-与氨氮生成MgNH4PO4∙6H2O沉淀以达到去除氨氮的效果。
已知:磷在pH=8-10时主要存在形式为HPO42-
Ksp(MgNH4PO4∙6H2O)=2.5×10-13
(1)请写出pH=8时,化学沉淀法去除NH4+的离子方程式为_。
(2)氨氮去除率与含磷微粒浓度随pH变化如图1所示,已知:Ksp[Mg3(PO4)2]=6.3×10-26,请解释pH>10时氨氮去除率随pH变化的原因:__。
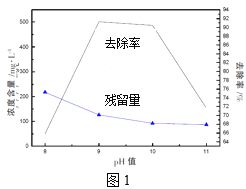
II.光催化法
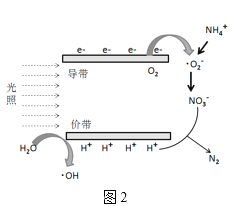
(3)光催化降解过程中形成的羟基自由基(·OH)和超氧离子(·O2-)具有光催化能力,催化原理如图2所示。请写出NO3-转化为无毒物质的电极反应式:__。
(4)经过上述反应后,仍有NH4+残留,探究其去除条件。
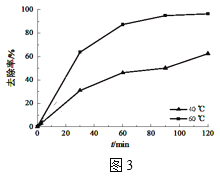
①温度对氨氮去除率影响如图3所示。温度升高,氨氮去除率变化的可能原因是:__;__(请写出两条)。
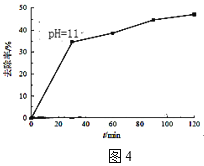
②选取TiO2作为催化剂,已知:TiO2在酸性条件下带正电,碱性条件下带负电。请在图4中画出pH=5时,氨氮去除率变化曲线_____。
(5)为测定处理后废水中(含少量游离酸)残留NH4+浓度,可选用甲醛-滴定法进行测定。取20mL的处理后水样,以酚酞为指示剂,用0.0100mol/LNaOH滴定至酚酞变红,此时溶液中游离酸被完全消耗,记下消耗NaOH的体积V1mL;然后另取同样体积水样,加入甲醛,再加入2-3滴酚酞指示剂,静置5min,发生反应:6HCHO+4NH4+=(CH2)6N4H+ +6H2O+3H+,继续用NaOH滴定,发生反应:(CH2)6N4H++OH-=(CH2)6N4+H2O;H++OH-=H2O。滴定至终点,记录消耗NaOH的体积V2mL,水样中残留NH4+浓度为__mol/L。
-
水体砷污染已成为一个亟待解决的全球性环境问题,我国科学家研究零价铁活化过硫酸钠(Na2S2O8)去除废水中的正五价砷[As(Ⅴ)],其机制模型如图。
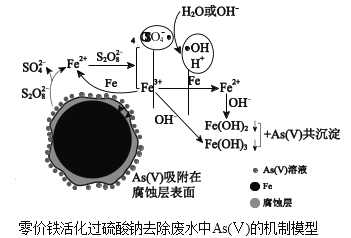
资料:
Ⅰ.酸性条件下SO 为主要的自由基,中性及弱碱性条件下SO
为主要的自由基,中性及弱碱性条件下SO ·和·OH同时存在,强碱性条件下·OH为主要的自由基。
·和·OH同时存在,强碱性条件下·OH为主要的自由基。
Ⅱ.Fe2+、Fe3+形成氢氧化物沉淀的pH
| 离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe2+ | 7.04 | 9.08 |
| Fe3+ | 1.87 | 3.27 |
(1)砷与磷在元素周期表中位于同一主族,其原子比磷多一个电子层。
①砷在元素周期表中的位置是_____。
②砷酸的化学式是_____,其酸性比H3PO4_____(填“强”或“弱”)。
(2)零价铁与过硫酸钠反应,可持续释放Fe2+,Fe2+与S2O 反应生成Fe3+和自由基,自由基具有强氧化性,利于形成Fe2+和Fe3+,以确保As(Ⅴ)去除完全。
反应生成Fe3+和自由基,自由基具有强氧化性,利于形成Fe2+和Fe3+,以确保As(Ⅴ)去除完全。
①零价铁与过硫酸钠反应的离子方程式是_____。
②Fe3+转化为Fe2+的离子方程式是_____。
③SO ·和H2O反应的离子方程式是_____。
·和H2O反应的离子方程式是_____。
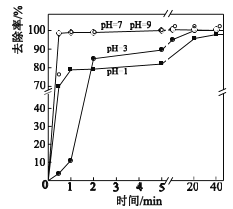
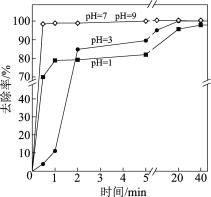
(3)不同pH对As(Ⅴ)去除率的影响如图。5min内pH=7和pH=9时去除率高的原因是_____。
-
(12分)味精厂、化肥厂、垃圾渗滤液等排放的废水中往往含有高浓度的氨氮,若不经处理直接排放会对水体造成严重的污染。
(1)生物硝化法:在富氧条件下,通过硝酸盐菌的作用,将氨氮(以 NH4+表示,下同)氧化成硝酸盐,其反应的离子方程式为 。
(2)MAP 沉淀法:向氨氮废水中投加磷酸盐和镁盐,使之和 NH4+生成难溶复盐MgNH4PO4·6H2O(简称MAP)结晶,是一种比较新颖有效的处理方法。
①用离子方程式表示反应的原理 。
②MAP沉淀法需要控制反应的pH 在 7.5~10 之间。当 pH>10时,由于 而不利于MAP的生成。
(3)电化学氧化法:电化学去除氨氮主要是氯气和次氯酸的间接氧化作用。对某养猪场废水进行电化学氧化处理,选用 IrO2-TiO2/Ti电极作为阳极,阴极采用网状钛板,加入一定量的NaCl,调节溶液的pH,在电流密度为 85 mA·cm-2下电解,180 min内去除率达到98.22%。
①阳极发生的电极反应式是 ; HClO 氧化除去氨氮的反应离子方程式是 。
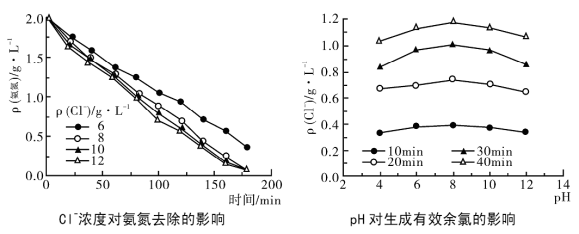
②为了提高氨氮的去除率,需要控制溶液中 Cl-的浓度和 pH,根据下图判断: Cl-的适宜浓度为 ,适宜的 pH 为 。
-
地下水受到硝酸盐污染已成为世界范围内一个相当普遍的环境问题。用零价铁去除水体中的硝酸盐(NO3-)是地下水修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示。
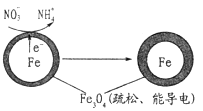
作负极的物质是___________;正极的电极反应式是_____________。
(2)将足量铁粉投入水体中,测定NO3-去除率和pH,结果如下:
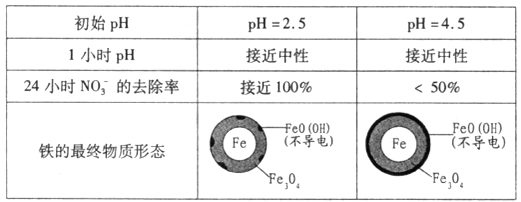
在pH =4.5的水体中,NO3-的去除率低的原因是_____________。
(3)为提高pH =4.5的水体中NO3-的去除率,某课题组在初始pH =4.5的水体中分别投入①Fe2+、②Fe、③Fe和Fe2+做对比实验结果如图:
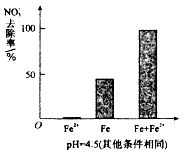
此实验可得出的结论是____,Fe2+的作用可能是_________。(2)中NO3-去除率和铁的最终物质形态不同的原因______________。
(4)地下水呈中性,在此条件下,要提高NO3-的去除速率,可采取的措施有_______。(写出一条)
-
地下水受到硝酸盐污染已成为世界范围内一个相当普遍的环境问题。用零价铁去除水体中的硝酸盐(NO3-)是地下水修复研究的热点之一。
(1)Fe还原水体中NO3-的反应原理如图所示。
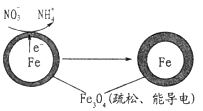
作负极的物质是___________;正极的电极反应式是_____________。
(2)将足量铁粉投入水体中,测定NO3-去除率和pH,结果如下:

在pH =4.5的水体中,NO3-的去除率低的原因是_____________。
(3)为提高pH =4.5的水体中NO3-的去除率,某课题组在初始pH =4.5的水体中分别投入①Fe2+、②Fe、③Fe和Fe2+做对比实验结果如图:
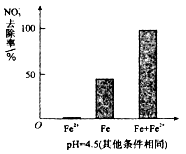
此实验可得出的结论是____,Fe2+的作用可能是_________。(2)中NO3-去除率和铁的最终物质形态不同的原因______________。
(4)地下水呈中性,在此条件下,要提高NO3-的去除速率,可采取的措施有_______。(写出一条)
-
水体砷污染已成为一个亟待解决的全球性环境问题,我国科学家研究零价铁活化过硫酸钠(Na2S2O8)去除废水中的正五价砷[As(Ⅴ)],其机制模型如下。
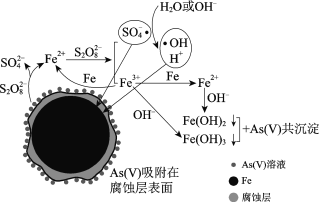
零价铁活化过硫酸钠去除废水中As(Ⅴ)的机制模型
资料:
Ⅰ.酸性条件下SO4−·为主要的自由基,中性及弱碱性条件下SO4−·和·OH同时存在,强碱性条件下·OH为主要的自由基。
Ⅱ.Fe2+、Fe3+形成氢氧化物沉淀的pH
| 离子 | 开始沉淀的pH | 沉淀完全的pH |
| Fe2+ | 7.04 | 9.08 |
| Fe3+ | 1.87 | 3.27 |
(1)砷与磷在元素周期表中位于同一主族,其原子比磷多一个电子层。
① 砷在元素周期表中的位置是______。
② 砷酸的化学式是______,其酸性比H3PO4______(填“强”或“弱”)。
(2)零价铁与过硫酸钠反应,可持续释放Fe2+,Fe2+与S2O82−反应生成Fe3+和自由基,自由基具有强氧化性,利于形成Fe2+和Fe3+,以确保As(Ⅴ)去除完全。
①S2O82−中S的化合价是______。
②零价铁与过硫酸钠反应的离子方程式是______。
③Fe3+转化为Fe2+的离子方程式是______。
(3)不同pH对As(Ⅴ)去除率的影响如图。5 min内pH = 7和pH = 9时去除率高的原因是______。
-
中共十九大报告指出,加快水污染防治、实施流域环境和近岸海域综合治理、环境污染的治理是化学工作者研究的重要课题,也是践行“绿水青山就是金山银山”的重要举措。请回答下列问题:
(1)氨氮水体污染可用次氯酸除去,已知:
Ⅰ. 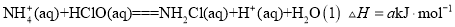
Ⅱ. 
Ⅲ. 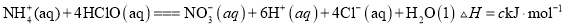
写出水体中 与
与 反应生成
反应生成 的热化学方程式:____________________________。
的热化学方程式:____________________________。
(2)工业上可用排放的 与
与 合成尿素的方法,达到
合成尿素的方法,达到 减排的目的:
减排的目的: 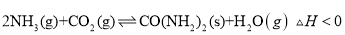 。
。
①一定条件下,在1L的密闭容器中充入1mol 和一定量的
和一定量的 ,模拟工业生产得到
,模拟工业生产得到 的平衡转化率(
的平衡转化率( )随氨碳比
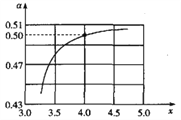
)随氨碳比 的变化如图所示,其他条件不变,
的变化如图所示,其他条件不变,  随
随 增大而增大的原因是_______________________________________________;实际工业生产中氨碳比控制在4.0左右,而不是4.5的原因是____________________________________;该温度下反应的平衡常数
增大而增大的原因是_______________________________________________;实际工业生产中氨碳比控制在4.0左右,而不是4.5的原因是____________________________________;该温度下反应的平衡常数 ______________________________。
______________________________。
②若 ,在1L的恒容密闭容器中充入一定量的
,在1L的恒容密闭容器中充入一定量的 和
和 ,此时体系压强为
,此时体系压强为 ,5min达到平衡时生成1mol
,5min达到平衡时生成1mol ,此时容器内压强为
,此时容器内压强为 ,则用
,则用 表示该反应的平均速率为______________________________,
表示该反应的平均速率为______________________________,  的平衡转化率为__________。
的平衡转化率为__________。
(3)采用电解法可使酸性废水中的 转经为
转经为 而除去,则阴极的电极反应式为________________________________________。
而除去,则阴极的电极反应式为________________________________________。
-
Ⅰ、氮肥的使用在提高粮食产量的同时,也导致了土 壤、水体污染等环境问题。
壤、水体污染等环境问题。
(1)长期过量使用铵态化肥NH4Cl,易导致土壤酸化,请用化学用语解释原因 
(2)工业上处理氨氮废水的方法是采用电解法将NO3-转化为N2,如图所示
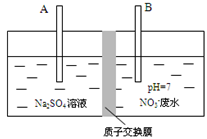
B极的电极反应方程式是_________________________
(3)除去60L废水中的62 mg NO3-后, 废水的pH= 。
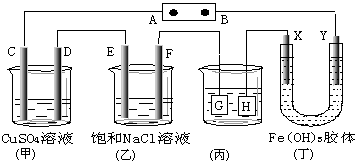
Ⅱ、如下图所示C、D、E、F、X、Y都是惰性电极。将电源接通后,向(乙)中滴入酚酞溶液,在 F极附近显红色。
(1)若用甲醇、空气燃料电池作电源,电解质为KOH溶液 ,则A极的电极反应式为 。
,则A极的电极反应式为 。
(2)欲用(丙)装置给铜镀银,银应该是 电极(填G或H)。
(3)(丁)装置中Y极附近红褐色变 (填深或浅)。
(4)通电一段时间后,C、D、E、F电极均有单质生成,其物质的量之比为 。
-
国家主席习近平在2017年新年祝词上表示,我国将实行“河长制”。水体污染的治理再次成为议的焦点。游离氨或氨盐是水体的常见污染物。
(1)氨氮的处理方法之一是用次氯酸将水中的氨氮(用NH3表示)转化为氮气除去,反应如下:
① 配平该反应方程式:___NH3(aq) +HClO(aq)= N2(g)+ H2O(I)+ HCl (aq),每生成lmol氧化产物,转移的电子数个数为________。
② 已知:NH3(aq)+HClO (aq)=NH2Cl (aq)+H2O (l)△H1=akJ·mol-1
NH2Cl(aq)+HCO(aq) = NHCl2(aq)+H2O(l)△H2=bkJ·mol-1
2NHCl2(aq) + H2O(l)= N2(g)+HClO(aq)+3HCl (aq)△H3=ckJ·mol-1
则上述次氯酸处理水中氨氮反应的△H=_______。(用a、b、c表示)
(2)吹脱法是处理氨氮的另一方法。其原理是利用气体,将反应NH4+ +OH- NH3+H2O中的氨气吹出。
NH3+H2O中的氨气吹出。
① 下列因素,不会影响吹脱法处理效果的是__________(填序号)。
A.温度 B.溶液的pH
C.通入气体的速率和物质的量 D.通入气体的摩尔质量
② 25℃时,向25.00mL 0.1000mol/L (NH4)2SO4溶液中滴加0.1000mol/L NaOH 溶液所得的滴定曲线如图。(不考虑NH3逸出及溶液混合对体积的影响), 则a点的c(NH4+)=____mol/L,b点的c (NH4+) + c ( NH3·H2O) =____ mol/L,下列关于c点的叙述正确的是_____(填序号)。

A. pH = 13
B. c (NH4+) + c(NH3·H2O)=c(Na+)
C. c (NH4+) + c(Na+) + c(H+) =c(SO42-)+ c (OH-)
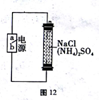
(3)如图所示,利用电解法产生的Cl2也可氧化除去水中的氨氮,实验室用石墨电极电解一定浓度的(NH4)2SO4 与NaCl 混合溶液来模拟。电解时,b为电源____极,阳极的电极反应式为___________

和游离态的
保持平衡状态而存在。将空气直接通入水中,使气相和液相充分接触。水中溶解的游离氨穿过气液界面,向气相转移,从而达到脱除氨的目的。氨氮废水中
和
平衡态的平衡关系有________。
值、空气流量对脱除氨有很大的影响。
值、空气流量对脱除氨影响如图所示。由图可以看出,空气流量一定时,
时,吹脱率随着
增加而增加,请用化学平衡移动原理解释原因________。

的氨氮废水还可以用电化学沉淀与阴极氧化协同去除水中的氨氮,装置如图所示。电解过程中,石墨毡电极产生
,在通入
的情况,又产生
,以氧化水中的
,同时
还可以通过生成
沉淀而持续被除去。

转化为
的离子方程式是________。
大于
不利于
的生成,原因是________。















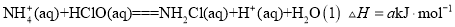

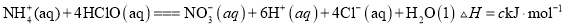
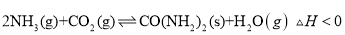 。
。



