-
已知2H2(g)+O2(g)=2H2O(l) ΔH=-571.6kJ/mol
H2O(l)=H2O(g) ΔH=+44kJ/mol
下列说法中,不正确的是( )
A.H2的燃烧热为285.8kJ/mol
B.2H2(g)+O2(g)=2H2O(g) ΔH=-483.6kJ/mol
C.1molH2完全燃烧生成气态水放出的热量等于285.8kJ
D.形成1molH2O的化学键释放的总能量大于断裂1molH2和0.5molO2的化学键所吸收的总能量
高二化学单选题中等难度题查看答案及解析
-
已知:2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ·mol-1
2H2O(g)=2H2(g)+O2(g) ΔH=+483.6 kJ·mol-1
现有1g液态H2O,蒸发时吸收的热量是( )
A.2.44 kJ B.4.88 kJ C.44.0 kJ D.88.0 kJ
高二化学选择题简单题查看答案及解析
-
已知H2(g)+
O2(g)═H2O(l)△H=-285.8kJ/mol.下列说法不正确的是( )
A.H2的燃烧热为285.8 kJ/mol
B.2H2(g)+O2(g)═2H2O(l)△H=-571.6 kJ/mol
C.1 mol H2完全燃烧生成气态水放出的热量大于285.8 kJ
D.形成1 mol H2O的化学键释放的总能量大于断裂1 mol H2和0.5 mol O2 的化学键所吸收的总能量高二化学选择题中等难度题查看答案及解析
-
已知:2H2(g)+O2(g) === 2 H2O (l) △H= -571.6 kJ· mol-1,下列说法正确的是
A.2 L液态水分解成2L氢气与1L氧气吸收571.6 kJ热量
B.2 mol氢气与1mol氧气反应生成2mol气态水放出热量大于571.6 kJ
C.在相同条件下,2 mol氢气与1mol氧气的能量总和大于2mol液态水的能量
D.使用催化剂能降低该反应的活化能使反应放出得热量小于571.6 kJ
高二化学选择题简单题查看答案及解析
-
已知下列热化学方程式:
2H2(g) + O2(g)=2H2O(l) △H=-571.6 kJ/mol
C3H8(g) + 5O2(g)=3CO2(g) +4 H2O(g ) △H=-2044.0 kJ/mol
(1)氢气的燃烧热是__________________。
(2)已知:H2O(l)=H2O(g ) △H=+44.0 kJ/mol写出丙烷(C3H8)燃烧生成二氧化碳和液态水的热化学方程式:_____________________。
(3)实验测得H2和C3H8的混合气体共3mol,完全燃烧生成液态水时放热2791.6 kJ,计算混合气体中H2和C3H8的体积比是________________。
(4)C3H8(g) + 5O2(g)=3CO2(g) +4 H2O(g ) △H=-2044.0 kJ/mol当反应中转移10mol电子时,燃烧的丙烷(C3H8)的质量是________ g,生成的CO2在标准状况下的体积是_________ L。
高二化学填空题困难题查看答案及解析
-
(8分)、已知:2H2(g)+O2(g)=2 H2O(l) △H= -571.6 kJ·mol-1
H2(g)+1/2O2(g)=H2O(g) ΔH= -241.8 kJ/mol
C3H4(g)+4O2(g) = 3CO2(g) +2H2O(g) △H= -2100.0 kJ·mol-1
根据上面两个热化学方程式回答下列问题:
(1) 的燃烧热为________;
(2)1mol和2molC3H4 组成的混合气体完全燃烧生成液态水时释放的热量为________
________;
(3)现有和C3H4的混合气体共5mol,完全燃烧生成CO2和气态水时,则放出热量(Q)的取值范围是________;若生成CO2和H2O的物质的量相等,则放出的热量是________。
高二化学填空题简单题查看答案及解析
-
已知:①2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ/mol-1②H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1。下列说法中错误的是 ( )
A. ①式表示25 ℃,101 kpa时,2 mol H2和1 mol O2完全燃烧生成2 mol H2O(l)放热571.6 kJ
B. 2H2(g)+O2(g)===2H2O(g)中ΔH大于-571.6 kJ·mol-1
C. 将含1 mol NaOH的水溶液与50 g 98%的硫酸溶液混合后放出的热量为57.3 kJ
D. 将含1 mol NaOH的稀溶液与含1 mol CH3COOH的稀溶液混合后放出的热量小于57.3 kJ
高二化学单选题简单题查看答案及解析
-
已知:①2H2(g)+O2(g)=2H2O(l) ΔH=-571.6 kJ/mol-1②H+(aq)+OH-(aq)=H2O(l) ΔH=-57.3 kJ·mol-1。下列说法中错误的是 ( )
A.①式表示25 ℃,101 kpa时,2 mol H2和1 mol O2完全燃烧生成2 mol H2O(l)放热571.6 kJ
B.2H2(g)+O2(g)===2H2O(g)中ΔH大于-571.6 kJ·mol-1
C.将含1 mol NaOH的水溶液与50 g 98%的硫酸溶液混合后放出的热量为57.3 kJ
D.将含1 mol NaOH的稀溶液与含1 mol CH3COOH的稀溶液混合后放出的热量小于57.3 kJ
高二化学选择题简单题查看答案及解析
-
已知2H2(g)+O2(g)═2H2O(l)△H1=-571.6kJ•mol-1,则关于化学方程式:H2O(l)═H2(g)+
O2(g)△H2=a的说法中正确的是( )
A.方程式中化学计算可以表示分子数
B.a>0
C.a=-285.9kJ•mol-1
D.△H2表示18g水分解时放出的热量高二化学选择题中等难度题查看答案及解析
-
下列热化学方程式书写正确的是( )
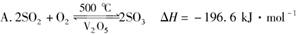
B.H2(g)+1/2O2(g)===H2O(l) ΔH=-285.8 kJ·mol-1
C.2H2(g)+O2(g)===2H2O(l) ΔH=-571.6 kJ
D.C(s)+O2(g)===CO2(g) ΔH=+393.5 kJ·mol-1
高二化学选择题简单题查看答案及解析