下列关于电解质溶液的说法正确的是
A.0.1 L 0.5 mol·L-1 CH3COOH溶液中含有的H+数为0.05NA
B.室温下,稀释0.1 mol·L-1 CH3COOH溶液,溶液的导电能力增强
C.向0.1 mol·L-1 CH3COOH溶液中加入少量水,溶液中所有离子浓度均减小
D.CH3COOH溶液加水稀释后,溶液中的值减小
高二化学单选题简单题
下列关于电解质溶液的说法正确的是
A.0.1 L 0.5 mol·L-1 CH3COOH溶液中含有的H+数为0.05NA
B.室温下,稀释0.1 mol·L-1 CH3COOH溶液,溶液的导电能力增强
C.向0.1 mol·L-1 CH3COOH溶液中加入少量水,溶液中所有离子浓度均减小
D.CH3COOH溶液加水稀释后,溶液中的值减小
高二化学单选题简单题
下列关于电解质溶液的说法正确的是
A.0.1 L 0.5 mol·L-1 CH3COOH溶液中含有的H+数为0.05NA
B.室温下,稀释0.1 mol·L-1 CH3COOH溶液,溶液的导电能力增强
C.向0.1 mol·L-1 CH3COOH溶液中加入少量水,溶液中所有离子浓度均减小
D.CH3COOH溶液加水稀释后,溶液中的值减小
高二化学单选题简单题查看答案及解析
NA代表阿伏加德罗常数的值。下列叙述正确的是( )
A. 14 g乙烯和丙烯混合气体中的氢原子数为2NA
B. 0.1 L 0.5 mol/L CH3COOH溶液中含有的H+数为0.05NA
C. 60g丙醇中存在的共价键总数为10NA
D. 标准状况下,2.24 L CCl4含有的共价键数为0.4NA
高二化学单选题中等难度题查看答案及解析
下列有关电解质溶液的说法正确的是( )
A. 向0.1 mol·L-1 CH3COOH溶液中加入少量水,溶液中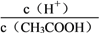 减小
减小
B. 将CH3COONa溶液从20 ℃升温至30 ℃,溶液中 增大
增大
C. 在pH=8的NaB溶液中:c(Na+)﹣c(B﹣)=9.9×10﹣8molL﹣1
D. 向AgCl、AgBr的饱和溶液中加入少量AgNO3,溶液中不变
高二化学单选题中等难度题查看答案及解析
下列关于0.05mol /L的K2SO4溶液的说法中,正确的是
A.1L溶液中含有K+、SO42-总数为0.03NA
B.1L溶液中含有K+数目是0.1NA
C.1 L溶液中K+的浓度是0.20 mol / L
D.2 L溶液中含有SO42-的浓度是0.3mol / L
高二化学选择题简单题查看答案及解析
高二化学选择题中等难度题查看答案及解析
25℃时,有下列四种溶液:①0.1mol/L的CH3COOH溶液;②pH=13的NaOH溶液;③0.05mol/L的H2SO4溶液;④0.1mol/L的Na2CO3溶液。则下列有关说法中正确的是( )
A.溶液④显碱性,用离子方程式解释其原因可表示成:CO32-+2H2OH2CO3+2OH-
B.在上述四种溶液中,pH由大到小的顺序为:②④①③
C.将该温度下amL的溶液②与bmL的溶液③混合,所得混合溶液的pH=7,则a:b=1:2
D.若将溶液④和Al2(SO4)3溶液混合,一定可观察到有白色胶状沉淀和无色气体生成
高二化学选择题困难题查看答案及解析
下列说法中正确的是( )
A. 常温下,在pH=3的CH3COOH溶液和pH=3的H2SO4溶液中,水的电离程度前者小于后者
B. 0.1 mol•L﹣1 CH3COONa溶液与0.05 mol•L﹣1盐酸等体积混合后的酸性溶液中:c(Cl﹣)>c(CH3COO﹣)>c(CH3COOH)>c(H+)
C. 某温度时水的离子积常数KW=10-13,若将此温度下pH=11的NaOH溶液a L与pH=1的稀硫酸b L混合,若所得混合液pH=2,则a∶b=9 ∶2(忽略溶液混合后的体积变化)
D. 常温下,在10 mL pH=12的氢氧化钠溶液中加入pH=2的HA至pH刚好等于7,所得溶液体积V(总)≥20 mL(忽略溶液混合后的体积变化)
高二化学选择题困难题查看答案及解析
设NA为阿伏加德罗常数的值。下列说法正确的是
A.常温下,0.05 mol·L-1 Fe2(SO4)3溶液中含Fe3+数目为0.1NA
B.1 mol氯气和足量NaOH溶液反应转移的电子数目为2NA
C.常温下,9.2 g NO2和N2O4的混合气体中含有的氮原子数目为0.2 NA
D.标准状况下,22.4 L甲苯中含C-H数目为8 NA
高二化学单选题中等难度题查看答案及解析
高二化学选择题中等难度题查看答案及解析
NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.0.1L0.5mol/LCH3COOH溶液中含有的氢离子数为0.05NA
B.密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA
C.1L 0.1mol·L-1的NaHCO3溶液中HCO3-和CO32-离子数之和为0.1NA
D.某电池的总反应为Fe+2Fe3+=3Fe2+,当有5.6gFe溶解时电路中有0.2mol e-通过
高二化学单选题中等难度题查看答案及解析