-
(1)海水中有丰富的食盐资源,工业上以粗食盐水(含少量Ca2+、Mg2+杂质)、氨、石灰石等为原料,可以制备Na2CO3。流程如下:
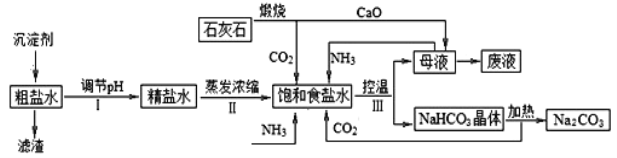
请回答:
①粗盐精制过程中加入的沉淀剂是石灰乳和纯碱,加入顺序是_____。
②上述流程中循环使用的物质是____。
③上图中制得的饱和食盐水还可用于氯碱工业,NaCl 溶液的电解产物可用于生产盐酸、漂白粉、氢氧化钠等产品。工业上电解饱和食盐水的离子方程式为_____。
④氨气可用电解法合成,其原料转化率大幅度提高, 有望代替传统的工业合成氨工艺。电解法合成氨的两种原理及装置如图 1 和图 2 所示。
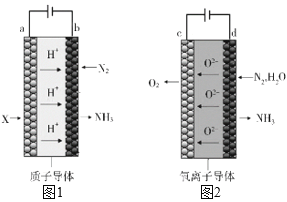
图 1 中,a 电极上通入的X 为_____。图 2 中,d 电极上的电极反应式为_________。
(2)海水中有丰富的锂资源,我国科学家研发出利用太阳能从海水中提取金属锂的技术,提取原理如图 3 所示:

图 3
①金属锂在电极_____(填“A”或“B”)上生成。
②阳极产生两种气体单质,电极反应式是_____。
③某种锂离子二次电池的总反应为:FePO4(s)+Li(s) LiFePO4(s) , 装置如下图所示(a 极材料为金属锂和石墨的复合材料)。下列说法不正确的是_____。
LiFePO4(s) , 装置如下图所示(a 极材料为金属锂和石墨的复合材料)。下列说法不正确的是_____。
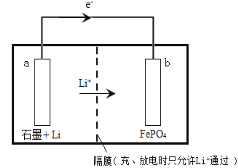
A.图中 e-及 Li+移动方向说明该电池处于放电状态
B.该电池中a 极不能接触水溶液
C.充电时 a 极连接外接电源的正极
D.充电时,b 极电极反应式为:LiFePO4-e-= Li++ FePO
-
海洋中资源丰富,以海水为原料可制得一系列产品,如下图所示:

下列有关说法正确的是
A.第①步除去粗盐SO42-、Ca2+、Mg2+、Fe3+等杂质离子,加入的药品顺序为: Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B.将第②步结晶出的MgCl2 6H2O在空气中加热分解制备无水MgCl2
6H2O在空气中加热分解制备无水MgCl2
C.在第③④⑤步中溴元素均被氧化
D.电解饱和食盐水时,在阴极区生成NaOH
-
海洋中资源丰富,以海水为原料可制得一系列产品,如下图所示。下列说法中正确的是
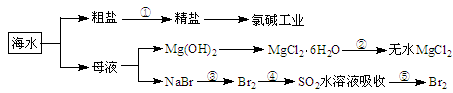
A.第①步除去粗盐中SO42-、Ca2+、Mg2+、Fe3+等杂质离子,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B.将第②步结晶出的MgCl2 6H2O在空气中加热分解制备无水MgCl2
6H2O在空气中加热分解制备无水MgCl2
C.在第③④⑤步中溴元素均被氧化
D.电解饱和食盐水时,在阴极区生成NaOH
-
海水中蕴含丰富的资源,对海水进行综合利用,可制备一系列物质(见下图),下列说法正确的是( )
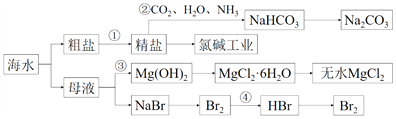
A. 步骤①中,除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入试剂及相关操作顺序可以是:NaOH溶液→BaCl2溶液→Na2CO3溶液→盐酸→过滤
B. 步骤②中反应利用的原理是:相同条件下NaHCO3的溶解度比NaCl小
C. 步骤③在工业上通过向母液中加NaOH固体实现
D. 步骤④利用了Br2的挥发性、还原性,该步的作用是富集
-
海水资源的利用具有非常广阔的前景。
(1)海水淡化的主要方法有(只写出1种即可)________。
(2)海水中丰富的氯化钠是重要的化工原料,如电解饱和食盐水可以制备多种化工产品。
①用石墨电极电解饱和食盐水时,阴极的电极反应式是
_______________________________________________________________。
②常温下,用石墨电极电解饱和食盐水,当阴极产生的气体体积为112 mL(已折算为标准状况)时停止电解,此时溶液体积为1 L,若忽略气体的溶解,最终溶液的pH约为________。
-
食盐是日常生活必需品,也是重要的化工原料。
(1)某种粗盐含有少量Ca2+、Mg2+、Fe3+、SO42-等杂质离子,实验室提纯该粗盐的流程如下:
粗盐溶解
 滤液
滤液
 纯NaCl
纯NaCl
提供的试剂有:a.饱和Na2CO3溶液 b.饱和K2CO3溶液 c.NaOH溶液 d.BaCl2溶液 e.Ba(NO3)2溶液
欲除去粗盐溶液中的Ca2+、Mg2+、Fe3+、SO42-离子,需依次加入三种试剂,顺序依次为
(填序号); ;
(2)食盐是工业上生产氯气和烧碱的重要原料。下图是工业上电解饱和食盐水的离子交换膜电解槽示 意图(阳极用金属钛网制成,阴极由碳钢网制成)。

①F电极是 (填阴极或阳极);G处进口的物质是 ;
电解总反应的离子方程式为: 。
②通电几分钟后,如果将直流电源的正负极与电极接反,在电极F附近可以观察到的现象是 。
(3)采用无膜电解槽电解饱和食盐水(离子交换膜更换为搅拌器),可制取次氯酸钠溶液作消毒液,制取消毒液的离子反应方程式为 ,当收集到22.4L标准状况下的H2时,理论上所得混合溶液中次氯酸钠的质量最多为 。
-
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。下列有关说法不正确的是( )
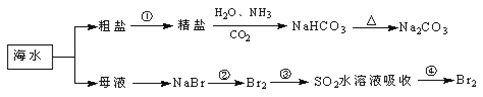
A. 除去粗盐中杂质(Mg2+、SO42﹣、Ca2+),加入的药品顺序为:Na2CO3溶液→BaCl2溶液→NaOH溶液→过滤后加盐酸
B. 用澄清的石灰水不可鉴别NaHCO3和Na2CO3
C. 在第②、④步骤中,溴元素均被氧化
D. 从第②步到第④步的目的是为了富集
-
海洋中有丰富的食品、矿产、能源、药物和水产资源,下图为海水利用的部分过程。
下列有关说法正确的是
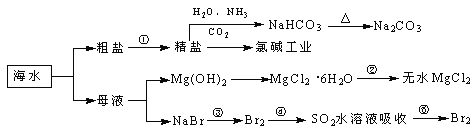
A. 过程①中除去粗盐中的SO42-、Ca2+、Mg2+、Fe3+等杂质,加入的药品顺序为:Na2CO3溶液→NaOH溶液→BaCl2溶液→过滤后加盐酸
B. 用澄清的石灰水可鉴别NaHCO3和Na2CO3
C. 过程②中结晶出的MgCl2·6H2O要在HCl氛围中加热脱水制得无水MgCl2
D. 工业上通过电解饱和MgCl2溶液制取金属镁
-
海水中蕴藏着丰富的资源.海水综合利用的流程图如下:
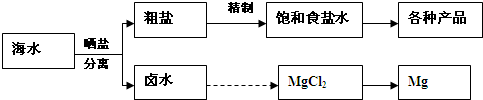
粗盐各种产品卤水MgCl2Mg晒盐分离海水精制饱和食盐水
(1)用NaCl做原料可以得到多种产品.
①工业上由NaCl制备金属钠的化学方程式是________.
②实验室用惰性电极电解100mL NaCl溶液,若阴阳两极均得到112mL气体(标准状况),则所得溶液的pH为________(忽略反应前后溶液的体积变化).
③电解氯化钠稀溶液可制备“84”消毒液,通电时氯气被溶液完全吸收,若所得消毒液仅含一种溶质,写出相应的化学方程式________.
(2)分离出粗盐后的卤水中蕴含着丰富的镁资源,经转化后可获得MgCl2粗产品.从卤水中提取镁的步骤为:
a.将海边大量存在的贝壳煅烧成石灰,并将石灰制成石灰乳;
b.将石灰乳加入到海水沉淀池中经过滤得到Mg(OH)2沉淀;
c.在Mg(OH)2沉淀中加入盐酸得到MgCl2溶液,再经蒸发结晶得到MgCl2•6H2O;
d.将MgCl2•6H2O在一定条件下加热得到无水MgCl2;
e.电解熔融的氯化镁可得到Mg.
①步骤d中的“一定条件”指的是________,目的是________.
②上述提取镁的流程中,为了降低成本,减少污染,可以采取很多措施,请写出其中一点________.
③有同学认为:步骤b后可加热Mg(OH)2得到MgO,再电解熔融的MgO制金属镁,这样可简化实验步骤,体现实验的简约性原则.你同意该同学的想法吗?________,请说出你同意或不同意的理由________.
-
海水是取之不尽的化工原料资源库,从海水中可提取各种化工原料。下列是工业上对海水的几项综合利用的示意图:
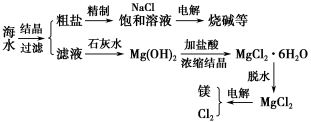
试回答下列问题:
(1)粗盐中含有Ca2+、Mg2+、SO42-等杂质,精制时所用试剂为:A.盐酸;B.BaCl2溶液;C.NaOH溶液;D.Na2CO3溶液。加入试剂的顺序是________________________________________________________________。
(2)电解饱和食盐水时,与电源正极相连的电极上发生的反应为________。与电源负极相连的电极附近溶液pH________(填“变大”“不变”或“变小”)。若1 mol电子的电量为96 500 C,则用电流强度为100 A的稳恒电流持续电解3分13秒,则在两极上共可收集到气体________mL(STP)。若保证电解后饱和食盐水的浓度不变,则可采取的方法是________________________________________________________________。
(3)由MgCl2·6H2O晶体脱水制无水MgCl2时,MgCl2·6H2O晶体在________气氛中加热脱水,该气体的作用是_____________________________________________________。
(4)电解无水MgCl2所得的镁蒸气可以在下列________气体中冷却。
A.H2 B.N2 C.CO2 D.O2



LiFePO4(s) , 装置如下图所示(a 极材料为金属锂和石墨的复合材料)。下列说法不正确的是_____。








